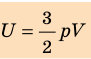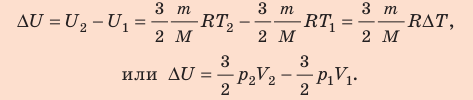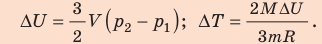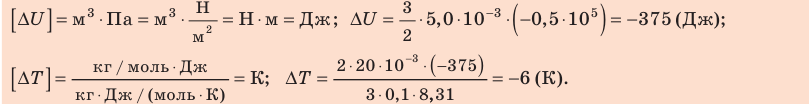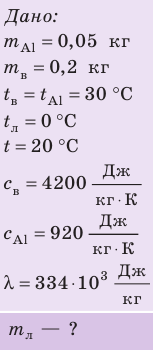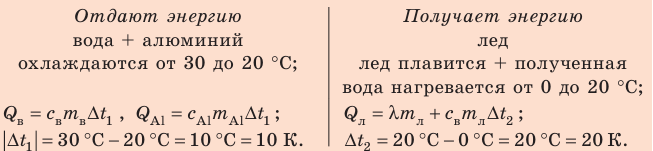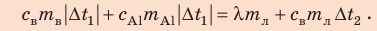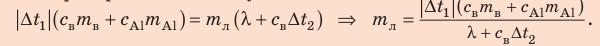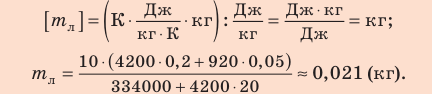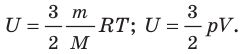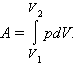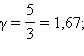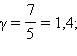Содержание:
Внутренняя энергия:
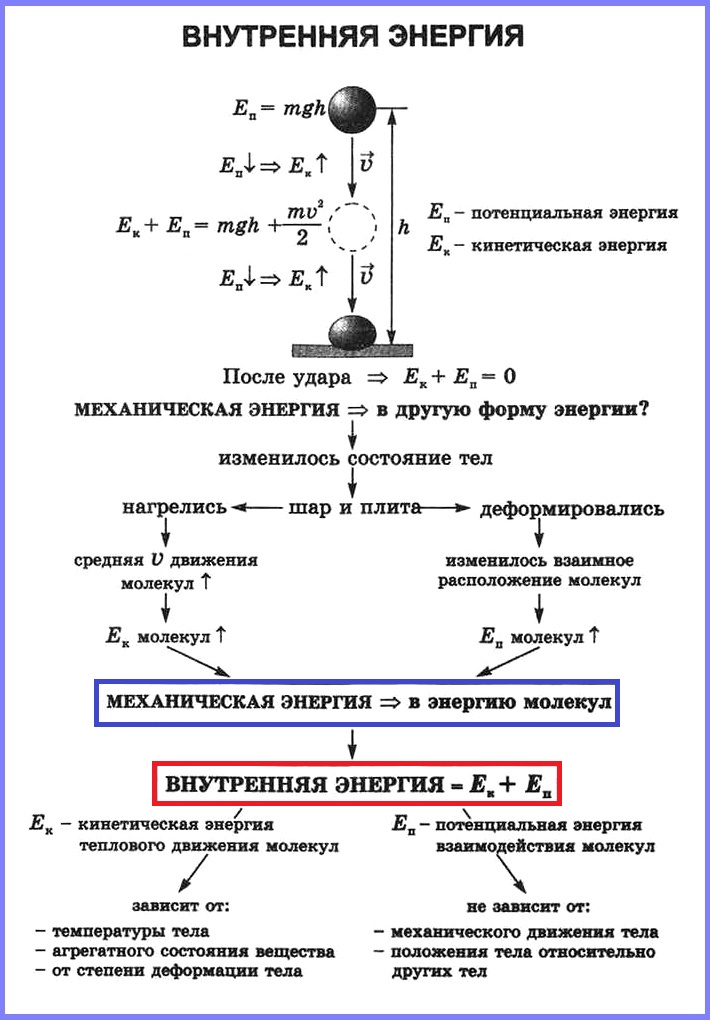
Вы знаете, что движущееся тело обладает кинетической энергией. А если оно еще и взаимодействует с другим телом, то обладает потенциальной энергией. Оба вида энергии представляют собой механическую энергию. Они взаимно превращаемы: кинетическая энергия может переходить в потенциальную и наоборот. Кроме того, вы знаете, что любое тело имеет дискретную структуру, т. е. состоит из частиц (атомов, молекул). Частицы находятся в непрерывном хаотическом движении. А частицы жидкости и твердого тела еще и взаимодействуют между собой. Следовательно, частицы обладают кинетической, а частицы жидкости и твердых тел — еще и потенциальной энергией. Сумма кинетической и потенциальной энергий всех частиц тела называется внутренней энергией. Внутренняя энергия измеряется в джоулях. Чем отличается внутренняя энергия от механической? В чем ее особенности? Может ли механическая энергия переходить во внутреннюю?
Для ответа на эти вопросы рассмотрим пример. Шайба, двигавшаяся горизонтально по льду (рис. 1), остановилась. Как изменилась ее механическая энергия относительно льда?
Кинетическая энергия шайбы уменьшилась до нуля. Положение шайбы над уровнем льда не изменилось, шайба не деформировалась. Значит, изменение потенциальной энергии равно нулю. Означает ли это, что се механическая (кинетическая) энергия исчезла бесследно? Нет. Механическая энергия шайбы перешла во внутреннюю энергию шайбы и льда.
А может ли внутренняя энергия тела, как механическая, быть равной нулю? Движение частиц, из которых состоит тело, не прекращается даже при самых низких температурах. Значит, тело всегда (подчеркиваем, всегда) обладает некоторым запасом внутренней энергии. Его можно либо увеличить, либо уменьшить — и только!
Велико ли значение внутренней энергии тела? Энергия одной частицы, например кинетическая, в силу незначительности ее массы чрезвычайно мала. Расчеты для средней энергии поступательного движения молекулы кислорода показывают, что ее значение при комнатной температуре
Главные выводы:
- Независимо от того, есть у тела механическая энергия или нет, оно обладает внутренней энергией.
- Внутренняя энергия тела равна сумме кинетической и потенциальной энергий частиц, из которых оно состоит.
- Внутренняя энергия тела всегда не равна нулю.
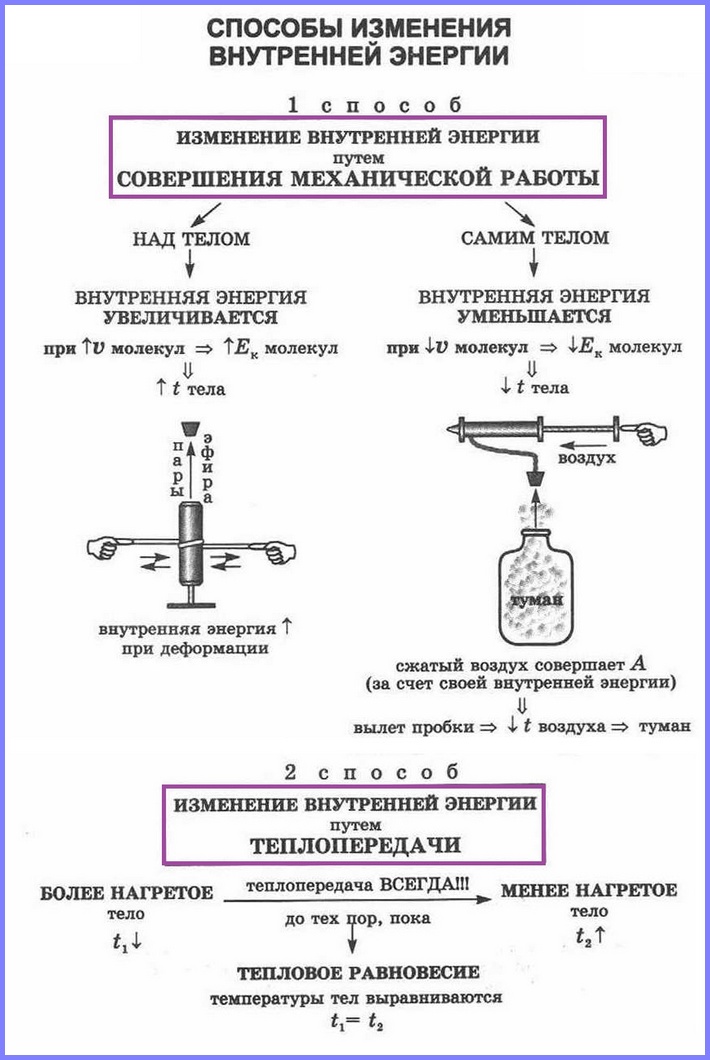
Способы изменения внутренней энергии
Чтобы изменить механическую энергию тела, надо изменить скорость его движения, взаимодействие с другими телами или взаимодействие частей тела. Вы уже знаете, что это достигается совершением работы.
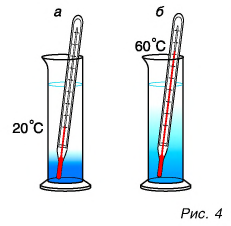
Как можно изменить (увеличить или уменьшить) внутреннюю энергию тела? Рассуждаем логически. Внутренняя энергия определяется как сумма кинетической и потенциальной энергий частиц. Значит, нужно изменить либо скорость движения частиц, либо их взаимодействие (изменить расстояния между ними). Очевидно, можно изменить и скорость, и расстояния между частицами одновременно. Изменить скорость частиц тела можно, увеличив или уменьшив его температуру. Действительно, наблюдения за диффузией показывают, что быстрота ее протекания увеличивается при нагревании (рис. 4, а, б).
Значит, увеличивается средняя скорость движения частиц, а следовательно, их средняя кинетическая энергия. Отсюда следует важный вывод: температура является мерой средней кинетической энергии частиц.
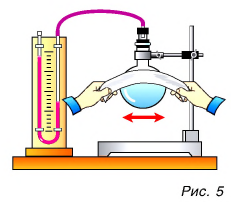
Как изменить кинетическую энергию частиц тела? Существуют два способа. Рассмотрим их на опытах. Будем натирать колбу с воздухом полоской сукна (рис. 5).
Через некоторое время уровень жидкости в правом колене манометра (см. рис. 5) опустится, т. е. давление воздуха в колбе увеличится. Это говорит о нагревании воздуха. Значит, увеличилась скорость движения и кинетическая энергия его молекул, а следовательно, и внутренняя энергия. Но за счет чего? Очевидно, за счет совершения механической работы при трении сукна о колбу. Нагрелась колба, а от нее — газ.
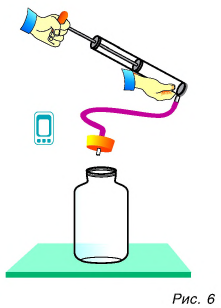
Проведем еще один опыт. В толстостенный стеклянный сосуд нальем немного воды (чайную ложку для увлажнения воздуха в нем. Насосом (рис. 6) будем накачивать в сосуд воздух. Через несколько качков пробка вылетит, а в сосуде образуется туман. Из наблюдений за окружающей средой мы знаем, что туман появляется тогда, когда после теплого дня наступает холодная ночь. Образование тумана в сосуде свидетельствует об охлаждении воздуха, т. е. об уменьшении его внутренней энергии. Но почему уменьшилась энергия? Потому что за ее счет совершена работа по выталкиванию пробки из сосуда.
Сравним результаты опытов. В обоих случаях изменилась внутренняя энергия газа, но в первом опыте она увеличилась, так как работа совершалась внешней силой (над колбой с газом), а во втором — уменьшилась, ибо работу совершала сила давления самого газа.
А можно ли, совершая работу, изменить потенциальную энергию взаимодействия молекул?
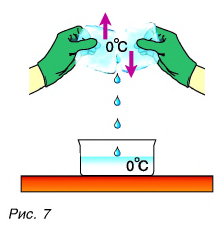
Опять обратимся к опыту. Два куска льда при О °C будем тереть друг о друга (рис. 7).
Лед превращается в воду, при этом температура воды и льда остается постоянной, равной О °C (см. рис. 7). На что тратится механическая работа силы трения?
Конечно же, на изменение внутренней энергии!
Но кинетическая энергия молекул не изменилась, так как температура не изменилась. Лед превратился в воду. При этом изменились силы взаимодействия молекул 
Совершение механической работы — один из способов изменения внутренней энергии тела.
А есть ли возможность изменить внутреннюю энергию тела, не совершая механическую работу?
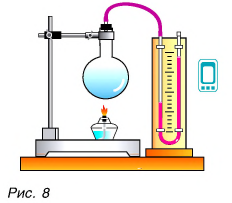
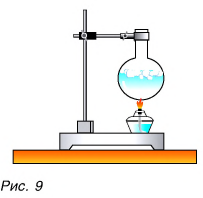
Да, есть. Нагреть воздух в колбе (рис. 8), расплавить лед (рис. 9) можно с помощью спиртовки, передав и воздуху, и льду теплоту. В обоих случаях внутренняя энергия увеличивается.
При охлаждении тел (если колбы со льдом и воздухом поместить в морозильник) их внутренняя энергия уменьшается. Теплота от тел передается окружающей среде.
Процесс изменения внутренней энергии тела, происходящий без совершения работы, называется теплопередачей (теплообменом).
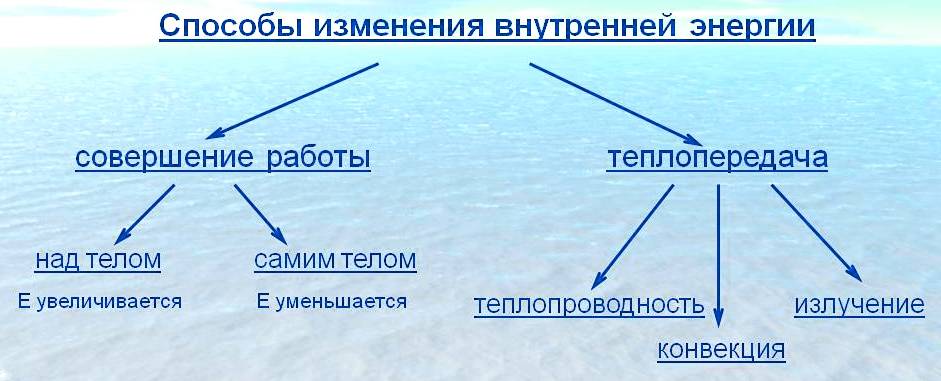
Таким образом, совершение механической работы и теплопередача — два способа изменения внутренней энергии тела.
Величину, равную изменению внутренней энергии при теплопередаче, называют количеством теплоты (обозначается Q). Единицей количества теплоты, как работы и энергии, в СИ является 1 джоуль.
Для любознательных:
Физики XVIII в. и первой половины XIX в. рассматривали теплоту не как изменение энергии, а как особое вещество — теплород — жидкость (флюид), которая может перетекать от одного тела к другому. Если тело нагревалось, то считалось, что в него вливался теплород, а если охлаждалось — то выливался. При нагревании тела расширяются. Это объяснялось тем, что теплород имеет объем. Но если теплород — вещество, то тела при нагревании должны увеличивать свою массу. Однако взвешивания показывали, что масса тела не менялась. Поэтому теплород считали невесомым. Теорию теплорода поддерживали многие ученые, в том числе и такой гениальный ученый, как Г. Галилей. Позже Дж. Джоуль на основании проведенных им опытов пришел к выводу, что теплород не существует и что теплота есть мера изменения кинетической и потенциальной энергий движущихся частиц тела.
В дальнейшем выражение «сообщить телу количество теплоты» мы будем понимать как «изменить внутреннюю энергию тела без совершения механической работы, т. е. путем теплообмена». А выражение «нагреть тело» будем понимать как «повысить его температуру» любым из двух способов.
Главные выводы:
- Внутреннюю энергию тела можно изменить путем совершения механической работы или теплопередачи (теплообмена).
- Изменение внутренней энергии при нагревании или охлаждении тела при постоянном объеме связано с изменением средней кинетической энергии его частиц.
- Изменение внутренней энергии тела при неизменной температуре связано с изменением потенциальной энергии его частиц.
Основы термодинамики
МКТ стала общепризнанной на рубеже XIX и XX веков. Задолго до ее создания исследованием тепловых процессов занималась термодинамика — раздел физики, изучающий превращение внутренней (тепловой) энергии в другие виды энергии и наоборот, а также количественные соотношения при таких превращениях.
- Заказать решение задач по физике
Внутренняя энергия и ее особенности
Внутренняя энергия макроскопического тела определяется характером движения и взаимодействия всех микрочастиц, из которых состоит тело (система тел). Таким образом, к внутренней энергии следует отнести:
- кинетическую энергию хаотического (теплового) движения частиц вещества (атомов, молекул, ионов);
- потенциальную энергию взаимодействия частиц вещества;
- энергию взаимодействия атомов в молекулах (химическую энергию);
- энергию взаимодействия электронов и ядра в атоме и энергию взаимодействия нуклонов в ядре (внутриатомную и внутриядерную энергии).
Однако для описания тепловых процессов важно не столько значение внутренней энергии, как ее изменение. При тепловых процессах химическая, внутриатомная и внутриядерная энергии практически не изменяются. Именно поэтому внутренняя энергия в термодинамике определяется как сумма кинетических энергий хаотического (теплового) движения частиц вещества (атомов, молекул, ионов), из которых состоит тело, и потенциальных энергий их взаимодействия.
Внутреннюю энергию обозначают символом U.
Единица внутренней энергии в СИ — джоуль: [U]=1 Дж (J).
Особенности внутренней энергии идеального газа
- Атомы и молекулы идеального газа практически не взаимодействуют друг с другом, поэтому внутренняя энергия идеального газа равна кинетической энергии поступательного и вращательного движений его частиц.
- Внутренняя энергия данной массы идеального газа прямо пропорциональна его абсолютной температуре. Докажем данное утверждение для одноатомного газа. Атомы такого газа движутся только поступательно, поэтому, чтобы определить его внутреннюю энергию, следует среднюю кинетическую энергию поступательного движения атомов умножить на количество атомов:
Итак, для одноатомного идеального газа:
. Используя уравнение состояния
, выражение для внутренней энергии идеального одноатомного газа можно представить так:
- Внутренняя энергия — функция состояния системы, то есть она однозначно определяется основными макроскопическими параметрами (p, V, T), характеризующими систему. Независимо от того, каким образом система переведена из одного состояния в другое, изменение внутренней энергии будет одинаковым.
- Внутреннюю энергию можно изменить двумя способами: совершением работы и теплопередачей.
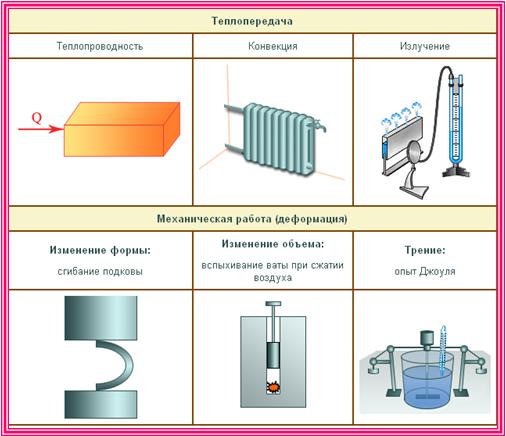
Какие существуют виды теплопередачи
Теплопередача (теплообмен) — процесс изменения внутренней энергии тела или частей тела без совершения работы. Процесс теплопередачи возможен только при наличии разности температур. Самопроизвольно тепло всегда передается от более нагретого тела к менее нагретому. Чем больше разность температур, тем быстрее — при прочих равных условиях — протекает процесс передачи тепла.
| Виды теплопередачи | ||
|---|---|---|
| Теплопроводность | Конвекция | Излучение |
|
Вид теплопередачи, который обусловлен хаотическим движением частиц вещества и не сопровождается переносом этого вещества. Лучшие проводники тепла — металлы, плохо проводят тепло дерево, стекло, кожа, жидкости (за исключением жидких металлов); самые плохие проводники тепла — газы. Передача энергии от горячей воды к батарее отопления, от поверхности воды до ее нижних слоев и т. д. происходит благодаря теплопроводности. |
Вид теплопередачи, при котором тепло переносится потоками жидкости или газа. Теплые потоки жидкости или газа имеют меньшую плотность, поэтому под действием архимедовой силы поднимаются, а холодные потоки — опускаются. Благодаря конвекции происходит циркуляция воздуха в помещении, нагревается жидкость в стоящей на плите кастрюле, существуют ветры и морские течения и т. д. В твердых телах конвекция невозможна. | Вид теплопередачи, при котором энергия передается посредством электромагнитных волн. Излучение — универсальный вид теплопередачи: тела всегда излучают и поглощают инфракрасное (тепловое) излучение. Это единственный вид теплообмена, возможный в вакууме (энергия от Солнца передается только излучением). Лучше излучают и поглощают энергию тела с темной поверхностью. |
Как определить количество теплоты
Количество теплоты Q — это физическая величина, равная энергии, которую тело получает (или отдает) в ходе теплопередачи.
Единица количества теплоты в СИ — джоуль: [П] =1 Дж (J).
Из курса физики 8 класса вы знаете, что количество теплоты, которое поглощается при нагревании вещества (или выделяется при его охлаждении), вычисляют по формуле: Q=cm∆Т=cm∆t , где c — удельная теплоемкость вещества; m — масса вещества; 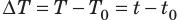
Обратите внимание! Произведение удельной теплоемкости на массу вещества, из которого изготовлено тело, называют теплоемкостью тела: C=cm . Если известна теплоемкость C тела, то количество теплоты, которое получает тело при изменении температуры на ∆T, вычисляют по формуле: Q=C∆T .
| Расчет количества теплоты при фазовых переходах | |
|---|---|
| Кристаллическое состояние ↔ Жидкое состояние | Жидкое состояние ↔ Газообразное состояние |
|
Температуру, при которой происходят фазовые переходы «кристалл → жидкость» и «жидкость → кристалл», называют температурой плавления. Температура плавления зависит от рода вещества и внешнего давления. Количество теплоты Q, которое поглощается при плавлении кристаллического вещества (или выделяется при кристаллизации жидкости), вычисляют по формуле: Q = λm, где m — масса вещества; λ — удельная теплота плавления. |
Фазовые переходы «жидкость → пар» и «пар → жидкость» происходят при любой температуре. Количество теплоты Q, которая поглощается при парообразовании (или выделяется при конденсации), вычисляют по формуле: Q=rm (Q=Lm), где m — масса вещества; r (L) — удельная теплота парообразования при данной температуре (обычно в таблицах представлена удельная теплота парообразования при температуре кипения жидкости). |
| Напомним: и при плавлении, и при кипении температура вещества не изменяется. |
Пример решения задачи №1
Неон массой 100 г находится в колбе объемом 5,0 л. В процессе изохорного охлаждения давление неона уменьшилось с 100 до 50 кПа. На сколько при этом изменились внутренняя энергия и температура неона?
Решение:
Неон — одноатомный газ; для таких газов изменение внутренней энергии равно:
Поскольку охлаждение изохорное, объем неона не изменяется: 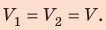
Проверим единицы, найдем значения искомых величин:
Анализ результатов. Знак «–» свидетельствует о том, что внутренняя энергия и температура неона уменьшились, — это соответствует изохорному охлаждению. Ответ: ∆U = –375 Дж; ∆T = –6 К.
Пример решения задачи №2
Внутренний алюминиевый сосуд калориметра имеет массу 50 г и содержит 200 г воды при температуре 30 °С. В сосуд бросили кубики льда при температуре 0 °С, в результате чего температура воды в калориметре снизилась до 20 °С. Определите массу льда. Удельные теплоемкости воды и алюминия: 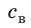
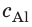
Анализ физической проблемы.
Калориметр имеет такое устройство, что теплообмен с окружающей средой практически отсутствует, поэтому для решения задачи воспользуемся уравнением теплового баланса. В теплообмене участвуют три тела: вода, внутренний сосуд калориметра, лед.
Решение:
Запишем уравнение теплового баланса:
После преобразований получим:
Проверим единицу, найдем значение искомой величины:
Ответ: 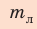
Выводы:
- В термодинамике под внутренней энергией U тела понимают сумму кинетических энергий хаотического движения частиц вещества, из которых состоит тело, и потенциальных энергий их взаимодействия. Внутренняя энергия однозначно определяется основными макроскопическими параметрами (p, V, T), характеризующими термодинамическую систему. Внутреннюю энергию идеального одноатомного газа определяют по формулам:
- Внутреннюю энергию можно изменить двумя способами: совершением работы и теплопередачей. Существует три вида теплопередачи: теплопроводность, конвекция, излучение.
- Физическую величину, равную энергии, которую тело получает или отдает при теплопередаче, называют количеством теплоты (Q): Q=cm∆T = С∆T — количество теплоты, которое поглощается при нагревании тела (или выделяется при его охлаждении); Q = λm — количество теплоты, которое поглощается при плавлении вещества (или выделяется при кристаллизации); Q=rm (Q=Lm) — количество теплоты, которое поглощается при парообразовании вещества (или выделяется при конденсации).
- Теплопроводность в физике
- Конвекция в физике
- Излучение тепла в физике
- Виды излучений в физике
- Машины и механизмы в физике
- Коэффициент полезного действия (КПД) механизмов
- Тепловые явления в физике
- Тепловое движение в физике и его измерение
«Внутренняя энергия»
Существуют два вида механической энергии: кинетическая и потенциальная. Сумма кинетической и потенциальной энергии тела называется его полной механической энергией, которая зависит от скорости движения тела и от его положения относительно того тела, с которым оно взаимодействует. Если тело обладает энергией, то оно может совершить работу. При совершении работы энергия тела изменяется. Значение работы равно изменению энергии. (подробнее о Механической энергии в конспекте «Механическая энергия. Закон сохранения энергии»)
Внутренняя энергия
Если в закрытую пробкой толстостенную банку, дно которой покрыто водой, накачивать, то через какое-то время пробка из банки вылетит и в банке образуется туман. Пробка вылетела из банки, потому что находившийся там воздух действовал на неё с определённой силой. Воздух при вылете пробки совершил работу. Известно, что работу тело может совершить, если оно обладает энергией. Следовательно, воздух в банке обладает энергией.
При совершении воздухом работы понизилась его температура, изменилось его состояние. При этом механическая энергия воздуха не изменилась: не изменились ни его скорость, ни его положение относительно Земли. Следовательно, работа была совершена не за счёт механической, а за счёт другой энергии. Эта энергия — внутренняя энергия воздуха, находящегося в банке.
Внутренняя энергия тела – это сумма кинетической энергии движения его молекул и потенциальной энергии их взаимодействия. Кинетической энергией (Ек) молекулы обладают, так как они находятся в движении, а потенциальной энергией (Еп), поскольку они взаимодействуют. Внутреннюю энергию обозначают буквой U. Единицей внутренней энергии является 1 джоуль (1 Дж). U = Eк + En.
Способы изменения внутренней энергии
Чем больше скорости движения молекул, тем выше температура тела, следовательно, внутренняя энергия зависит от температуры тела. Чтобы перевести вещество из твёрдого состояния в жидкое состояние, например, превратить лёд в воду, нужно подвести к нему энергию. Следовательно, вода будет обладать большей внутренней энергией, чем лёд той же массы, и, следовательно, внутренняя энергия зависит от агрегатного состояния тела.
Внутреннюю энергию можно изменить при совершении работы. Если по куску свинца несколько раз ударить молотком, то даже на ощупь можно определить, что кусок свинца нагреется. Следовательно, его внутренняя энергия, так же как и внутренняя энергия молотка, увеличилась. Это произошло потому, что была совершена работа над куском свинца.
Если тело само совершает работу, то его внутренняя энергия уменьшается, а если над ним совершают работу, то его внутренняя энергия увеличивается.
Если в стакан с холодной водой налить горячую воду, то температура горячей воды понизится, а холодной воды — повысится. В рассмотренном примере механическая работа не совершается, внутренняя энергия тел изменяется путём теплопередачи, о чем и свидетельствует понижение её температуры.
Молекулы горячей воды обладают большей кинетической энергией, чем молекулы холодной воды. Эту энергию молекулы горячей воды передают молекулам холодной воды при столкновениях, и кинетическая энергия молекул холодной воды увеличивается. Кинетическая энергия молекул горячей воды при этом уменьшается.
Теплопередача – это способ изменения внутренней энергии тела при передаче энергии от одной части тела к другой или от одного тела к другому без совершения работы.
Конспект урока по физике в 8 классе «Внутренняя энергия».
Следующая тема: «Виды теплопередачи: теплопроводность, конвекция, излучение».
Наука о тепловых явлениях называется термодинамика. Термодинамика исходит из наиболее общих закономерностей тепловых процессов и свойств макроскопических систем.
При изучении основ термодинамики необходимо помнить следующие определения. Физическая система, состоящая из большого числа частиц — атомов или молекул, которые совершают тепловое движение и, взаимодействуя между собой, обмениваются энергиями, называется термодинамической системой.
Состояние термодинамической системы определяется макроскопическими параметрами, например удельным объемом, давлением, температурой.
Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновесия. Это означает, что в таких системах прекратились все наблюдаемые макроскопические процессы. Важным свойством термодинамически равновесной системы является выравнивание температуры всех ее частей.
Термодинамика рассматривает только равновесные состояния, т.е. состояния, в которых параметры термодинамической системы не меняются со временем.
Если термодинамическая система была подвержена внешнему воздействию, то в конечном итоге она перейдет в другое равновесное состояние. Такой переход называется термодинамическим процессом.
Термодинамическим процессом называется переход системы из начального состояния в конечное через последовательность промежуточных состояний.
Процессы бывают обратимыми и необратимыми.
Обратимым называется такой процесс, при котором возможен обратный переход системы из конечного состояния в начальное через те же промежуточные состояния, чтобы в окружающих телах не произошло никаких изменений. Обратимый процесс является физической абстракцией. Примером процесса, приближающегося к обратимому, является колебание тяжелого маятника на длинном подвесе. В этом случае кинетическая энергия практически полностью превращается в потенциальную, и наоборот. Колебания происходят долго без заметного уменьшения амплитуды ввиду малости сопротивления среды и сил трения.
Любой процесс, сопровождаемый трением или теплопередачей от нагретого тела к холодному, является необратимым. Примером необратимого процесса является расширение газа, даже идеального, в пустоту. Расширяясь, газ не преодолевает сопротивления среды, не совершает работы, но, для того чтобы вновь собрать все молекулы газа в прежний объем, т. е. привести газ в начальное состояние, необходимо затратить работу. Таким образом, все реальные процессы являются необратимыми.
Изменение внутренней энергии газа в процессе теплообмена и совершаемой работы.
Одним из важнейших понятий термодинамики является внутренняя энергия тела. Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения молекулярно-кинетической теории внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом.
Внутренняя энергия – это сумма энергий молекулярных взаимодействий и энергии теплового движения молекул.
В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении. Внутренняя энергия идеального газа зависит только от его температуры и не зависит от объема (закон Джоуля).
Молекулярно-кинетическая теория приводит к следующему выражению для внутренней энергии одного моля идеального одноатомного газа (гелий, неон и др.), молекулы которого совершают только поступательное движение:
Поскольку потенциальная энергия взаимодействия молекул зависит от расстояния между ними, в общем случае внутренняя энергия
U тела зависит наряду с температурой T также и от объема V: U = U(T, V).
Таким образом, внутренняя энергия системы зависит только от её состояния и является однозначной функцией состояния, внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела. Она не зависит от того, каким путем было реализовано данное состояние.
Внутреннюю энергию тела можно изменить разными способами:
- Совершение механической работы.
- Теплообмен.
Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную).
Например, газ подвергается сжатию в цилиндре под поршнем площадью S. Поршень, сжимая газ, движется с некоторой скоростью v. Молекулы газа, беспорядочно двигаясь, ударяются о поршень. После упругого удара молекулы о поршень скорость молекулы возрастает, а значит возрастает и её кинетическая энергия, что приводит к увеличению внутренней энергии газа.
При сжатии газа его внутренняя энергия увеличивается за счет совершения поршнем механической работы. При расширении газа его внутренняя энергия уменьшается, превращаясь в механическую энергию поршня.
При сжатии газа внешние силы совершают над газом некоторую положительную работу A’.
В то же время силы давления, действующие со стороны газа на поршень, совершают работу
A = –A’.
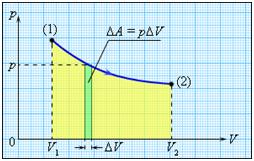
Если объем газа изменился на малую величину ΔV, то газ совершает работу pSΔx = pΔV, где p – давление газа, S – площадь поршня, Δx – его перемещение.
При расширении работа, совершаемая газом, положительна, при сжатии – отрицательна.
В общем случае при переходе из некоторого начального состояния (1) в конечное состояние (2) работа газа выражается формулой:
или в пределе при ΔVi → 0: 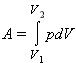
Работа численно равна площади под графиком процесса на диаграмме (p, V):
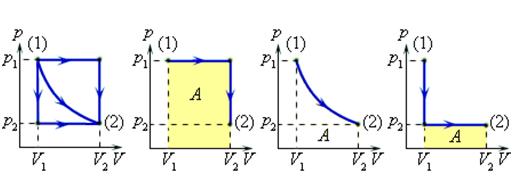
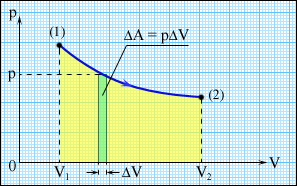
Величина работы зависит от того, каким путем совершался переход из начального состояния в конечное. На рис. 2 изображены три различных процесса, переводящих газ из состояния (1) в состояние (2). Во всех трех случаях газ совершает различную работу.
Рисунок 2.
Три различных пути перехода из состояния (1) в состояние (2).
Во всех трех случаях газ совершает разную работу, равную площади под графиком процесса.
Процессы, изображенные на рис. 2, можно провести и в обратном направлении; тогда работа A просто изменит знак на противоположный.
Процессы которые можно проводить в обоих направлениях, называются обратимыми.
В отличие от газа, жидкости и твердые тела мало изменяют свой объем, так что во многих случаях работой, совершаемой при расширении или сжатии, можно пренебречь. Однако, внутренняя энергия жидких и твердых тел также может изменяться в результате совершения работы. При механической обработке деталей (например, при сверлении) они нагреваются. Это означает, что изменяется их внутренняя энергия.
Внутренняя энергия тела может изменяться не только в результате совершаемой работы, но и вследствие теплообмена.
При тепловом контакте тел внутренняя энергия одного из них может увеличиваться, а внутренняя энергия другого – уменьшаться. В этом случае говорят о тепловом потоке от одного тела к другому. Передача энергии от одного тела другому в форме тепла может происходить только при наличии разности температур между ними.
Приведем в соприкосновение два тела с разными температурами. Пусть температура первого тела выше, чем второго. В результате обмена энергиями температура первого тела уменьшается, а второго — увеличивается. В рассматриваемом примере кинетическая энергия хаотического движения молекул первого тела переходит в кинетическую энергию хаотического движения молекул второго тела.
Тепловой поток всегда направлен от горячего тела к холодному.
Процесс передачи внутренней энергии без совершения механической работы называется теплообменом.
Мерой энергии, получаемой или отдаваемой телом в процессе теплообмена, служит физическая величина, называемая количеством теплоты.
Количеством теплоты Q, полученной телом, называют изменение внутренней энергии тела в результате теплообмена.
Количество теплоты Q является энергетической величиной. В СИ количество теплоты измеряется в единицах механической работы – джоулях (Дж).
До введения СИ количество теплоты выражали в калориях.
Калория — это количество теплоты, необходимое для нагревания 1 г дистиллированной воды на 1°С, от 19,5°С до 20,5°С.
Единица, в 1000 раз большая калории, называется килокалорией (1 ккал = 1000 кал). Соотношение между единицами: 1 кал =4,19 Дж.
Если в результате теплообмена телу передается некоторое количество теплоты, то внутренняя энергия тела и его температура изменяются.
Чтобы нагреть тело массой m от температуры t1 до температуры t2 ему необходимо сообщить количество теплоты
Q = cm(t2 – t1)
Количество теплоты Q, необходимое для нагревания 1 кг вещества на 1 К называют удельной теплоемкостью вещества c.
c = Q / (mΔT).
Во многих случаях удобно использовать молярную теплоемкость C:
C = M · c, где M – молярная масса вещества.
При передаче тепла от одного тела к другому всегда выполняется уравнение теплового баланса, по которому количество теплоты Q1, отданное первым телом, равно количеству теплоты Q2, полученному вторым телом.
Q1 = Q2
Теплота и работа являются не видом энергии, а формой ее передачи, они существуют лишь в процессе передачи энергии.
В реальных условиях оба способа передачи энергии системе в форме работы и форме теплоты обычно сопутствуют друг другу.
Первое начало термодинамики.
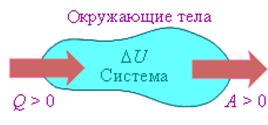
На рисунке изображены энергетические потоки между термодинамической системой и окружающими телами. в результате теплообмена и совершаемой работы:
Величина Q > 0, если тепловой поток нправлен в сторону термодинамической системы. Величина A > 0, если система совершает положительную работу над окружающими телами.
Если система обменивается теплом с окружающими телами и совершает работу (положительную или отрицательную), то изменяется состояние системы, то есть изменяются ее макроскопические параметры (температура, давление, объем).
Процессы теплообмена и совершения работы сопровождаются изменением ΔU внутренней энергии системы.
Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Он формулируется следующим образом:
Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами.
ΔU = Q – A.
Соотношение, выражающее первый закон термодинамики, часто записывают в другой форме:
Q = ΔU + A.
Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
Первый закон термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Если между телами, составляющими замкнутую систему, действуют силы трения, то часть механической энергии превращается во внутреннюю энергию тел (нагревание).
При любых физических взаимодействиях энергия не возникает и не исчезает. Она лишь превращается из одной формы в другую. Этот экспериментально установленный факт выражает фундаментальный закон природы – закон сохранения и превращения энергии.
Задачи для самостоятельного решения ( Дмитриева В.Ф. Задачи по физике)
№ 2, стр. 148
Определите p — давление насыщенного водяного пара при температуре Т=290 К, если пло ность насыщенного водяного пара при этой температуре ρ=2,56·10-2 кг/м3 (ответ р=3,43 Па)
№ 12, стр. 149
Определите m — массу стоградусного водяного пара, необходимого для нагревания m1=10 кг воды от t1=100С до t2=600С. (ответ m=0,086 кг)
№ 1, стр. 156
Поверхностное натяжение керосина α=2,4·10-2 Н/м. Какую работу А совершат силы поверхностного натяжения при уменьшении поверхностного слоя керосина на 25 см2? (ответ А=60 мкДж)
№ 7, стр. 156
В одной и той же капиллярной трубке вода поднимается на 50 мм, а спирт на 19 мм. Определите поверхностное натяжение спирта αс. Поверхностное натяжение воды αв=0,072 Н/м (ответ αс=22·10-3 Н/м)
№ 8, стр. 163
Определите Q — теплоту, необходимую для плавления свинца массой m=10 кг, находящегос при температуре плавления. Удельная теплота плавления свинца λ=25 кДж/кг. (ответ Q=250 кДж)
Внутренняя энергия. Термодинамика.
Внутренняя
энергия идеального газа, способы ее
изменения.
Термодинамика
– это наука о тепловых явлениях. В
противоположность молекулярно-кинетической
теории,
которая делает выводы на основе
представлений о молекулярном строении
вещества, термодинамика исходит из
наиболее общих закономерностей тепловых
процессов и свойств макроскопических
систем. Выводы термодинамики опираются
на совокупность опытных фактов и не
зависят от наших знаний о внутреннем
устройстве вещества, хотя в целом ряде
случаев термодинамика использует
молекулярно-кинетические модели для
иллюстрации своих выводов.
Термодинамика
рассматривает изолированные
системы тел, находящиеся в состоянии
термодинамического
равновесия.
Это означает, что в таких системах
прекратились
все наблюдаемые макроскопические
процессы.
Важным свойством термодинамически
равновесной системы является выравнивание
температуры всех ее частей.
Если термодинамическая
система была подвержена внешнему
воздействию, то в конечном итоге она
перейдет в другое равновесное состояние.
Такой переход называется термодинамическим
процессом.
Если процесс протекает достаточно
медленно (в пределе бесконечно медленно),
то система в каждый момент времени
оказывается близкой к равновесному
состоянию. Процессы, состоящие из
последовательности равновесных
состояний, называются квазистатическими.
Одним из важнейших
понятий термодинамики является внутренняя
энергия
тела. Все макроскопические тела обладают
энергией, заключенной внутри самих тел.
С точки зрения молекулярно-кинетической
теории внутренняя энергия вещества
складывается из кинетической энергии
всех атомов и молекул и потенциальной
энергии их взаимодействия друг с другом.
В частности, внутренняя энергия идеального
газа равна сумме кинетических энергий
всех частиц газа, находящихся в непрерывном
и беспорядочном тепловом движении.
Внутренняя энергия идеального газа
зависит только от его температуры и не
зависит от объема (закон Джоуля).
Молекулярно-кинетическая
теория приводит к следующему выражению
для внутренней энергии одного моля
идеального одноатомного газа (гелий,
неон и др.), молекулы которого совершают
только поступательное движение:
|
Поскольку
потенциальная энергия взаимодействия
молекул зависит от расстояния между
ними, в общем случае внутренняя энергия
U
тела зависит наряду с температурой T
также и от объема V:
|
U = U(T,V). |
Таким образом,
внутренняя
энергия U
тела однозначно определяется
макроскопическими параметрами,
характеризующими состояние тела.
Она не зависит от того, каким путем было
реализовано данное состояние. Принято
говорить, что внутренняя энергия является
функцией состояния.Внутренняя энергия
тела может изменяться, если действующие
на него внешние силы совершают работу
(положительную или отрицательную).
Например, если газ подвергается сжатию
в цилиндре под поршнем, то внешние силы
совершают над газом некоторую положительную
работу A’.
В то же время силы давления, действующие
со стороны газа на поршень, совершают
работу A = –A’.
Если объем газа изменился на малую
величину ΔV,
то газ совершает работу pSΔx = pΔV,
где p
– давление газа, S
– площадь поршня, Δx
– его перемещение (рис. ). При расширении
работа, совершаемая газом, положительна,
при сжатии – отрицательна. В общем
случае при переходе из некоторого
начального состояния (1) в конечное
состояние (2) работа
газа
выражается формулой:
|
|
или в пределе при
ΔVi → 0:
|
|
|
|
Работа газа при |
Работа численно
равна площади под графиком процесса на
диаграмме (p, V).
Величина работы зависит от того, каким
путем совершался переход из начального
состояния в конечное. На рис. изображены
три различных процесса, переводящих
газ из состояния (1) в состояние (2). Во
всех трех случаях газ совершает различную
работу.
|
|
|
Три различных |
Процессы, изображенные
на рис. можно провести и в обратном
направлении; тогда работа A
просто изменит знак на противоположный.
Процессы такого рода, которые можно
проводить в обоих направлениях, называются
обратимыми.
В отличие от газа,
жидкости и твердые тела мало изменяют
свой объем, так что во многих случаях
работой, совершаемой при расширении
или сжатии, можно пренебречь. Однако,
внутренняя энергия жидких и твердых
тел также может изменяться в результате
совершения работы. При механической
обработке деталей (например, при
сверлении) они нагреваются. Это означает,
что изменяется их внутренняя энергия.
Другим примером может служить опыт
Джоуля (1843 г.) по определению
механического
эквивалента теплоты
(рис). При вращении вертушки, погруженной
в жидкость, внешние силы совершают
положительную работу (A’ > 0);
при этом жидкость из-за наличия сил
внутреннего трения нагревается, т. е.
увеличивается ее внутренняя энергия.
В этих двух примерах процессы не могут
быть проведены в противоположном
направлении. Такие процессы называются
необратимыми.
Внутренняя энергия
газа является функцией его абсолютной
температуры.
Существуют два
способа изменения внутренней энергии
– теплопередача и работа.
Теплопередача –
без совершения работы.
-
Теплопроводность
– перенос тепла при взаимодействии
частиц. -
Конвекция
– перенос тепла потоками жидкости или
газа. -
излучение
– перенос тепла с помощью тепловых
лучей
Количество
теплоты, удельная теплоемкость вещества.
Количество теплоты
Q
– количество энергии, получаемой или
отдаваемой системой при теплообмене.
Передается от белее нагретых к менее
нагретым телам. Для изменения температуры
различных тел на одну и ту же величину
требуется разное количество теплоты Q
= cmT,
где с –
удельная теплоемкость.
Удельная теплоемкость
численно равна количеству теплоты,
которое необходимо сообщить одному
килограмму вещества для изменения его
температуры на один Кельвин.
Работа в
термодинамике.
Если газ находится
под поршнем массой m,
площадью сечения S,
то давление газа определяется атмосферным
давлением и давлением поршня.
P
= Pатм
+ mg/S
Если газ расширяется
и поршень поднимается на х,
то работа силы давления положительна
и равна А = Fgх
= PSх,
т.к. Sх
= V2
– V1
то
А = P(V2
– V1)
В случае расширения
работа газа положительна, в случае
сжатия – отрицательна.
Работа силы давления
при расширении газа
A
= PSх
Работа внешней
силы
откуда
Работа всегда
зависит от характера процесса.
Закон сохранения
и превращения энергии в тепловых
процессах.
Изменение внутренней
энергии системы при переходе ее из
одного состояния в другое равно сумме
количестве теплоты, сообщенного системе,
и работы внешних сил, совершаемый над
системой, т.е.
Работа внешних
сил равна работе системы с обратным
знаком:
откуда
Количество теплоты,
сообщаемое системе, расходуется на
изменение внутренней энергии системы
и на совершение системой механической
работы.
Адиабатный
процесс.
Адиабатный процесс
– процесс в какой-либо системе, который
происходит без обмена теплом с окружающей
средой, т.е. Q
= 0. Следовательно, U
= -A.
Адиабатное
расширение газа сопровождается понижением
его температуры, а адиабатное сжатие –
повышением температуры.
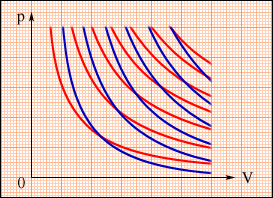
На плоскости (p, V)
процесс адиабатического расширения
(или сжатия) газа изображается кривой,
которая называется адиабатой.
При адиабатическом расширении газ
совершает положительную работу (A > 0);
поэтому его внутренняя энергия уменьшается
(ΔU < 0).
Это приводит к понижению температуры
газа. Вследствие этого давление газа
при адиабатическом расширении убывает
быстрее, чем при изотермическом расширении
(рис. ).
|
|
|
Семейства изотерм |
В термодинамике
выводится уравнение адиабатического
процесса для идеального газа. В координатах
(p, V)
это уравнение имеет вид
|
Это соотношение
называют уравнением
Пуассона.
Здесь γ = Cp / CV
– показатель адиабаты, Cp
и CV
– теплоемкости газа в процессах с
постоянным давлением и с постоянным
объемом. Для одноатомного газа
для двухатомного
для
многоатомного
Работа газа в
адиабатическом процессе просто выражается
через температуры T1
и T2
начального и конечного состояний:
|
Адиабатический
процесс также можно отнести к изопроцессам.
В термодинамике важную роль играет
физическая величина, которая называется
энтропией.
Изменение энтропии в каком-либо
квазистатическом процессе равно
приведенному
теплу ΔQ / T,
полученному системой. Поскольку на
любом участке адиабатического процесса
ΔQ = 0,
энтропия в этом процессе остается
неизменной.
Адиабатический
процесс (так же, как и другие изопроцессы)
является процессом квазистатическим.
Все промежуточные состояния газа в этом
процессе близки к состояниям
термодинамического равновесия. Любая
точка на адиабате описывает равновесное
состояние.
Применение
первого начала термодинамики к различным
процессам.
-
Изотермический
процесс. (T=const).
Т.к. температура постоянна, то внутренняя
энергия не изменяется U
= 0, то Q
= A,
т.е. все количество теплоты сообщаемое
системе, идет на совершение механической
работы. Изотермический газ нагреть
нельзя. -
Изобарный
процесс (P
= const).
Если Q
> 0, то газ и нагревается и совершает
механическую работу: Q
= U
+ A,
A = PV -
Изохорный
процесс (V
= const).
При изохорном процессе механическая
работа газом не совершается, следовательно
Q
= U
, т.е. все количество теплоты идет на
изменение внутренней энергии.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
07.02.201512.92 Mб32Копаева.pdf
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Вы
знаете, что существует два вида механической энергии — кинетическая и
потенциальная. Давайте вспомним, что кинетической энергией обладает всякое
движущееся тело: .
Потенциальная
энергия определяется взаимным положением взаимодействующих тел или отдельных
частей тела: Eп = mgh.
Изучая
механические явления, вы узнали, что кинетическая и потенциальная энергии могут
превращаться друг в друга таким образом, что их сумма остаётся постоянной величиной:
E = Ek + Eп = const.
В этом
заключается один из наиболее общих и фундаментальных законов природы — закон
сохранения и превращения энергии.
Однако,
вы знаете, что в реальных опытах закономерности превращения энергии выглядят
гораздо сложнее.
Например,
возьмём гирю из какого-либо мягкого металла, например, из свинца, и стальную
плиту. Поднимем гирю вверх на какую-либо высоту, тем самым сообщив ей некоторый
запас потенциальной энергии. А затем отпустим. Во время полёта гири её
потенциальная энергия уменьшается, а кинетическая, наоборот, увеличивается.
После падения, гиря остановится. Её потенциальная энергия относительно плиты
равна нулю, как равна нулю и кинетическая энергия, поскольку гиря неподвижна.
Означает ли это, что нарушился основной закон природы, и энергия бесследно
исчезла?
Конечно
же нет. Механическая энергия перешла в другой вид энергии. Если внимательно
посмотреть на гирю после удара, то мы обнаружим, что она, как и плита, слегка
сплющилась, то есть деформировалась. А если мы измерим её температуру до и
после падения, то окажется, что она увеличилась.
Мы уже
знаем, что при изменении температуры тела, изменяется скорость движения его
молекул. Помимо этого, в результате деформации гири, изменилось и взаимное
расположение молекул друг относительно друга. Значит изменилась и их
потенциальная энергия.
Следовательно,
механическая энергия, которой обладала гиря в начале опыта, не исчезла: она перешла
в потенциальную и кинетическую энергию её молекул.
Сумма
кинетической энергии теплового движения частиц, из которых состоит тело, и
потенциальной энергии их взаимодействия, называется внутренней энергией тела.
Обозначают
внутреннюю энергию буквой U. А измеряют её в тех
же единицах, что и механическую энергию: [U] = [Дж].
Возникает
логичный вопрос: а каково значение внутренней энергии какого-либо тела?
Для
примера рассмотрим какой-нибудь газ, например, кислород. Потенциальная энергия
взаимодействия его молекул между собой практически отсутствует. А кинетическая
энергия одной молекулы кислорода очень мала. Расчёты показывают, что среднее
значение кинетической энергии молекулы кислорода при комнатной температуре
равно 3,7 ∙ 10−21 Дж.
Кто-то
скажет, что это очень маленькая величина, и будет прав. Но, например, в 1 м3
газообразного кислорода содержится примерно 2,7 ∙ 1025. А их
общая энергия равна почти 100 кДж. А это значение энергии уже весьма
значительно. Такой энергией, например, будет обладать одна тонный бизон, если
его поднять на высоту десяти метров.
Теперь
выясним, от чего зависит внутренняя энергия тела?
Вы уже
знаете, что чем больше температура тела, тем быстрее движутся молекулы. Чем
больше скорость движения, тем больше их кинетическая энергия. Значит,
внутренняя энергия тела зависит от его температуры.
Также вам
должно быть известно, что для перевода вещества из жидкого состояния в
газообразное, например, чтобы превратить воду в пар, нужно подвести энергию.
Следовательно, пар будет обладать большей внутренней энергией, чем вода той же
массы. Значит, внутренняя энергия тела при неизменной массе зависит от его
агрегатного состояния.
Т. к.
масса тела равна сумме масс составляющих его частиц, то внутренняя энергия
зависит и от массы тела.
Но
внутренняя энергия тела не зависит от его механического движения и от его
взаимодействия с другими телами. Так, например, внутренняя энергия мяча,
лежащего на полу и поднятого на некоторую высоту от пола, одинакова, так же,
как и мяча, неподвижного и катящегося по полу (если, конечно, пренебречь силами
сопротивления его движению).
Возникает
вопрос, а может ли у тела отсутствовать внутренняя энергия?
Чтобы
правильно на него ответить, достаточно вспомнить, что движение частиц, из
которых состоит тело, никогда не прекращается, даже при очень низких
температурах. Поэтому тело всегда обладает внутренней энергией.
Как
правило, значение внутренней энергии в большинстве случаев вычислить очень
трудно, поскольку каждое тело состоит из огромного числа частиц. Однако нас
чаще будет интересовать не само значение внутренней энергии, а её изменение. А
о нём можно судить, в частности, по значению совершённой работы.
Вот мы
и подошли ко второй важной проблеме — можно ли как-то изменить внутреннюю
энергию тела?
Рассуждаем
последовательно. Внутренняя энергия определяется энергией движения и энергией
взаимодействия частиц. Следовательно, если мы сможем изменить скорость движения
частиц, либо усилить или ослабить их взаимодействие друг с другом, то мы сможем
изменить и внутреннюю энергию тела.
Рассмотрим
каждую из возможностей изменения внутренней энергии отдельно.
Мы уже
знаем, что изменить кинетическую энергию частиц тела можно путём увеличения или
уменьшения температуры тела.
Существует
два способа это сделать. Рассмотрим их на конкретных примерах. И так, возьмём
закрытый сосуд с воздухом, к которому присоединим манометр. И начнём натирать
сосуд с помощью тряпочки или сукна.
Уровень
жидкости в левом колене манометра начинает понижаться. Это обусловлено тем, что
воздух в колбе начинает нагреваться, вследствие чего, увеличивается его
давление. Значит увеличивается и кинетическая энергия молекул воздуха. Таким
образом, совершив механическую работу (трение сукна о колбу) мы смогли
увеличить кинетическую энергию молекул находящегося в колбе воздуха.
Проделаем
ещё один опыт. Возьмём толстостенный стеклянный сосуд, на дне которого
находится небольшое количество воды. Закроем его пробкой с пропущенной через
неё трубкой. Соединим трубку с насосом и начнём накачивать в сосуд воздух.
Через некоторое время пробка из сосуда вылетит и в нём образуется туман.
Туман
— это превратившийся в воду водяной пар.
Подумайте,
когда образуется туман? Наверняка каждый из вас замечал, что чаще всего туман
образуется тогда, когда после тёплого дня, наступает прохладная ночь, т. е. при
значительном понижении температуры.
Следовательно,
температура воздуха в сосуде понизилась. А понизилась она из-за того, что
воздух, находящийся в сосуде, совершил работу. Вследствие чего, внутренняя
энергия молекул воздуха в сосуде уменьшилась.
Таким
образом, мы с вами можем сделать важный вывод о том, что внутренняя энергия
тела изменяется при совершении работы. При этом если тело совершает работу,
то его внутренняя энергия уменьшается. А если над телом совершают
работу, то его внутренняя энергия увеличивается.
Теперь
подумаем, можно ли изменить внутреннюю энергию тела, без совершения
механической работы?
Вернёмся
к опыту с колбой и манометром. Теперь не будем натирать колбу, а нагреем в ней
воздух при помощи спиртовки. И опять через небольшой промежуток времени уровень
жидкости в левом колене манометра начнёт понижаться. Что свидетельствует о том,
что опять происходит изменение внутренней энергии воздуха в колбе.
Теперь
обратимся к ситуации, с которой вы сталкиваетесь в жизни постоянно. Возьмём
стакан с горячим чаем и металлическую ложку. Вы хорошо знаете, что если ложку
опустить в стакан с чаем, то она через некоторое время тоже становится горячей.
В этом
случае, как и в предыдущем, работа не совершается, но внутренняя энергия ложки
увеличивается, о чём и свидетельствует повышение её температуры.
Поскольку
вначале температура воды выше, чем температура ложки, то и средняя скорость
молекул воды больше. А это значит, что молекулы воды обладают большей
кинетической энергией, чем частицы металла, из которого сделана ложка. При
столкновении с частицами металла молекулы воды передают им часть своей энергии,
и кинетическая энергия частиц металла увеличивается. А кинетическая энергия
молекул воды при этом уменьшается.
В
рассмотренных нами примерах внутренняя энергия тел изменялась путём теплопередачи.
Теплопередача
— способ изменения внутренней энергии тела, при котором энергия передаётся от
одной части тела к другой или от одного тела к другому без совершения работы.
Стоит
обратить внимание на то, что процесс теплопередачи происходит в определённом
направлении — от более нагретых тел к менее нагретым, но не наоборот. А
когда температуры тел выравниваются, теплопередача прекращается.
Таким
образом, возможны два способа изменения внутренней энергии —совершение
механической работы и теплопередача.
Существует
три вида теплопередачи — теплопроводность, конвекция и излучение. Но о
них мы с вами поговорим на следующих занятиях.

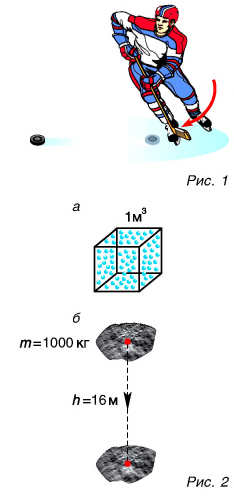
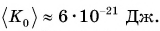
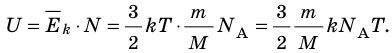 Итак, для одноатомного идеального газа:
Итак, для одноатомного идеального газа: 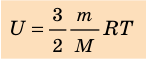 . Используя уравнение состояния
. Используя уравнение состояния 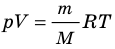 , выражение для внутренней энергии идеального одноатомного газа можно представить так:
, выражение для внутренней энергии идеального одноатомного газа можно представить так: