В конце XX века тогда еще начинающие британские биохакеры совершили настоящий прорыв в генетике и предоставили любому человеку возможность с помощью ДНК-теста узнать больше о своих далеких предках и загадочной наследственности. Тогда, правда, только избранные могли объяснить, зачем и кому это нужно, — генетика была интересна лишь узкой группе специалистов, работающих с редкими заболеваниями. Но теперь за простым любопытством стоит более глобальная задача — разобраться в своей наследственности. А причина этому — надвигающийся тренд на тотальное оздоровление, исцеление и персонализированную медицину.
Сегодня эксперты уже не сомневаются в том, что генетика — основополагающая наука медицины будущего, хотя ее технологии и без того кажутся чем-то из мира научной фантастики. Перспективы развития генетики в России обсудят на площадках форума «БИОТЕХМЕД», который пройдет 16 и 17 сентября в Геленджике. В преддверии этого события «РБК Стиль» пообщался с одним из экспертов форума — врачом-генетиком Екатериной Захаровой — и узнал у нее, как работает ДНК, какие особенности мы можем унаследовать от родителей и безопасно ли вмешательство генетиков в организм.
Екатерина Захарова
Заведующая лабораторией наследственных болезней обмена веществ ФГБНУ «Медико-генетический научный центр им. академика Н.П. Бочкова», член экспертного совета по редким болезням при комитете Государственной думы по охране здоровья
Как устроена клетка
Со школьных времен всем известно, что организм человека состоит из множества клеток, в каждой из которых есть ядро — именно там хранится генетическая информация. Ее мы наследуем от родителей и дальше передаем своим детям. В материальном обличии эта информация представлена в виде той самой нити ДНК — дезоксирибонуклеиновой кислоты. Эта макромолекула была открыта достаточно давно, но то, что именно в ней хранится генетическая информация, стало известно только в XX веке.
Дезоксирибонуклеиновая кислота (ДНК) — макромолекула, которая хранит и передает из поколения в поколение генетическую программу функционирования живых организмов. Биологическая информация в ДНК представлена в виде уникального генетического кода, состоящего из последовательности нуклеотидов.

© DrAfter123/gettyimages.com
Зачем нужна ДНК
Говоря о том, зачем нам ДНК и что она делает, можно привести аналогию: каждый белок в нашем организме синтезируется по определенному «рецепту». В нем указано, сколько должно быть аминокислот, в какой последовательности они будут соединяться и куда дальше последуют. В таком случае ДНК — это поваренная книга, в которой записаны рецепты всех наших белков, а мутация — это повреждение белка или изменение текста поваренной книги. Если в рецепте появляется опечатка, то белок получается «неправильный» и не выполняет свои функции должным образом, отчего страдает как клетка, так и весь организм, что приводит к развитию заболевания.
Во всех наших клетках хранятся одинаковые гены. Но функции у клеток разные: одни, например, синтезируют гемоглобин, другие занимаются мышечными белками, третьи — нервными. Это обеспечивается с помощью системы регуляции активности генов: она способна «включать» одни гены и оставлять в молчании другие.
Чем генетика отличается от наследственности
Генетика — большая и очень разнообразная наука. Клиническая генетика изучает, как проявляются наследственные болезни, популяционная — наше происхождение и особенности каждого народа. А вот наследственность — понятие уже более узкое. Люди давно заметили, что есть признаки, которые ярко проявляются у представителей одной семьи и передаются из поколения в поколение.
Если вспомнить живопись и портреты членов династии испанских Габсбургов, то многим сразу придут на ум их наследственные приметы: выступающая «габсбургская губа» и гипертрофированная нижняя челюсть, которая, говорят, даже мешала монарху нормально пережевывать пищу. Совершенно очевидно, что эти признаки связаны с изменениями определенных генов в известном роду.
Что еще хранится в ДНК
Информация, закодированная в ДНК, способна рассказать как о заболеваниях, так и о цвете волос, форме глаз, группе крови и даже вкусовых предпочтениях. Например, в ходе генетических исследований ученые обнаружили, что всех людей можно разделить на две категории: тех, кто любит капусту брокколи, и тех, кто ее просто ненавидит. Оказалось, что у второй группы есть определенные повреждения в гене, ответственные за восприятие этого вкуса, — им брокколи кажется горькой и неприятной.
В ДНК также могут быть записаны наши пагубные привычки, склонность к полноте или употреблению алкоголя. Изменения в некоторых генах делают нас более восприимчивыми к этим факторам. Но, как правило, за них отвечает не один, а сразу множество взаимосвязанных генов. Кроме того, врачи уверены, что более существенную роль в данном вопросе играют воспитание и другие социальные факторы.

© DrAfter123/gettyimages.com
Можно ли унаследовать интеллектуальные способности
Считается, что интеллектуальные и эмоциональные способности будущего ребенка определяются большим набором генов, и предсказать, какую именно комбинацию они составят, наука пока не в состоянии. Поэтому утверждать, что у гениальных родителей рождаются только гениальные дети, нельзя. Хотя такой миф до сих пор существует: некоторые женщины даже продолжают выбирать себе избранника, исходя из его интеллектуальных способностей, или искать какого-нибудь выдающегося донора — нобелевского лауреата.
Однако есть теория, согласно которой IQ будущего ребенка в большей степени определяется матерью, поскольку в тех областях мозга, которые отвечают за интеллект, чаще активируется ген, наследуемый от нее. А вот за эмоциональное состояние и характер чаще отвечает отец. И в этом случае нобелевский лауреат может оказаться не самым лучшим кандидатом на отцовство.
Как наследуются болезни
Болезни могут наследоваться по-разному. В некоторых случаях патология должна быть у одного из родителей, который, в свою очередь, передает ее детям (с вероятностью 50%). В других болезнь наследуется только по женской линии, и в итоге страдают ей мальчики, а девочки остаются ее здоровыми носительницами. Есть и заболевания, которые переносят оба родителя — у них больной ребенок может появиться на свет только в 25% случаев.
Кроме того, существует множество патологий, которые не наследуются, а появляются случайным образом. Например, в одной половой клетке матери или отца происходят изменения без особых на то причин, и в семье, где никогда не встречались с генетическими заболеваниями, может родиться малыш с синдромом Дауна (хромосомной патологией) или ахондроплазией — моногенным заболеванием, которое проявляется как карликовость. В такой ситуации одна из главных задач врача-генетика — выяснить, как наследуется болезнь, проинформировать семью о возможных рисках рождения больного ребенка, а также рассказать, что можно сделать, чтобы ребенок родился здоровым.
© DrAfter123/gettyimages.com
Наследуются ли онкологические заболевания
Большинство онкологических заболеваний — это мутации в генах. Однако они возникают не в половых, а в соматических клетках и не передаются по наследству. В таком случае на их развитие большое влияние оказывают именно внешние факторы: курение, радиация и канцерогенные химические вещества.
Но, к сожалению, есть отдельные виды онкозаболеваний, к которым приводит мутация в генах: они переходят от родителей к ребенку. Самый известный пример — рак молочной железы, за появление которого отвечают гены BRCA1 и BRCA2. В группу риска попадает подавляющее большинство девушек и женщин, у которых в семье были случаи рака молочной железы, поскольку наличие мутации в генах сильно повышает риск развития этого заболевания в определенном возрасте. Это означает, что рак может появиться вне зависимости от образа жизни, занятий спортом и сбалансированности рациона.
Как разгадать свои гены
Попытаться разобрать загадочную ДНК и узнать больше о своих генах можно при помощи генетических тестов. Как правило, их рекомендуют проводить в первую очередь тем семьям, где уже были зафиксированы случаи наследственных заболеваний. Но есть скрининг-тесты, которые проводятся для всех, вне зависимости от того, есть ли вероятность возникновения наследственного заболевания. Например, сейчас у всех беременных женщин есть возможность сдать анализы на определение генетических заболеваний у эмбриона. Скрининг на раннем сроке проводится специально для того, чтобы определить, входят ли будущая мама и ее малыш в группу риска. Дальше назначаются дополнительные обследования, которые подтверждают или опровергают развитие патологии. В ходе беременности не менее важно своевременно делать УЗИ, потому что пороки развития у плода встречаются намного чаще, чем любые наследственные заболевания.
Будущие родители должны осознавать, что комбинации их генов не всегда могут привести к идеальному результату. Но с некоторыми из наследственных патологий ребенок может жить совершенно нормально, поэтому пугаться их не стоит.
Может ли врач исправить наследственность
Если представить, что врач на начальном этапе сможет скомбинировать гены так, чтобы исправить недочеты в хромосомах будущего ребенка, родители, наверное, согласятся. Хотя стоит взять в расчет то, что часто двигателями прогресса, науки и искусства становятся именно неординарные люди. У талантливых художников, поэтов или музыкантов неоднократно были зафиксированы особенности развития, и если бы отбор по таким критериям существовал сотни лет назад, то мир лишился бы практически всех гениев.
Сейчас мы знаем многое о геноме человека и уже научились читать его последовательность. Но вот понять смысл этого «текста» можем далеко не всегда. Так же, как не всегда знаем, повлияет ли положительно наше вмешательство в структуру одного гена на работу других. Больше того, функция многих участков ДНК до сих пор остается не изучена.

© DrAfter123/gettyimages.com
ЭКО и дети из пробирки
Когда начинаешь работать с чем-то малоизвестным (а это часто встречается в генетике), всегда возникает вопрос о том, что делать правильно и этично, а что нет. Сегодня в цивилизованных странах накладывается запрет на генетические манипуляции с половыми клетками, потому что мы не знаем, как их изменения могут передаваться дальше и к каким последствиям это приведет. И, конечно, нельзя проводить эксперименты на живых эмбрионах.
Пока что в случае обнаружения какого-либо генетического заболевания врач может только предложить пренатальную или предимплантационную диагностику — метод, позволяющий произвести генетическую экспертизу одной клетки эмбриона перед процедурой ЭКО (экстракорпорального оплодотворения). Задача такой диагностики — предоставить возможность рождения здоровых детей в семьях, где существует высокий риск рождения ребенка с тяжелыми заболеваниями. Но у любых современных технологий, включая ЭКО, есть свои риски. Даже после подсадки эмбрион может не прижиться. При этом среди нас уже растет множество детей, которые появились благодаря искусственному оплодотворению, и они совершенно ничем не отличаются от обычных малышей.
Что происходит с эволюцией
В глобальном плане человеческие гены могут со временем мутировать и видоизменяться. И онкологические заболевания — одна из самых ярких иллюстраций этого процесса. Теперь, когда продолжительность жизни выросла, увеличилась и вероятность появления опухолей. С другой стороны, прогресс тоже не стоит на месте: появляется все больше методов диагностики и лечения, которые помогают справляться с тяжелыми недугами.
Еще до недавнего времени выявление генетических заболеваний было непростой задачей. Однако методы секвенирования уже позволяют «читать» ДНК не по одной букве-нуклеотиду, а разбирать все буквы одновременно. Так можно выявлять и мутации, передающиеся по наследству и новые, от появления которых не застрахован никто. Конечно, некоторые окружающие факторы тоже могут влиять на то, как ведут себя наши гены. Это и экология, и пища, и привычки. Их изучением наука тоже занимается активно.
Куда движется генетика
Генетика становится всеобъемлющей: по одной капле крови теперь можно определить все, что веками записывалось в ДНК человека. Вместо сотрудников диагностикой занимаются математические алгоритмы. Вполне возможно, что через некоторое время генетическая экспертиза станет обычным делом и без нее не будет обходиться даже рядовой прием у врача-терапевта.
И наверняка будет создаваться все больше препаратов, основанных на принципах персонализированной медицины, которые подбираются в зависимости от особенностей метаболизма пациента и его мутаций. Что же касается детей на заказ, то наука должна помогать нам корректировать гены только в случаях тяжелых наследственных заболеваний, а не для того, чтобы выбирать пол ребенка и цвет его глаз или особенности поведения. В этом вопросе нужно позволить природе комбинировать наши гены для появления на свет совершенно неповторимого чудесного существа — человека.
: 7 Окт 2017 , Россия Делает Сама , том 75,
№4
Что на роду написано, того не миновать?
Редактирование генома в терапии наследственных заболеваний
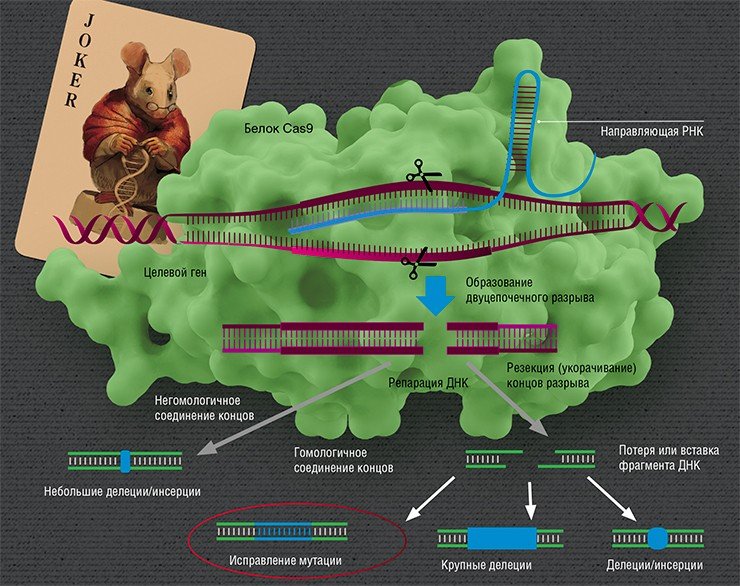
Наследственность – это своего рода фатализм нашего времени. Расшифровка последовательности ДНК сродни предсказанию судьбы человека. Нам говорят, что гены определяют все: от цвета глаз до склонности к девиантному поведению. Добавьте к этому болезни, передающиеся по наследству, и мутации, связанные с риском развития таких болезней, как рак. Но можно ли пойти наперекор зловещему року и изменить судьбу, записанную на «скрижалях» ДНК? Да, это возможно, и если не сегодня, то в недалеком будущем. Генетическая инженерия занимается этими проблемами уже несколько десятков лет, однако в последние годы вокруг редактирования геномов возник особый ажиотаж. Что же изменилось? Ответ на этот вопрос – аббревиатура CRISPR/Cas
Все началось в 1987 г., когда в бактериальной ДНК были обнаружены странные нуклеотидные повторы, разделенные небольшими участками уникальных последовательностей. Спустя десять лет было показано, что эти повторенные последовательности, названные CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats), являются системой адаптивного иммунитета бактерий – способом защиты против чужеродной ДНК, в частности, против бактериальных вирусов (бактериофагов).
Но какое отношение имеет это к наследственным болезням человека? Все дело в механизме действия системы CRISPR. Бактериофаги впрыскивают в клетку бактерии свою ДНК, которая многократно копируется и упаковывается в белковую оболочку за счет «хозяина» – таким образом на свет появляются новые бактериофаги. Защитная система бактерии, включающая белок-«ножницы» Cas, распознает чужую ДНК в случае, если она уже встречалась с ней раньше, и разрезает ее. Захватчики побеждены.
Узнавание мишени происходит по знаменитому принципу комплементарности, по которому образуются пары нуклеотидов в двуспиральной структуре ДНК. Этот принцип работает во всех живых организмах на нашей планете, включая клетки человека. Поэтому главное в механизме CRISPR/Cas – его простота и универсальность.
Знаковое событие случилось в 2012 г., когда была опубликована совместная работа француженки Э. Шарпентье и американки Д. Дудна, где было показано, что бактериальная система CRISPR/Cas может быть использована для внесения разрывов в последовательность любой ДНК, что свидетельствовало об ее огромном потенциале для редактирования геномов (Jinek et al., 2012). Ведь, зная нуклеотидную последовательность, можно внести разрыв в точно выбранное место любой ДНК.
Так в руках ученых оказался простой и эффективный инструмент, позволяющий направленно вносить изменения в ДНК живой клетки, т. е. переписывать те самые «скрижали». С тех пор вышли сотни научных статей, свидетельствующих о том, что эта система работает в самых различных видах организмов, позволяет вносить разрывы в любые последовательности генов, в том числе несущие мутации, вызывающие наследственные болезни (Немудрый, 2014).
Ремонтируем ДНК направленно
Но вот ДНК разрезана – что дальше? Дальше идет «ремонт» (репарация). Вообще разрывы в ДНК не такая уж и редкость: ежесуточно в каждой клетке человека под действием активных форм кислорода их возникает около 10 тысяч, и клетка их тщательно «штопает», восстанавливая целостность ДНК (Helbock et al., 1998). Но эти разрывы случайны, в отличие от действия CRISPR/Cas.
Существуют «терапевтические» мутации, предотвращающие развитие заболеваний. Например, мутации в гене CCR 5 предотвращают заражение клеток ВИЧ (Genovese et al., 2014, Liu et al., 1996), а мутация A673T в гене APP – развитие болезни Альцгеймера (Jonsson et al., 2012). С помощью системы CRISPR/Cas можно внести в геном необходимые изменения, «сломав» целевые гены либо внеся целевые замены (Cox et al., 2015)
Направленные разрывы, внесенные CRISPR/Cas, могут быть репарированы по-разному: существует несколько способов, отличающихся механизмом, точностью и т. п. В зависимости от пути репарации можно получить следующие результаты. Во-первых, «сломать» ген, если при репарации ДНК произойдет мутация. Такого эффекта можно добиться, если репарация произойдет, например, по механизму соединения негомологичных концов, для которого характерна неточность. Также возможно добиться крупной делеции (утраты фрагмента ДНК) и удалить участок либо целый ген.
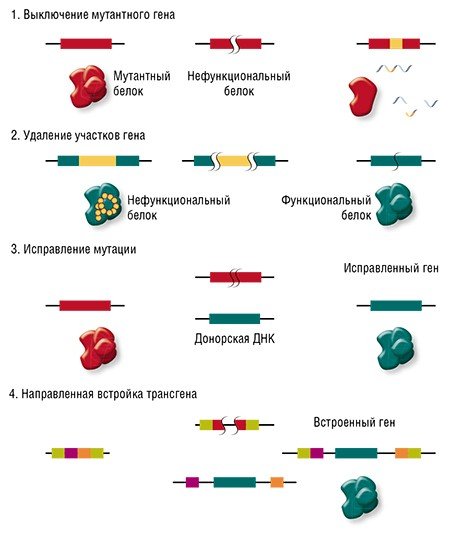
Сестринская хромосома присутствует в клетке в единичном экземпляре, а копий «донорной» ДНК можно доставить множество, что дает искусственной ДНК конкурентное преимущество, пусть она и отличается немного от поврежденного участка. Таким образом можно «исправить», к примеру, мутацию, или вставить небольшой новый фрагмент ДНК.
И вот здесь мы вплотную подходим к терапии генетических заболеваний. Начнем с того, что все такие патологии отличаются друг от друга: они вызваны мутациями в разных генах, да и сами мутации могут иметь различную природу и давать разный эффект в одном и том же гене. Соответственно, есть разные варианты применения геномного редактирования: ген можно «сломать» или просто удалить мутантный участок, «исправить» мутацию или, напротив, добавить в геном полезные «терапевтические» мутации или даже новый дополнительный трансген.
В теории все это выглядит прекрасно, но вот в чем вопрос: в организме взрослого человека имеются десятки триллионов клеток, и в каждой из них содержится мутантный ген. Как эти подходы применить на практике? Как лечить реального пациента?
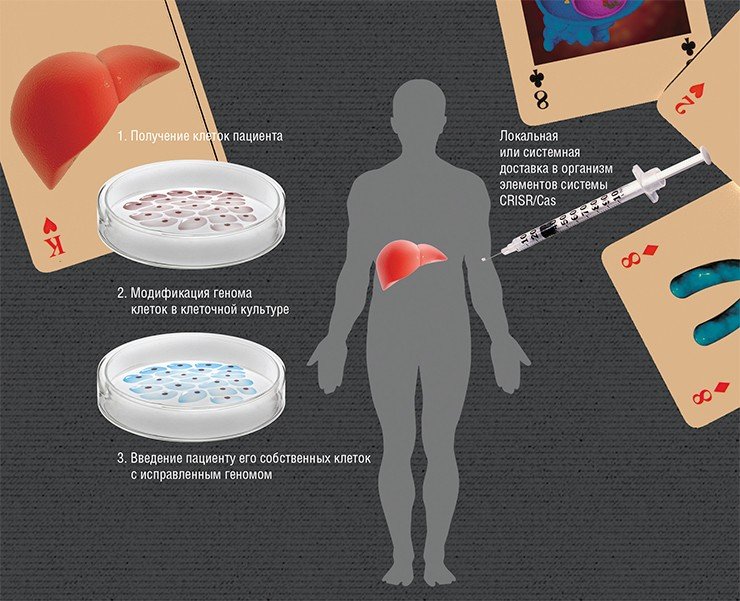
Работаем «в пробирке» и в организме
На самом деле в большинстве случаев нет нужды исправлять мутацию в каждой клетке организма. Например, серповидноклеточная анемия вызвана мутациями в гене, кодирующем субъединицу гемоглобина, что приводит к дисфункции только клеток крови – эритроцитов. А наследственные нейродегенеративные заболевания, например боковой амиотрофический склероз, связаны с гибелью нейронов определенных типов. Таким образом, мишенями для терапии многих генетических заболеваний могут быть клетки лишь определенных органов или тканей, где специфично синтезируются/не синтезируются продукты мутантных генов.
Суть редактирования геномов ex vivo («вне живого») заключается во введении в организм «здоровых» клеток, в которых, к примеру, будет синтезироваться нужный белок. Но если вводить клетки, взятые даже от здорового донора, то организм пациента с большой вероятностью их отторгнет. Поэтому нужно взять клетки самого пациента и изменить в них мутантный ген, а потом ввести их обратно. Наиболее разработан этот подход для заболеваний крови, поскольку забор и пересадка костного мозга, где идет кроветворение, практикуется с 1959 г.
Но что делать в случае, если «дефектные» клетки не так просто получить? Например, если болезнь проявляется в головном мозге? Вдобавок не все типы клеток способны пережить все процедуры в чашке Петри вне организма. Здесь на помощь приходит другая крайне перспективная технология нашего времени, связанная с получением так называемых индуцированных плюрипотентных стволовых клеток (ИПСК).
Плюрипотентные стволовые клетки бессмертны: теоретически они могут делиться бесконечно и при действии определенных стимулов образовывать любые клетки тканей и органов взрослого организма. Используя необходимый набор стимулов, можно направить развитие стволовых клеток в определенный тип клеток, например, в нейроны. Этот процесс называют направленной дифференцировкой
Относительно простой и эффективный способ получения стволовых клеток из клеток кожи в результате репрограммирования был изобретен в 2006 г. японскими исследователями К. Такахаси и С. Яманака (Takahashi & Yamanaka, 2006). Таким образом, появился метод вернуть практически любую клетку организма (крови, кожи, жировой ткани и т. д.) в состояние стволовой.
Возможность использования ИПСК для клеточной терапии наследственных заболеваний была впервые продемонстрирована на модели серповидноклеточной анемии (Hanna et al., 2007). В геном лабораторных мышей были встроены мутантные гены человека, приводящие к развитию этой болезни.
Из клеток кожи этих животных были получены индуцированные плюрипотентные стволовые клетки, в которых мутация была исправлена с помощью гомологичной рекомбинации. Путем направленной дифференцировки из этих клеток были получены стволовые предшественницы клеток крови, которые трансплантировали в организм животных. Последние не только прижились, но и превратились в здоровые эритроциты. Лечение оказалось успешным.
С тех пор cписок наследственных болезней, для которых успешно был опробован этот подход, пополнился десятками наименований и продолжает расти.
Но зачем тратить время и деньги на извлечение и культивирование клеток, если можно все сделать прямо «на месте»? Ведь система CRISR/Cas в силу своей универсальности теоретически способна работать непосредственно в клетках живого организма. Главная проблема – это эффективно и безопасно доставить элементы этой системы в нужное место.
Сегодня наиболее часто для доставки генов CRISPR/Cas в организм используются вирусные частицы. В качестве таких носителей обычно выступают аденоассоциированные вирусы – дефектные вирусы, способные размножаться только в присутствии «помощников»-аденовирусов. Эти вирусы эффективно заражают клетки человека, но не вызывают у него никаких патологий. А вирусные частицы, в геном которых встроены гены CRISPR/Сas, после заражения уже не могут размножаться. При этом разные серотипы этих вирусов имеют «склонность» к разным тканям. Например, серотип AAV8 предпочитает ткани печени, а уже сегодня можно создать искусственные серотипы, нацеленные на любой орган.
Активно развиваются и невирусные способы доставки, например, упаковка готовых молекулярных комплексов РНК-белок в липосомы (липидные пузырьки) или полимерные частицы. Это более безопасно, а также обеспечивает более строгий контроль над дозой.
Это все здорово, но…
Всегда есть это «но». Технология CRISPR/Cas начала применяться для редактирования геномов млекопитающих пять лет назад. На сегодня получено колоссальное количество данных, достигнут огромный прогресс на пути к клиническому применению, но все же остается ряд вопросов, которые необходимо будет решить для каждого конкретного генетического заболевания. Например, какая доставка будет оптимальна? Приживутся ли введенные клетки? Какова будет эффективность и безопасность лечения? И etc. …
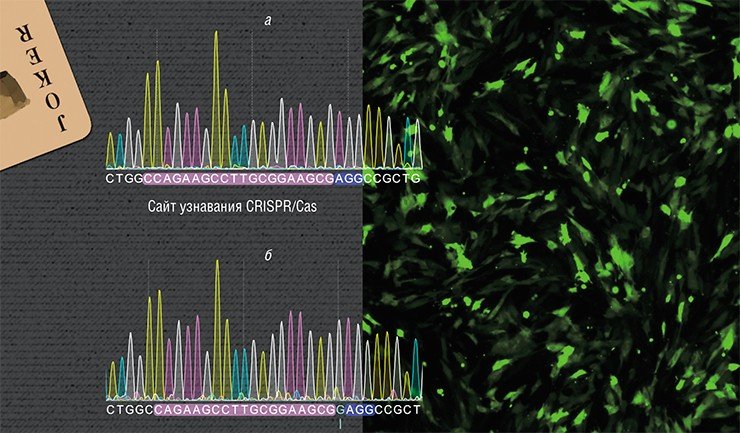
Возьмем для примера пару вопросов из этого списка и посмотрим, какие конкретные ответы на них уже получены в научном сообществе. Одна из проблем использования CRISPR/Cas связана с возможностью нецелевых эффектов: система может вносить разрывы в участки, отличающиеся от целевого на несколько «букв» – нуклеотидов, что чревато риском возникновения нежданных мутаций. Особенно остро вопрос безопасности стоит при редактировании геномов in vivo, когда проверить результат предварительно невозможно.
Для решения этой проблемы лидирующие группы ученых под руководством Д. Дудны, Ф. Чжана и К. Джуна независимо друг от друга создали мутантные «улучшенные» варианты белка Cas9 с повышенной специфичностью, частота нецелевых эффектов которых упала на несколько порядков.
С помощью технологии геномного редактирования можно не только лечить наследственные заболевания, но и создавать «дизайнерских» детей. Ведь если можно исправить ген, вызывающий болезнь, то почему бы не изменить ген, регулирующий цвет глаз, продолжительность жизни, наконец, интеллект? Уже сегодня в Китае с помощью CRISPR/Cas выведены собаки породы бигль, у которых «выключен» ген, кодирующий миостатин – фактор, подавляющий рост мышечной ткани. В результате эти животные отличаются повышенной мускулистостью. А что мешает «выключить» этот ген в эмбрионе человека?
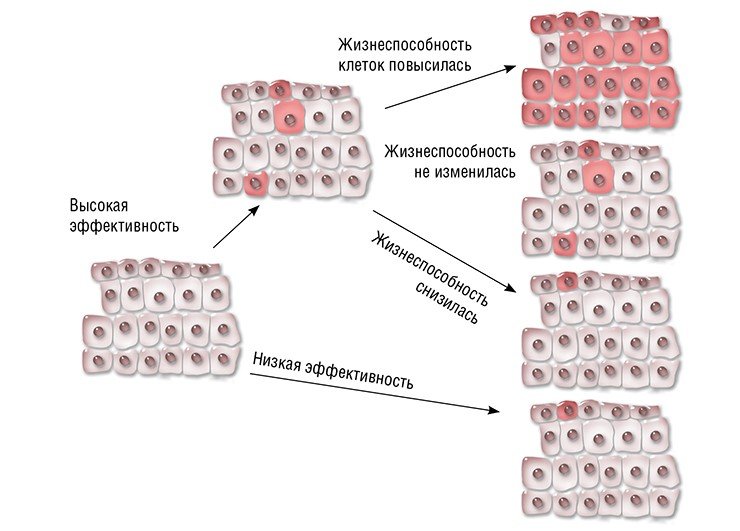
Что касается эффективности терапии, то все зависит от особенностей самого заболевания и мутации, его вызывающей. Возможны три варианта: после исправления мутации жизнеспособность клеток увеличится, не изменится или ухудшится. В первом случае исправленные клетки получают конкурентное преимущество и могут постепенно заместить мутантные. Например, на линии мышей с наследственным заболеванием печени – тирозинемией I типа – было показано, что при системной доставке CRISPR/Cas непосредственно в организм животного мутация «исправляется» в 6 % клеток печени. Даже такого небольшого количества клеток достаточно, чтобы предотвратить падение веса и привести в норму биохимические показатели печени животных. А более жизнеспособные клетки с исправленной мутацией начинают «обживать» печень.
Но, к примеру, в случае гемофилии B жизнеспособность клеток после исправления мутации не повышается. Тем не менее уже 3—7 % клеток печени, продуцирующих нормальный фактор свертывания крови, достаточно для устойчивого терапевтического эффекта (Ohmori et al., 2017).
Что же касается исправления мутаций в онкогенах, то жизнеспособность и скорость пролиферации таких клеток будет снижаться относительно раковых, поэтому эффективность подобной терапии вызывает сомнения.
Тем не менее пример гемофилии B показывает, что если заболевание связано с отсутствием какого-то фермента или гормона, то небольшого числа клеток, его продуцирующих, может хватить, по крайней мере, для перевода болезни в более мягкую форму, а в некоторых случаях и для полного восстановления утраченных функций.
Классическими же модельными заболеваниями в исследованиях по терапии с помощью геномного редактирования являются гемоглобинопатии и мышечная дистрофия Дюшенна. Именно на этих заболеваниях была подтверждена работоспособность концепций такого лечения, показано, что клетки с исправленной мутацией демонстрируют «здоровый» фенотип. В случае мышечной дистрофии Дюшенна такие клетки не только успешно встраивались в мышечную ткань взрослых мышей, но и улучшали функциональные показатели всей мышцы в целом.
Система CRISPR/Cas9 открывает перед человечеством большие перспективы, но нужно понимать, что это не волшебная палочка для решения всех проблем, а инструмент, такой, как, например, молоток. И нужно учиться применять этот инструмент для каждой конкретной задачи.
Главный шаг, который уже был сделан в этой области, – это выход за пределы лабораторий. Уже существует ряд компаний, занимающихся внедрением технологии CRISPR/Cas в практику, и не только медицинскую. Этот подход, к примеру, используется сегодня для получения модифицированных микробов для нужд биотехнологии и модифицированных растений.
Можно ожидать, что уже в ближайшее десятилетие новая технология найдет и клиническое применение. Так, в 2016 г. в Китае стартовали первые клинические испытания нового метода иммунотерапии метастазирующего немелкоклеточного рака легкого, в котором используются T-лимфоциты с «отредактированным» геномом.
С. М. ЗАКИЯН: «НАМ БЫЛ БРОШЕН ВЫЗОВ, И МЫ ДОЛЖНЫ НА НЕГО ОТВЕТИТЬ!» Исследования по применению системы CRISPR/Cas для терапии наследственных заболеваний начались в лаборатории эпигенетики развития ИЦиГ СО РАН под руководством С. М. Закияна в 2013 г., буквально сразу после выхода первых публикаций на эту тему.
Исследования ведутся на лабораторных крысах линии Brattleboro – модели генетически детерминированного заболевания, при котором наблюдается дефицит гормона аргинин-вазопрессина. В результате у животных развивается наследственный несахарный диабет с характерным для него чрезмерным потреблением жидкости. На сегодня уже получена линия клеток с исправленной мутацией в гене, кодирующем этот гормон.
В данном случае задача усложнялась тем, что ген вазопрессина по последовательности нуклеотидов схож с геном другого гормона – окситоцина. Более того, на участке, в котором возникла мутация у крыс Brattleboro, эти гены практически идентичны. Тем не менее удалось добиться специфичного действия CRISPR/Cas в гене вазопрессина без нецелевых двунитевых разрывов ДНК в гене окситоцина. На следующем этапе предполагается вводить исправленные клетки в организм животных для оценки терапевтического эффекта
Возможности, которые дает нам технология CRISPR/Cas, пугающие и захватывающие одновременно. Сначала китайские исследователи, а затем их коллеги из США смогли внести изменения в эмбрионы человека. Недавно группа американских ученых под руководством Ш. Миталипова «исправила» в человеческом эмбрионе мутацию, вызывающую гипертрофическую кардиомиопатию (Ma et al., 2017). Эти эмбрионы были получены специально в результате искусственного оплодотворения, для которого были использованы здоровая яйцеклетка и сперматозоиды носителя мутации. Согласно современным нормам, зародыши были выведены из эксперимента на стадии бластоцисты. Однако с помощью современных репродуктивных технологий уже сегодня можно было бы имплантировать такие эмбрионы суррогатным матерям.
И здесь возникает очень серьезный этический вопрос: имеем ли мы право вмешиваться в ДНК человека? Или, наоборот, этично ли бездействовать, обрекая будущего ребенка на страдания?
Генетические изменения, внесенные в эмбрионы, сохранятся во всех клетках взрослого организма, и, соответственно, будут передаваться по наследству. Какой эффект окажет распространение таких модифицированных генов на человеческую популяцию в эволюционном аспекте, не говоря уже о риске возникновения новых евгенических движений?
Именно поэтому Д. Дудна, имеющая колоссальный авторитет в научном мире, призывает своих коллег не торопиться с применением этой технологии на эмбрионах человека, пока не будут разработаны международные этические и законодательные нормы для ее регулирования. В наши дни по всему миру проходят встречи, конференции, конгрессы и симпозиумы, на которых обсуждается будущее CRISPR/Cas. Возможно, от решений, которые будут приняты на них сейчас, зависят судьба человечества и то, как будет выглядеть наш мир в будущем.
В сентябре 2018 г. в новосибирском Академгородке также планируется провести международный конгресс по современным технологиям редактирования геномов, на котором будет обсуждаться технология CRISPR/Cas и, в частности, ее будущее в Российской Федерации.
Литература
Немудрый А. А., Валетдинова К. Р., Медведев С. П. и др. Системы редактирования геномов TALEN и CRISPR/Cas – инструменты открытий // Acta Naturae. 2014. Т. 6. № 3(22). С. 20—42.
Cox D. B., Platt R. J., Zhang F. Therapeutic genome editing: prospects and challenges // Nat Med. 2015. V. 21. N. 2. P. 121—131.
Jinek M., Chylinski K., Fonfara I. et al. A Programmable Dual-RNA-Guided DNA Endonuclease in Adaptive Bacterial Immunity // Science. 2012. V. 337. N. 6096. P. 816—821.
Ma H., Marti-Gutierrez N., Park S. W. et al. Correction of a pathogenic gene mutation in human embryos // Nature. 2017. V. 548. N. 7668. P. 413—419.
: 7 Окт 2017 , Россия Делает Сама , том 75,
№4
Статья на конкурс «био/мол/текст»: Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к молекуле ДНК и повлиять на нее, необходимо использовать точнейшие молекулярные инструменты — белки или РНК. В этой статье рассказывается о новейшем инструменте для внесения мутаций в геном in vivo — сиквенс-cпецифичных нуклеазах.
История изучения ДНК непроста, как и любое значительное исследование. Открыта она была еще в 1868 году Иоганном Фридрихом Мишером, который выделил некое вещество, содержащее азот и фосфор, из остатков клеток в гное [1]. После того, как Мишер обнаружил, что оно обладает кислотными свойствами, вещество назвали нуклеиновой кислотой. Однако долгое время функция ДНК была неясной: ее считали всего лишь способом запасания фосфора в организме. Данная теория считалась правильной почти до середины XX века; в качестве косвенного доказательства ученые ссылались на однообразное, по их мнению, строение молекулы ДНК (состоящей исключительно из четырех различных видов нуклеотидов: дезоксиаденозина — А, дезоксигуанозина — G, дезокситимидина — Т, дезоксицитидина — С).
Носителями генетической информации первоначально предполагались белки. Потребовались опыты нескольких групп ученых, чтобы опровергнуть эту теорию. В частности, эксперименты Освальда Эвери, Колина Мак-Леода и Маклин Мак-Карти в 1944 году [2] показали, что для трансформации бактерий — приобретения болезнетворных свойств ранее безвредной культурой — необходима именно ДНК, выделенная из мертвых болезнетворных бактерий. В 1952 году были проведены опыты Альфреда Херши и Марты Чейз [3], благодаря которым выяснили, что при заражении фагами бактерий внутрь последних впрыскивается только ДНК первых, в то время как белок остается снаружи. Новое поколение фагов, однако, полностью повторяет родительское как по белку, так и по содержащейся ДНК.
Функцию ДНК, естественно, открыли раньше, чем ее вторичную структуру, которая оставалась неизвестной вплоть до 1953 года. Соответственно, из-за этого не могли установить, как проходят такие процессы как передача наследственной информации, как белки распознают определенные последовательности в ДНК и т.п.
В 1949–1951 годах Эрвин Чаргафф сформулировал свои знаменитые правила, которые говорят о строгом соотношении количества азотистых оснований внутри каждой молекулы ДНК [4] (в частности, что количество аденина равняется количеству тимина, а количество цитозина — количеству гуанина); затем Морисом Уилкинсом и Розалиндой Франклин были получены рентгеноструктурные данные, несущие структурную информацию о ДНК. На основании этих двух фактов Френсис Крик и Джеймс Уотсон предложили структуру двойной спирали ДНК [5], которая была доказана позднее в опытах Мэтью Мезельсона и Франклина Сталя [6].
Как только была открыта вторичная структура ДНК, стало легче предсказывать, а затем доказывать экспериментами механизмы различных процессов, происходящих с ДНК. Репликация (удвоение молекулы ДНК), транскрипция (перенос генетической информации с ДНК на РНК), различная регуляция экспрессии генов стали главными проблемами, интересующими молекулярных биологов.
Очевидно, что для осуществления этих процессов необходимы определенные белки, которые, в свою очередь, взаимодействуют как друг с другом, так и с ДНК. И если некоторые стадии протекают неспецифично (например, у эукариот репликация ДНК может начаться во множестве участков ДНК [7]), то, например, регуляция экспрессии генов происходит с помощью взаимодействия белков с довольно консервативными, т.е. строгими последовательностями ДНК.
Эндонуклеазы рестрикции: «Режем ДНК в нужном вам месте!»
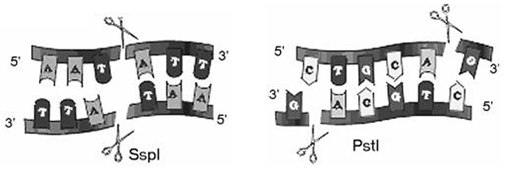
Одними из первых открытых белков, специфически связывающих ДНК, являются эндонуклеазы рестрикции. Это ферменты, которые разрезают ДНК по специфическим нуклеотидным последовательностям, называемым сайтами рестрикции (рис. 1) [8].
Рисунок 1. Рестрикция с образованием а) «тупых» концов; б) «липких» концов
Сам термин «рестрикция» появился благодаря исследованиям фага λ и феномена контролируемой рестрикции и модификации бактериальных вирусов клетками-хозяевами. Этот процесс был впервые обнаружен в результате работ Сальвадора Лурии [9] и Джузеппе Бертани [10] в 1950-х годах. Ученые обнаружили, что если фаг λ хорошо растет в одном штамме Escherichia coli, то в другом штамме его рост падает на несколько порядков, т.е. клетка-хозяин может снижать его биологическую активность. Оказалось, что запрет роста — «рестрикция» — вызывается ферментативным расщеплением ДНК фага. Соответственно, и фермент, отвечающий за этот процесс, назвали ферментом рестрикции.
Сами ферменты были обнаружены в лабораториях Вернера Арбера и Мэттью Мезельсона [11]; причем эндонуклеазы, которые исследовались в их работах, принадлежали, как определили позже, к I классу эндонуклеаз рестрикции. Они разрезают ДНК в случайном месте снаружи от места распознавания, причем как минимум на расстоянии 1000 нуклеотидов.
В 1970-х годах Гамильтон Смит, Томас Келли и Кент Велкокс выделили и охарактеризовали первую эндонуклеазу рестрикции II класса. Этот тип ферментов рестрикции более удобен для лабораторного использования, поскольку расщепляет ДНК внутри своего сайта распознавания, который, как правило, представляет собой палиндром из 4–8 нуклеотидов. Кроме того, эндонуклеазы этого класса не нуждаются в энергетической молекуле АТФ для активности, — только в ионах магния в качестве кофактора.
В 1990-х и ранних 2000-х годах были открыты другие представители данного семейства, которые не соответствовали всем критериям этого класса ферментов [12]. На данный момент уже открыты эндонуклеазы типов IIB, IIE, IIF, IIG, IIM, IIS, IIT… Возможно, в будущем этот список еще значительно расширится.
Существует также III класс эндонуклеаз рестрикции. Они были также открыты как компоненты прокариотической защитной системы против чужеродной ДНК. Эндонуклеазы III типа распознают две отдельных последовательности ДНК длиной 5–6 нуклеотидов и разрезают её примерно через 20–30 пар после сайта распознавания. Для их работы необходимы молекулы АТФ.
Эндонуклеазы рестрикции используют для обработки ДНК в различных лабораторных экспериментах. Обычно их применяют для вставки генов в процессах генного клонирования и экспериментах по исследованию белков.
Кроме того, эндонуклеазы могут быть использованы для выявления различий в аллелях гена [13]. Это возможно только в случае, если мутация произойдет в сайте узнавания, содержащемся внутри аллеля. Таким образом, отпадает нужда в дорогостоящем секвенировании гена; в частности, до изобретения секвенирования обработка эндонуклеазами рестрикции использовалась для картирования геномов.
Одно из новейших применений нуклеаз — внесение с помощью них различных изменений в геном клетки, таких как мутации уже имеющихся генов, вставка новых генов или вырезание исходных. Это очень перспективное направление генной инженерии с широчайшими возможностями практического применения! О нем будет рассказано в следующем разделе.
Эндонуклеазы — это эффекторы, т.е. белки действия. Если они окажутся у цели, то точно ее разрежут. Но природные белки распознают лишь небольшое число последовательностей ДНК, что накладывает огромные ограничения на использование этого уникального инструмента. Ах, если бы можно было доставить эндонуклеазу к любой желаемой последовательности ДНК!..
Революция в области ДНК-связывающих белков: «Доставим ваш белок по любому адресу ДНК, используя TAL-эффекторы или CRISPR/Cas9-систему»
Одной из наиболее заманчивых идей для ученых является возможность напрямую точечно влиять на работу клетки. Для этого необходимо прицельно воздействовать на ДНК именно в области интересующего гена. Воздействие может быть разного характера: включение/выключение гена, внесение мутации и др. Для этого потребовалось уметь синтезировать белки, узнающие конкретную последовательность ДНК («следопыты»), к которым можно было бы пришить белки «действия».
Недавно открытые белки TAL-эффекторы и система Cas9 произвели настоящую революцию в нацеливании различных эффекторов на специфическую последовательность ДНК!
TAL-эффекторы: «Используем паразитов во благо»
TAL-эффекторы (Transcription Activator Like Effectors) — белки, синтезируемые многочисленным видами бактерий рода Xanthomonas — паразитами растений. Они были открыты в 2009 году практически одновременно несколькими группами ученых. TAL-эффекторы активируют считывание нужных паразитам генов в растениях-хозяевах (крайне специфично связываясь с хозяйской ДНК), что облегчает бактериальную колонизацию этого растения и выживание бактерий внутри него [14].
TAL-эффектор можно мысленно поделить на три части (рис. 2); наибольший интерес представляет средняя, крайне консервативная центральная область белка, состоящая из повторяющихся блоков размером 34 аминокислоты. В 2009 же году была показана простая и однозначная связь между повторами и узнаваемыми нуклеотидами. Блоки отличаются друг от друга лишь аминокислотами № 12 и № 13, которые и определяют вид нуклеотида, распознаваемый данным мономером. На каждый из четырех нуклеотидов ДНК приходится определенное сочетание этих аминокислот TAL-эффектора [15]; т.е. можно представить себе этот белок как паровозик, состоящий из одинаковых вагонов, центральное окошко которых покрашено в один из четырех цветов.
Рисунок 2. Строение TAL-эффектора на примере avrBs3
Простота «TALE-кода» открывает многочисленные возможности для биологического применения этих белков. Недавние исследования показали, что можно специально подобрать «вагоны» для искусственного «паровозика» и синтезировать ранее не существовавшие в природе белки для узнавания конкретных последовательностей ДНК в различных типах клеток — как растений, так и млекопитающих. Многие группы ученых уже используют искусственные TAL-эффекторы, узнающие новые последовательности ДНК, например, в томатах, Arabidopsis thaliana [16] и клетках человека [17].
Синтезированные TAL-эффекторы также сшивают с каталитическим доменом нуклеазы (см. раздел «Эндонуклеазы рестрикции») для создания TAL-эффекторных нуклеаз. Эти нуклеазы могут быть полезны для генной инженерии и генной терапии [18].
TAL-нуклеазы используют для создания двуцепочечных разрывов в строго определенном месте ДНК. Известно, что нарушенные таким образом гены клетка может чинить двумя путями: либо просто соединением концов (что может привести к случайным мутациям), либо заново синтезируя поврежденную цепь по комплементарной ей цепи ДНК (т.н. гомологичная рекомбинация).
Во втором случае вырезается значительный по длине участок ДНК, а вместо него по комплементарной (на краях разрыва) матрице синтезируется вставка, закрывающая брешь [19]. Если в клетку поместить ДНК специально мутированного гена, то он будет использован в качестве донорной матрицы, и в геном встроится желаемая мутация. Можно таким методом даже вырезать отдельные гены — или вставлять новые! Таким образом, благодаря разработанной технике сборки ДНК-узнающих повторов, TAL-эффекторы в составе гибридных белков предоставляют возможность направить желаемый эффектор к любой специфической последовательности ДНК — и добиться самых разных воздействий на ДНК: от регуляции транскрипции до внесений мутаций.
CRISPR/Cas9 система: «Неожиданное альтернативное применение защитного комплекса бактерий»
В нашем организме, после того, как мы переболели какой-то болезнью, остаются клетки памяти иммунной системы, которые при повторном попадании в организм вредителей активизируются и помогают ускоренно справиться с ними.
Бактерии справляются со своими патогенами с помощью аналогичной «системы памяти»: CRISPR/Cas-системы обеспечивают иммунитет бактерий и архей против вирусов и плазмид. Этот защитный комплекс состоит из:
- «блокнотика памяти» — кассеты CRISPR, куда скопированы кусочки уникальных последовательностей ДНК поверженных вредителей, разделенные идентичными повторами;
- двух РНК, которые находят жертву — последовательность ДНК повторно вторгшегося патогена;
- белка, приводящего к подавлению чужеродных нуклеиновых кислот.
Этот комплекс был открыт в 2012 году при совместной работе ученых из США, Швейцарии, Австрии и Швеции [20], [21].
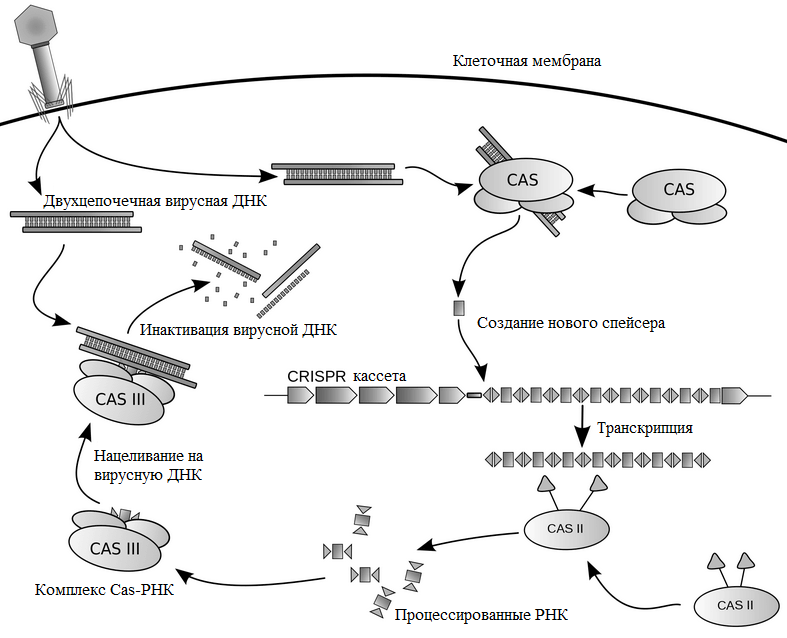
Иммунитет, обусловленный CRISPR/Cas, возникает за три стадии (рис. 3). В первой фазе бактерии или археи, у которых в геноме есть «блокнотик для записи» — CRISPR-кассета, — отвечают на появление вируса включением в конец кассеты коротких фрагментов чужеродной ДНК. На следующей стадии происходит транскрипция — считывание этой свежевключенной последовательности (образование описанных выше двух РНК) и обработка их нуклеазами. Теперь эти РНК могут специфично связаться с вирусной ДНК, и это взаимодействие через цепь событий приводит к ее расщеплению и «смерти» вредителя.
Рисунок 3. Схема работы комплекса Cas—РНК и CRISPR-кассеты
Грубо говоря, ситуация напоминает сказку про репку: первая РНК связывается с «репкой» — чужеродной ДНК — и «зовёт» вторую, вторая — специальный белок Cas9, который уже осуществляет двухцепочечный разрыв цепи чужой ДНК [22].
Несмотря на то, что в природе две РНК системы Cas9 разделены, учёные показали, что химерная РНК, представляющая собой сшитые в одну цепь вышеуказанные РНК, так же способна направлять Cas9 к ДНК-мишени. Более того, при соблюдении ряда условий можно менять последовательность первой внутри химерной РНК так, чтобы нацеливать Cas9 на желаемые гены.
Эта система даже проще TAL-эффекторов, поскольку для распознавания одного дезоксирибонуклеотида ДНК не нужен громоздкий «вагон» белка: один рибонуклеотид РНК легко и точно узнаёт комплементарный ему дезоксирибонуклеотид ДНК мишени! Экономия как в размере инструмента, так и в легкости его синтеза.
К настоящему времени показано, что эта система работает не только в археях и бактериях, но и в организмах рыб (Danio rerio), а также в клетках млекопитающих [23]. Уже установлено, что, как и в случае TAL-эффекторных нуклеаз, обработка ДНК Cas9-системой приводит к эффективному (10–30% случаев) возникновению мутаций.
* * *
Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к ДНК и повлиять на нее, необходимо спуститься на молекулярный уровень и использовать белки или РНК. Сейчас развитие данных направлений идет стремительно, каждый месяц случаются значительные прорывы в этой области. Кто знает, какие чудеса ожидают нас через год? Возможно, будет найдена новая система, максимально упрощающая исходно сложный и кропотливый процесс вмешательства человека в работу природы.
- Ralf Dahm. (2005). Friedrich Miescher and the discovery of DNA. Developmental Biology. 278, 274-288;
- O. T. Avery. (1944). STUDIES ON THE CHEMICAL NATURE OF THE SUBSTANCE INDUCING TRANSFORMATION OF PNEUMOCOCCAL TYPES: INDUCTION OF TRANSFORMATION BY A DESOXYRIBONUCLEIC ACID FRACTION ISOLATED FROM PNEUMOCOCCUS TYPE III. Journal of Experimental Medicine. 79, 137-158;
- A. D. Hershey. (1952). INDEPENDENT FUNCTIONS OF VIRAL PROTEIN AND NUCLEIC ACID IN GROWTH OF BACTERIOPHAGE. The Journal of General Physiology. 36, 39-56;
- ERWIN CHARGAFF, STEPHEN ZAMENHOF, CHARLOTTE GREEN. (1950). Human Desoxypentose Nucleic Acid: Composition of Human Desoxypentose Nucleic Acid. Nature. 165, 756-757;
- J. D. WATSON, F. H. C. CRICK. (1974). Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid. Nature. 248, 765-765;
- M. Meselson, F. W. Stahl. (1958). The replication of DNA in Escherichia coli. Proceedings of the National Academy of Sciences. 44, 671-682;
- Heinz-Peter Nasheuer, Richard Smith, Christina Bauerschmidt, Frank Grosse, Klaus Weisshart. (2002). Initiation of eukaryotic DNA replication: Regulation and mechanisms. Progress in Nucleic Acid Research and Molecular Biology. 41-94;
- Richard J. Roberts, Kenneth Murray. (1976). Restriction Endonuclease. CRC Critical Reviews in Biochemistry. 4, 123-164;
- Luria S.E. and Human M.L. (1952). A nonhereditary, host-induced variation of bacterial viruses. J. Bacteriol. 64, 557–569;
- Bertani G. and Weigle J.J. (1953). Host controlled variation in bacterial viruses. J. Bacteriol. 65, 113–121;
- Seymour Lederberg, Matthew Meselson. (1964). Degradation of non-replicating bacteriophage DNA in non-accepting cells. Journal of Molecular Biology. 8, 623-628;
- A. Pingoud. (2001). Structure and function of type II restriction endonucleases. Nucleic Acids Research. 29, 3705-3727;
- R. Zhang, Z. Zhu, H. Zhu, T. Nguyen, F. Yao, et. al.. (2005). SNP Cutter: a comprehensive tool for SNP PCR-RFLP assay design. Nucleic Acids Research. 33, W489-W492;
- Jens Boch, Ulla Bonas. (2010). XanthomonasAvrBs3 Family-Type III Effectors: Discovery and Function. Annu. Rev. Phytopathol.. 48, 419-436;
- M. J. Moscou, A. J. Bogdanove. (2009). A Simple Cipher Governs DNA Recognition by TAL Effectors. Science. 326, 1501-1501;
- R. Morbitzer, P. Romer, J. Boch, T. Lahaye. (2010). Regulation of selected genome loci using de novo-engineered transcription activator-like effector (TALE)-type transcription factors. Proceedings of the National Academy of Sciences. 107, 21617-21622;
- Jeffrey C Miller, Siyuan Tan, Guijuan Qiao, Kyle A Barlow, Jianbin Wang, et. al.. (2011). A TALE nuclease architecture for efficient genome editing. Nat Biotechnol. 29, 143-148;
- De Francesco L. (2011). Move over ZFNs. Nat Biotechnol. 29, 681-684;
- Alberts B. et al. Chapter 5: DNA Replication, Repair, and Recombination. In: Molecular Biology of the Cell (4th Edition). New York: Garland Science, 2002. 845 p.;
- M. Jinek, K. Chylinski, I. Fonfara, M. Hauer, J. A. Doudna, E. Charpentier. (2012). A Programmable Dual-RNA-Guided DNA Endonuclease in Adaptive Bacterial Immunity. Science. 337, 816-821;
- Элементы: «Прокариотическая система иммунитета поможет редактировать геном»;
- Woong Y Hwang, Yanfang Fu, Deepak Reyon, Morgan L Maeder, Shengdar Q Tsai, et. al.. (2013). Efficient genome editing in zebrafish using a CRISPR-Cas system. Nat Biotechnol. 31, 227-229;
- Seung Woo Cho, Sojung Kim, Jong Min Kim, Jin-Soo Kim. (2013). Targeted genome engineering in human cells with the Cas9 RNA-guided endonuclease. Nat Biotechnol. 31, 230-232.
Враг №2: активные формы кислорода Самый распространенный мутаген. Хитрость заключается в том, что эти активные формы генерируются в ходе самых обычных химических реакций, которые протекают в человеческом теле. Тут может возникнуть недоумение, ведь кислород — это газ, который содержится в атмосфере нашей планеты, с ним ассоциируется дыхание полной грудью, свежесть и еще какие-то приятные ощущения из рекламы стиральных порошков.
Разгадка кроется в названии. Кислород окисляет вещества, которые встречает на своем пути. Вспомните перекись водорода, которую выливают на разбитую коленку — примерно то же самое происходит в клеточных масштабах при выделении активных форм кислорода. Активные формы кислорода разрушают мембраны, из которых построены живые клетки, выдергивают отдельные основания из цепи ДНК и вносят разрывы. Страшно не только то, что они делают, но и то, как изощренно это происходит. Поскольку выделение АФК осуществляется постоянно, при поломке нейтрализующего их механизма клетки постоянно подвергаются бомбардировке мутагенами и гибнут в муках.
Доказано: от окисления и активных радикалов спасают антиоксиданты. Это вещества, которые содержатся в свежих ягодах и фруктах, зеленом чае, орехах и красном вине. Они переводят радикалы в неактивную форму. Иными словами, антиоксиданты — это такие альтруисты. Они выходят на улицу, видят, как хулиганы разрушают стены, и принимают удар на себя. Антиоксиданты обладают множеством чудесных свойств, одно из которых — защита от старения. Согласно некоторым гипотезам, старение ассоциировано с выделением АФК. Отдельно выделяется легион — витамин Е — собирательное название для нескольких жирорастворимых веществ, обладающих антиоксидантной активностью. При поступлении в пищеварительную систему ингредиенты витамина Е проходят отбор в печени, и уже в круг обмена веществ вступает в основном альфа-токоферол.
Важно учитывать собственную генетическую предрасположенность к усвоению витаминов, так как антиоксиданты при чрезмерном потреблении вредны: они могут препятствовать усвоению других микроэлементов.
Враг № 3: афлатоксины. Название принадлежит группе ядов-канцерогенов, вырабатываемых некоторыми видами плесени. Афлатоксины — это ответ на детский вопрос: «Почему нельзя есть землю и опавшие листья?», на взрослый вопрос: «Почему у чая есть срок годности?» и на старческий вопрос: «Почему нельзя есть заплесневевшую крупу?» Когда условия хранения не соблюдаются, на продукте, как на питательной среде, растут плесневые грибы рода Aspergillus. Опасность может подстерегать в крупах, специях, орехах, чае, молоке, яйцах, мясе, сухофруктах, хлебе и промышленных соках. Плесень может вырасти в результате неправильного или длительного хранения, а ароматизирующая добавка заглушит неприятный запах. Если доза афлатоксинов не смертельная, но регулярная, это может послужить причиной для развития цирроза и рака печени. Особую опасность продукты с афлатоксинами представляют для будущих матерей: помимо общего отравления, афлатоксины могут нарушить эмбриогенез.
Доказано: полезные пищевые привычки помогут избежать этого врага. Будьте аккуратны и не ешьте просроченные продукты. Старайтесь тщательно мыть продукты и готовить еду непосредственно перед употреблением. Впрочем, люди с непереносимостью глютена, лактозы или кофеина в отношении афлатоксина чувствуют себя немного спокойнее: больше половины продуктов из группы риска уже исключены из их меню. Такая особенность пищевого поведения, как привычка переедать, может быть вдвойне вредна в данной ситуации.
Враг №4: бензол. Бензол — химическое соединение, без которого невозможно представить современную жизнь. Это токсин и канцероген, который входит в состав нефти и бензина, а также широко применяется в производстве лекарств, пластмасс, резины и красителей. Если поместить человека в замкнутое пространство и постепенно закачивать туда бензол, то сначала он почувствует эйфорию. Затем появятся сонливость, тошнота, головная боль, мышечные подергивания. Если оставить испытуемого в этой камере на длительное время, то он умрет, если же его выпустить, то можно будет наблюдать целый комплекс расстройств, вызванных отравлением бензолом. Однако нам интересно не это. Бензол часто встречается в некачественной косметической продукции и пластмассовых изделиях, то есть не исключено систематическое отравление бензолом в небольших количествах, что может провоцировать возникновение различных видов гемато-онкологических заболеваний.
Доказано: витамины группы В — Ниацин, фолат и кобаламин — необходимы для репарации ДНК. Дефицит этих витаминов в первую очередь заметен при отравлении бензолом. Зачастую люди получают витамины этой группы с мясом животных. Подробнее узнать о том, на какие процессы влияют витамины группы В и как диагностировать их недостаток, можно по ссылке.
Берегите себя. Враги в лице мутагенов могут быть повсюду. Когда речь заходит о здоровом образе жизни, тем, кто пытается изменить все своими силами, приходится балансировать между массой советов и здравым смыслом. Граница зыбкая и устоять на ней больше шансов у того,, кто знает себя и не наносит себе вред.
Зачем ученые редактируют ДНК человека? Насколько это опасно и чего ждать в будущем?
В ходе давнего эксперимента ученого Хэ Цзянкуя в Китае родились дети с отредактированной ДНК, однако спустя некоторое время генетик пропал без вести. По просьбе Esquire наш эксперт, руководитель отдела новостей Владимир Губайловский рассказал историю Хэ и объяснил, что будет, если редактирование генома человека станет нормой.

Невероятное количество фильмов снято о людях, которые используют возможности организма на 100%. Но, как известно, все сюжеты для научно-фантастических картин вдохновлены реальностью. Так, один китайский учёный в 2018-м году впервые в истории человечества отредактировал ДНК человека в качестве научного эксперимента. И эта разработка стала толчком для ученого мира.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Редактирование генома человека в 2021
К середине июля 2021 ВОЗ опубликовала два доклада, в которых содержатся первые глобальные рекомендации, призванные помочь сделать редактирование генома человека инструментом общественного здравоохранения. В них учтены безопасность, эффективность и этические принципы.
Эти перспективные доклады стали результатом проведения множества консультаций по вопросам редактирования соматического, зародышевого и наследуемого генома человека. Они проводились на протяжении двух лет — в них приняли участие сотни людей из разных стран мира, включая ученых и исследователей, группы пациентов, религиозных лидеров и коренные народы — было определено несколько точек зрения.
«Редактирование генома человека способно расширить наши возможности лечить и излечивать болезни, однако полный эффект может быть достигнут только в том случае, если мы применим эти возможности на благо всех людей вместо того, чтобы усиливать неравенства в отношении здоровья между странами и внутри стран», – сказал Генеральный директор ВОЗ д-р Тедрос Адханом Гебрейесус.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Но это сейчас, а что же случилось почти 3 года назад?
25 ноября 2018 года. Гонконг
Около 19:00 китайский ученый публикует на YouTube ролик About Lulu and Nana: Twin Girls Born Healthy after Gene Surgery («Лулу и Нана: двойняшки родились здоровыми после генной хирургии»). В кадре Хэ сидит в хорошо освещенном кабинете, на нем голубая рубашка, он аккуратно подстрижен и доброжелательно улыбается.
«Две красивые китайские малышки, Лулу и Нана, пришли в этот мир такими же здоровыми, как и другие дети», — говорит он. Эти девочки — первые в истории люди с отредактированными ДНК. Они развивались из эмбриона, в который была внесена мутация, гарантирующая иммунитет от ВИЧ.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Хэ очень радовался за родителей, которых называл по именам — Марк и Грейс. Это псевдонимы. Их настоящие имена, равно как и любые данные о них, засекречены. Ученый расплывался в улыбке, вспоминая, как ВИЧ-инфицированный Марк благодарил его за рождение здоровых детей. Лицо Хэ становилось серьезным, когда он резко высказывается против создания «дизайнерских» детей — термин, подразумевающий редактирование ДНК с целью улучшений, влияющих на внешность, умственные и физические данные человека. «Редактирование допустимо только в том случае, когда это необходимо для спасения человеческой жизни, защиты от тяжелой наследственной болезни», — подчеркивал он.
Хэ сравнивал рождение Лулу и Наны с открытием экстракорпорального оплодотворения: «В 1960-е технологию встретили резко отрицательно, а сегодня это общепринятая практика».
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
На видео Хэ спокоен. Он улыбается. Видеообращение было записано на английском языке и с китайскими субтитрами. В Китае YouTube недоступен. Этот ролик — обращение к западному миру. И мир его услышал.
Тот же день. Кембридж, Массачусетс, США
Обозреватель научного журнала MIT Technology Review Антонио Регаладо посмотрел ролик китайского ученого и попытался установить его достоверность. Журналист нашел заявки, поданные Хэ на проведение эксперимента по редактированию генома человека, и номер сертификата этического контроля, выданный крупным госпиталем в Шэньчжэне — по‑видимому, того самого, в котором и родились девочки с отредактированной ДНК.
Редактирование генома человека — мечта научного мира, и в то же время, катастрофа, которую может сотворить генная инженерия.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Регаладо опубликовал статью, которая собрала больше просмотров, чем видеоролик Хэ на тот момент. Американское научное сообщество было взбудоражено. Ученые с нетерпением ждали выступления Хэ на Втором саммите по редактированию генома человека в Гонконге 28 ноября 2018 года.
26 ноября. Гонконг
Хэ приезжает в гостиницу для участников саммита и встречается с Дженнифер Дудной, американским исследователем и одной из авторов технологии редактирования ДНК. Они обсуждают предстоящее выступление китайского ученого. Хэ должен был представить свои работы по редактированию эмбрионов мышей и обезьян — но оказалось, что зашел намного дальше. Как позже рассказала Дудна журналистам: «Он держался одновременно высокомерно и наивно».
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Вечером 26 ноября Дудна уговаривает Хэ встретиться с другими генетиками. Ученые задают ряд вопросов: «Сколько было отредактировано эмбриональных клеток?», «Как проверялось наличие мутации?», «Знали ли участники эксперимента о возможных рисках?», «Было ли получено разрешение на эксперимент?». Хэ не ответил практически ни на один. В какой-то момент он просто вышел из комнаты, собрал вещи и уехал из гостиницы.
В тот же день Хэ дал интервью Associated Press — и новость о рождении близняшек с отредактированной ДНК оказалась на первых полосах ведущих мировых СМИ. The New York Times выходит с большим материалом: «Эксперимент Хэ открывает дверь рождению «дизайнерских» детей». В этом же номере — обращение за подписью 122 китайских ученых, где они называют своего коллегу «сумасшедшим», а его эксперимент — «страшным ударом по репутации китайской науки». До выступления Хэ остается чуть больше суток.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
28 ноября. Гонконг. Второй саммит по редактированию генома человека
Хэ поднимается на трибуну и объявляет о рождении Лулу и Наны. Он говорит быстро и сбивчиво, от доброжелательности и спокойствия, которые вы видели на ролике с YouTube выше, не осталось и следа. Он игнорирует вопросы из зала, быстро спускается со сцены — и исчезает.
Хэ Цзянкуй выступает на Втором саммите по редактированию генома человека, Гонконг, 28 ноября 2018 года.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
28 ноября 2018 года Хэ Цзянкуя последний раз видели на публике.
Вскоре оргкомитет саммита публикует заявление, в котором резко осудит эксперимент Хэ. Замминистра по науке и технологиям Китая Сюй Наньпин фактически зачитывает ученому приговор: «Инцидент с генетически измененными младенцами, о котором сообщают СМИ, грубо нарушает законы Китая». Журналисты окружают Дженнифер Дудну. На вопрос: «Не следует ли ввести мораторий на редактирование эмбрионов человека?» она отвечает: «Уже слишком поздно».
Октябрь, 2018 год
Ведущий популярной передачи BBC HARDtalk Стивен Сакур приглашает в студию известного генетика Роберта Пломина. Он только что опубликовал книгу Blueprint: How DNA Makes Us Who We Are («Как ДНК делает нас теми, кто мы есть»), моментально ставшую бестселлером.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
На основании почти 30-летних исследований Пломин делает вывод: генетическая наследственность определяет почти 50% личных и умственных способностей человека. Другие 50% формируются условиями внешней среды, воспитания и образования.
«Если у ребенка слабая память, то, вполне вероятно, она и останется слабой, как бы ни бились учителя и родители, — разводит руками ученый. — Он не вырастет лучшим в мире математиком. А если гены значат так много в жизни человека, то редактирование генома человека — по крайней мере в перспективе — неизбежно. И не только в случае наследственных болезней. Вы хотите, чтобы ваш ребенок вырос умным? Разве кто-то не хочет?»
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Декабрь, 2018 год
Уже месяц о местонахождении Хэ неизвестно ничего. Мировая пресса изучает его биографию.
Будущий ученый родился в 1984 году в небольшой провинции Хунань на юго-востоке Китая. Родители — фермеры, всю жизнь выращивают рис. Хэ успешно окончил школу, увлекался физикой, даже соорудил домашнюю лабораторию. Он продолжил изучать предмет в Университете науки и технологий в Хэфэе, а затем — в американском Университете Райса в Хьюстоне.
Однокурсники вспоминают, что Хэ был общительным и активным студентом — особенно ему нравились ухоженные футбольные поля в американском вузе. Но будущий ученый был заметен не только на футболе — его университетский руководитель, биоинженер Майкл Дим отмечал блестящие успехи подопечного в науке. Хэ проводил эксперименты на живых клетках и организмах, а после окончания Университета Райса, в 2011 году, был приглашен в Стэнфорд.До экспериментов, которые поставили Дженнифер Дудна, Эммануэль Шарпентье, Фэн Чжан и другие выдающиеся генетики и которые привели к открытию технологии редактирования ДНК человека, оставалось меньше двух лет. Многие из этих экспериментов были проведены в Беркли, в часе езды от Стэнфорда.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Хэ и сотрудница лаборатории Direct Genomics. Шэньчжэнь, провинция Гуандун, Китай. 4 августа 2016 года. До открытия Хэ возможности редактировать ДНК человека ещё 4 с лишним года.
В 2012-м блестящему молодому специалисту Хэ власти Китая предложили вернуться на родину в рамках программы поддержки молодых ученых «Тысяча талантов». Он согласился, получил грант в миллион юаней и начал преподавать в Университете Шэньчжэня, в 28 лет став самым молодым его доцентом. Но вскоре осознал, что он пропускает самое интересное и главные открытия были совершены без него.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Южный университет науки и техники в Шэньчжэне, Китай. Там преподавал учёный, в 2018-м году открывший способ редактировать ДНК человека.
В последующие годы Хэ не раз приезжал в Америку и встречался с генетиками. В 2017-м представил свою первую работу по редактированию эмбрионов мышей и обезьян. Хэ не раз говорил о возможном редактировании генома человека, но его выступления и работы не производили на коллег особого впечатления. За ученым закрепилось прозвище «Падающая звезда».
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Хэ все чаще говорил о редактировании ДНК — но не мышей или обезьян, а человека. Такие эксперименты проводят на эмбриональных клетках, которые затем уничтожают в течение трех-пяти дней. Но китайский ученый задавал коллегам вопросы: «Почему бы не пойти дальше?», «Почему не дать отредактированной клетке развиться, не дать «улучшенному» человеку родиться?». Как отмечали позднее в интервью американские ученые — и генетики, и специалисты по проблемам этики науки, — они думали, что Хэ говорит гипотетически — о далеком будущем. Оказалось, они ошибались.
Январь, 2017 год
Хэ начал подготовку к своему эксперименту. Он отобрал группу из нескольких семейных пар, в которых мужчина был ВИЧ-инфицирован, а женщина — здорова. Ученый предложил им отредактировать эмбрион так, чтобы из него развился не просто здоровый ребенок, но с гарантированной защитой от ВИЧ для всех своих потомков. И уже весной эксперимент был поставлен.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
В пяти парах женщины не смогли забеременеть после ЭКО, одна пара вышла из эксперимента, еще про одну не известно ничего. И только одна женщина — Грейс — родила. Так появились Лулу и Нана.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
28 декабря 2018 года
The New York Times публикует статью под заголовком «Китайского ученого, отредактировавшего ДНК человека, держат под стражей». Журналистам газеты удалось снять видео: Хэ на балконе третьего этажа университетского кампуса в Шэньчжэне. Балкон был огорожен металлической сеткой, а самого ученого опознал на снимках один из его бывших сотрудников.
Хэ Цзянкуй, учёный, впервые в истории отредактировавший ДНК человека, на балконе университетского кампуса. Шэньчжэнь, Китай. Декабрь 2018 года.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Двери в апартаменты, где находился ученый, охраняли четверо людей в штатском. Когда журналисты попытались войти, их остановили и задали вопрос — почему они решили, что Хэ находится здесь? Попасть внутрь им не удалось. The New York Times не удалось выяснить, кем были люди в штатском — имели ли они отношение к полиции города или другой организации. Сотрудники университета отказывались комментировать ситуацию вокруг ученого и генетически отредактированных людей.
После этой публикации стало понятно, что Хэ жив и может общаться с семьей — на том же балконе журналисты засняли жену ученого и их ребенка.
21 января 2019 года
Китайское информационное агентство «Синьхуа» публикует официальный комментарий представителя властей провинции Гуандун, в которой находится Университет Шэньчжэня. «Китайский исследователь Хэ Цзянкуй бросил вызов государственным запретам и провел исследование, добиваясь личной славы и выгоды».
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Ученого обвинили в подделке сертификата этического контроля, который он предъявил участникам эксперимента и своим сотрудникам, тем самым введя их в заблуждение. «Хэ и другие связанные с экспериментом по редактированию генома человека сотрудники и организации будут наказаны в соответствии с законом. Подозреваемые в совершении преступлений будут заключены под арест». Лулу и Нана, а также еще одна женщина, вынашивающая ребенка с отредактированной ДНК, находятся под постоянным наблюдением врачей, утверждалось в официальном заявлении.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Февраль, 2019 год
Ученый устанавливает тонкую стеклянную пипетку в микроскоп — лишь маленькая деталь эксперимента по редактированию генома человека. Лаборатория в Шэньчжэне, провинция Гуандун на юге Китая.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
После рождения Лулу и Наны мутация CCR5delta32, внесенная Хэ в их ДНК, привлекла к себе общественное внимание. Еще в 2016 году при опытах на мышах ученые обнаружили, что эта мутация влияет на работу гиппокампа, значительно улучшая память. На Втором саммите по редактированию генома человека в Гонконге ученые задали Хэ вопрос, знает ли он о влиянии CCR5delta32 на работу мозга? Китайский ученый ответил, что знаком с исследованием, но данных недостаточно.
Носители мутации CCR5delta32 имеют большие шансы на восстановление после инсульта, чем обычные люди. CCR5 — это первый ген, про который можно уверенно сказать, что его изменение влияет на работу мозга.На сегодняшний день эта мутация — набор сплошных плюсов: дает иммунитет к ВИЧ, улучшает память и способности к обучению, помогает быстрее восстанавливаться после инсульта или черепно-мозговой травмы. Единственный известный на данный момент минус — снижение сопротивляемости организма к лихорадке Западного Нила, но это заболевание достаточно редкое. Проблема только в том, что ни один генетик не может подтвердить, что искусственно созданная мутация не несет в себе какие-то другие риски и не спровоцирует в организме человека непредсказуемых изменений.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Фэн Чжан, Эммануэль Шарпентье и еще 16 генетиков призвали ввести во всем мире пятилетний мораторий на редактирование генома человека в марте 2019-го года.
В марте 2019 года Фэн Чжан, Эммануэль Шарпентье и еще 16 генетиков призвали ввести во всем мире пятилетний мораторий на использование генетического редактирования человеческих эмбрионов для рождения модифицированных людей. Ученые будут добиваться поддержки моратория рядом стран.
Тем временем под видео «Лулу и Нана: двойняшки родились здоровыми после генной хирургии» больше 2,5 тысячи комментариев. «Трейлер продолжения «Гаттаки» выглядит отлично», — пишет один комментатор («Гаттака» — фильм-антиутопия 1997 года об обществе генно-модифицированных людей). «Я в восторге, но мне так страшно», — пишет другой. «Вы только что открыли ящик Пандоры», — пишет третий.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
30 декабря 2019-го года стало известно, что суд в китайском городе Шэньчжэнь приговорил Хэ Цзянькуя к трем годам тюрьмы и штрафу в три миллиона юаней (около 465 тысяч долларов). Об этом сообщила China Daily.
Двое коллег Хэ Цзянькуя, помогавшие ему в проведении эксперимента, получили два и полтора года тюрьмы соответственно. Также они обязаны заплатить штрафы в 500 тысяч и миллион юаней (77 и 154 тысячи долларов).
Суд признал учёного Хэ Цзянькуя и его коллег виновными в незаконном редактировании генома человека.
Материал был впервые опубликован на сайте pravilamag.ru.
Каждый из живых организмов на Земле носит в клетках наследственный материал своих предков. Эти данные называются геномами, и они нужны непосредственно для создания и поддержания деятельности организма. Генная инженерия работает над изменениями в наследственной информации. Рассказываем, что происходит с редактированием геномов прямо сейчас.
Читайте «Хайтек» в
Применение генной инженерии в научных исследованиях
- Нокаут гена
Для изучения функции того или иного гена может быть применён нокаут гена. Так называется техника удаления одного или большего количества генов, что позволяет исследовать последствия подобной мутации.
Для нокаута синтезируют такой же ген или его фрагмент, измененный так, чтобы продукт гена потерял свою функцию. Основные методы реализации: цинковый палец, морфолино и TALEN.
Для получения нокаутных мышей полученную генно-инженерную конструкцию вводят в эмбриональные стволовые клетки, где конструкция подвергается соматической рекомбинации и замещает нормальный ген, а измененные клетки имплантируют в бластоцисту суррогатной матери. У плодовой мушки дрозофилы мутации инициируют в большой популяции, в которой затем ищут потомство с нужной мутацией. Сходным способом получают нокаут у растений и микроорганизмов.
- Искусственная экспрессия
Логичным дополнением нокаута является искусственная экспрессия, то есть добавление в организм гена, которого у него ранее не было. Этот способ генной инженерии также можно использовать для исследования функции генов. В сущности процесс введения дополнительных генов таков же, как и при нокауте, но существующие гены не замещаются и не повреждаются.
- Визуализация продуктов генов
Используется, когда задачей является изучение локализации продукта гена. Одним из способов мечения является замещение нормального гена на слитый с репортерным элементом, например, с геном зеленого флуоресцентного белка GFP. Этот белок, флуоресцирующий в голубом свете, используется для визуализации продукта генной модификации.
Хотя такая техника удобна и полезна, её побочными следствиями может быть частичная или полная потеря функции исследуемого белка. Более изощрённым, хотя и не столь удобным методом является добавление к изучаемому белку не столь больших олигопептидов, которые могут быть обнаружены с помощью специфических антител.
- Исследование механизма экспрессии
В таких экспериментах задачей является изучение условий экспрессии гена. Особенности экспрессии зависят прежде всего от небольшого участка ДНК, расположенного перед кодирующей областью, который называется промотор и служит для связывания факторов транскрипции.
Этот участок вводят в организм, поставив после него вместо собственного гена репортерный, например, GFP или фермента, катализирующего легко обнаруживаемую реакцию. Кроме того, что функционирование промотора в тех или иных тканях в тот или иной момент становится хорошо заметным, такие эксперименты позволяют исследовать структуру промотора, убирая или добавляя к нему фрагменты ДНК, а также искусственно усиливать его функции.
Зачем нужна генная инженерия человека
В применении к человеку генная инженерия могла бы применяться для лечения наследственных болезней. Однако, технически, есть существенная разница между лечением самого пациента и изменением генома его потомков.
Задача изменения генома взрослого человека несколько сложнее, чем выведение новых генноинженерных пород животных, поскольку в данном случае требуется изменить геном многочисленных клеток уже сформировавшегося организма, а не одной лишь яйцеклетки-зародыша. Для этого предлагается использовать вирусные частицы в качестве вектора.
Вирусные частицы способны проникать в значительный процент клеток взрослого человека, встраивая в них свою наследственную информацию; возможно контролируемое размножение вирусных частиц в организме. При этом для уменьшения побочных эффектов учёные стараются избегать внедрения генноинженерных ДНК в клетки половых органов, тем самым избегая воздействия на будущих потомков пациента.
Также стоит отметить значительную критику этой технологии в СМИ: разработка генноинженерных вирусов воспринимается многими как угроза для всего человечества.
С помощью генотерапии в будущем возможно изменение генома человека. В настоящее время эффективные методы изменения генома человека находятся на стадии разработки и испытаний на приматах.
Долгое время генетическая инженерия обезьян сталкивалась с серьёзными трудностями, однако в 2009 году эксперименты увенчались успехом: в журнале Nature появилась публикация об успешном применении генноинженерных вирусных векторов для излечения взрослого самца обезьяны от дальтонизма. В этом же году дал потомство первый генетически модифицированный примат (выращенный из модифицированной яйцеклетки) — обыкновенная игрунка (Callithrix jacchus).
Хотя и в небольшом масштабе, генная инженерия уже используется для того, чтобы дать шанс забеременеть женщинам с некоторыми разновидностями бесплодия. Для этого используют яйцеклетки здоровой женщины. Ребёнок в результате наследует генотип от одного отца и двух матерей.
Однако возможность внесения более значительных изменений в геном человека сталкивается с рядом серьёзных этических проблем. В 2016 в США группа учёных получила одобрение на клинические испытания метода лечения рака с помощью собственных иммунных клеток пациента, подвергаемых генной модификации с применением технологии CRISPR/Cas9.
В конце 2018 года в Китае родились двое детей, геном которых был искусственно изменён (выключен ген CCR5) на стадии эмбриона методом CRISPR/Cas9, в рамках исследований, проводимых с 2016 года по борьбе с ВИЧ. Один из родителей (отец) был ВИЧ-инфицированным, а дети, по заявлению, родились здоровыми.
Поскольку эксперимент был несанкционированным (до этого все подобные эксперименты на человеческом эмбрионе разрешались только на ранних стадиях развития с последующим уничтожением экспериментального материала, то есть без имплантации эмбриона в матку и рождением детей), ответственный за него учёный не предоставил доказательств своим заявлениям, которые были сделаны на международной конференции по редактированию генома.
В конце января 2019 года властями Китая были официально подтверждены факты проведения данного эксперимента. Тем временем учёному было запрещено заниматься научной деятельностью и он был арестован.
Как редактируют человеческий геном?
- Метод «цинковые пальцы»
«Цинковые пальцы» встречаются и в составе человеческих белков. Благодаря этому методу можно сконструировать цепь ZFN так, что она будет узнавать определённый участок ДНК. Это дает возможность точечного воздействия на заданные участки в составе сложных геномов.
Домены «цинковые пальцы» встречаются в составе человеческих факторов транскрипции – белков, регулирующих процесс синтеза РНК с матрицей ДНК. При создании искусственных нуклеаз можно сконструировать цепочку из «цинковых пальцев» так, что она будет узнавать определенный участок ДНК.
Если такая цепочка будет достаточно длинной, она может распознавать относительно протяженные последовательности ДНК, состоящие из ряда тринуклеотидных фрагментов. Это означает реальную возможность точечного воздействия на заданные участки в составе больших сложных геномов.
Однако у метода «цинковых пальцев» обнаружились и серьезные недостатки: во-первых, это не вполне строгое распознавание тринуклеотидных повторов, что приводит к заметному числу расщеплений ДНК в «нецелевых» участках.
Во-вторых, метод оказался весьма трудозатратным и дорогостоящим, поскольку для каждой последовательности ДНК необходимо создать свою оптимизированную белковую структуру zinc-finger нуклеазы. Поэтому система «цинковые пальцы» широкого распространения не получила.
- TALEN
В 2011 году журнал Nature Methods назвал систему TALEN (Transcription Activator-like Effector Nucleases) «методом года» благодаря широкому спектру возможных применений в разных областях фундаментальной и прикладной науки.
TALEN — один из способов направленного внесения разрыва в ДНК с последующим его «залечиванием» — для выключения генов у мышей. Сразу после них эту технологию применили для внесения в мышиный геном мутации, приводящей к развитию одного из наследственных синдромов. Авторам метода моделирования генетически обусловленных болезней удалось не только «испортить» мышиный геном, но и исправить его обратно.
- CRISPR/Cas9
Метод обеспечивает точное воздействие на заданные участки ДНК и может быть использован практически в любой современной молекулярно-биологической лаборатории.
В основе этой системы — особые участки бактериальной ДНК — CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats, или короткие палиндромные кластерные повторы). Разделяют эти повторы спейсеры — короткие фрагменты чужеродной ДНК. Последние встраиваются в геном после того, как ДНК рекомбинирует с её геномом.
Примеры редактирования человека
- Редактирование генома прямо в теле
Заболевание 44-летнего жителя Аризоны Брайана Мадо проявилось еще в раннем детстве. Оно неизлечимо и наследуют его в основном мужчины. Мукополисахаридоз II типа — это метаболическое расстройство: у людей с ним есть мутация в гене, ответственном за производство фермента, который участвует в расщеплении сложных углеводов. В итоге они накапливаются в клетках и вызывают многочисленные патологии органов.
Мужчина решил принять участие в клиническом испытании нового метода — генной терапии. Это лишь первая фаза исследования, а всего до регистрации терапии (то есть до разрешения применять этот метод для всех больных с синдромом Хантера) их должно быть три.
Метод, который использовали в случае Брайана Мадо, позволяет редактировать геном прямо в теле человека — и при этом достаточно точно попадать в конкретный участок ДНК. Редактирование происходит с помощью так называемых «цинковых пальцев».
- Генетически модифицированные дети
Китайский исследователь Хэ Цзянькуй отредактировал геномы человеческих эмбрионов перед процедурой искусственного оплодотворения, в результате чего на свет появились двое детей с измененной ДНК.
С помощью системы CRISPR/Cas9 исследователь отредактировал геномы эмбрионов семи пар во время репродуктивного лечения. В результате одной из беременностей от здоровой матери и ВИЧ-инфицированного отца родились две девочки-двойняшки с измененной ДНК. Хэ Цзянькуй пояснил, что удалил у детей ген CCR5, благодаря чему они получили пожизненный иммунитет к ВИЧ.
- Возвращение зрения с помощью генной терапии
Для восстановления зрения можно использовать оптогенетические технологии, с помощью которых работой нейронов можно управлять с помощью светочувствительных белков бактерий и вспышек лазера.
Руководствуясь этой идеей, биологи создали вирус, который может проникать в ганглионарные нейроны. Эти нервные клетки отвечают за передачу сигналов из сетчатки в мозг человека. Попавший в ганглионарный нейрос вирус заставляет его производить подобные сигнальные молекулы. Однако эта процедура не возвращает зрение сама по себе, так как белки бактерий реагируют на свет не так, как палочки и колбочки сетчатки.
Чтобы решить эту проблему, профессор Базельского университета Ботонд Роска и профессор Питтсбургского университета Хосе Сахель создали специальные очки, которые преобразуют поступающие в них изображение в понятный мозгу формат и стимулируют ганглионарные клетки вспышками лазера. В результате пациент может видеть силуэты крупных предметов и объектов и совершать другие сложные действия
Читать далее:
Ученые проверили теорию панспермии на тихоходках: они могут путешествовать в космосе
Ученые выяснили, что сверхобогащенное золото образуется как простокваша
Крошечный водородный двигатель заменил аналоги на ископаемом топливе