Если в древности, появление на свет детей с хромосомными патологиями считалось карой Божьей, то в наши дни предвидеть вероятность рождения ребенка с генетическими отклонениями можно диагностировать даже на ранних стадиях беременности с помощью пренатального скрининга. «Стандартные» процедуры предусматривают проведение биохимического анализа активных биологических веществ в крови матери, а также ультразвукового исследования, направленного на поиск специфических маркеров: отсутствие носовых костей, неправильная толщина воротничкового пространства, пороки сердца, аномалии ЦНС, укорочение костей и т.д.
Но точность таких исследований (<85%) вынуждает использовать иные методики подтверждения диагнозов: биопсия хориона (плодной оболочки), амниоцентез (забор околоплодных вод) хоть и дают более точный результат, но связаны с определенными рисками: от инфицирования организма матери, до непрерывного кровотечения или повышения вероятности внезапного прерывания беременности. При этом уровень погрешности может достигать 5%, давая ложноположительный или ложноотрицательный результат.
Благо, на смену «опасным» методикам диагностики приходят инновационные неинвазивные способы, появившиеся в результате многолетних исследований человеческого генома. Но прежде чем воспользоваться наработками ученых-генетиков стоит разобраться, что такое NIPT при беременности, какова достоверность теста и чем неинвазивный пренатальный тест превосходит все существующие на сегодняшний день виды скрининга.
Что представляет собой неинвазивный пренатальный тест для беременных?
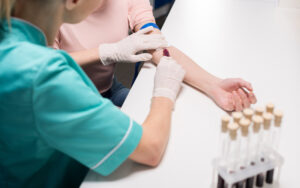
Суть процедуры схожа с биохимическим скринингом: в качестве образцов для проведения теста используется венозная кровь будущей матери. NIPT назначается в качестве дополнительной процедуры при комплексном скрининге за невозможностью или нежеланием пациентки проходить «стандартные» инвазивные процедуры. В сравнении с биопсией или забором околоплодных вод, исследование ДНК показывает высокую результативность при минимальной погрешности, не создавая осложнений для здоровья матери и не влияя на процесс развития плода.
NIPT позволяет установить:
- Трисомии 13, 18, 21 хромосом (синдромы Патау, Эдвардса, Дауна);
- Отсутствие X-хромосомы у девочек (болезнь Шерешевского-Тернера);
- Добавочные X и Y-хромосомы у мальчиков (патологии Клайнфельтера, Якобса);
- Делеции и микроделеции (отсутствие отдельных участков хромосом).
Кроме того, НИПТ позволяет определить пол ребенка на ранних (от 9-ой недели) стадиях беременности. В зависимости от теста, точность определения отклонения может достигать 99,9999%.
Доказано, что с 9 недели, в крови женщины, вынашивающей ребенка, появляются фрагменты клеток плода – фетальная ДНК. Современное материально-техническое оснащение позволяет выделять требуемые маркеры и сопоставлять их с наиболее распространенными генетическими сбоями и ошибками. Тем не менее, коллегия Американского конгресса акушеров и гинекологов выделяет «группу риска», для которых NIPT является обязательной процедурой.
К ним относятся:
- Женщины в возрасте старше 35 лет;
- Семьи, имеющие детей с хромосомными аномалиями;
- Матери, вынашивающие 2, 3 и 4 ребенка.
Точность теста зависит от правильного определения срока беременности, индивидуальных особенностей организма и скорости развития плода.
Могут ли результаты теста быть ошибочными?
Несмотря на высокую достоверность NIPT (в сравнении с другими методами дородовой диагностики хромосомных отклонений), метод не лишен недостатков. Для женщин, не входящих в группу риска, существует вероятность ошибки, дающей ложноположительный или ложноотрицательный результат, в особенности – при многоплодной беременности. В остальных случаях, показатель точности достигает 99%.
Инвазивный или неинвазивный тест — что лучше?
Из-за погрешности, свойственной инвазивным тестам, каждую двадцатую женщину в России отправляют на бессмысленные и, порой, опасные тесты, способные спровоцировать выкидыш. В случае с ложноположительными результатами, определить необходимость в назначении дополнительных исследований гораздо проще, чем с ложноотрицательными – «стандартные» тесты не различают каждую пятую хромосомную аномалию.
Именно поэтому, ученые рекомендуют использовать неинвазивные пренатальные тесты, обладающие рядом достоинств в сравнении с иными видами дородовой диагностики генетических отклонений в развитии плода.
К списку особенностей NIPT можно отнести:
- Абсолютную безопасность;
- Отсутствие болезненных ощущений;
- Оперативность выполнения теста;
- Возможность сдачи образцов с 8-10 недели беременности.
Забор венозной крови длиться менее минуты. Исследование маркеров, выделенных из образцов, занимает не более 12 рабочих дней. Более того, неинвазивная пренатальная ДНК-диагностика не имеет противопоказаний и не требует особой подготовки к сдаче биоматериала.
Но учитывая, что исследование направлено на выявление хромосомных аномалий плода и носит информативный характер, в случае выявления нарушений, для исключения или подтверждения вероятности развития патологий, будущей матери придется пройти инвазивную диагностику.
Располагая всем, что необходимо для проведения неинвазивной пренатальной диагностики и обработки образцов, полученных методом биопсии, лаборатория «INLABgenetics» готова поручиться за точность и достоверность результатов исследований.
Кроме того, мы гарантируем:
- Первоклассный сервис;
- Бесплатные консультации;
- Быстрое выполнение тестов;
- Адекватные, доступные цены;
- Комфортные условия оплаты.
Менеджеры центра генетических исследований готовы ответить на любой интересующий вас вопрос: для этого достаточно воспользоваться формой «обратной связи», позвонить по номеру «Горячей линии», оставить запрос на e-mail или посетить нашу лабораторию!
NIPT — не является медицинским прибором, инструментом, аппаратурой для анализов, медицинской услугой, аппаратом для диагностических целей и медицинских анализов, терапевтической услугой, консультацией по вопросам фармацевтики и медицинской помощью.
В самом начале должны открыть правду — в медицине НИЧЕГО не бывает на 100%. Априори ни один метод диагностики и скрининга патологий плода не превышает точность 99.9999% Потому что медицина, генетика, биология, биоинформатика и прочие науки постоянно развиваются, всегда появляются новые теории и методы, что оставляет ученым всегда право на ошибку. В структуре хромосомной патологии человека 45% случаев относятся к анеуплоидиям половых хромосом, а 25% приходится на группу аутосомных трисомий, самыми частыми из которых являются трисомии по хромосомам 21, 18, 13 [1].
Клиническая картина хромосомных патологий:
- врожденные пороки развития,
- малые аномальные развития,
- умственная отсталость;
- неврологическая,
- психиатрическая,
- гематологическая патология,
- нарушения слуха,
- зрения.
Хромосомные аномалии одна из самых актуальных проблем здравоохранения, по данным ВОЗ:
- 0,8% всех новорождённых,
- 40% новорожденных с множественными пороками развития,
- 15% детей с умственной отсталостью,
- 7% случаев мертворождений,
- ХА причина 70% случаев инвалидности у детей,
- нет лечения социальная дезадаптация
По состоянию на 2021 год в России применяется несколько методов определения генетических патологий плода:
Ранний пренатальный скрининг
Инвазивная диагностика
Неинвазивное пренатальное тестирование
Ранний пренатальный скрининг
Или по другому комбинированный скрининг I триместра. В России широкое применение РПС по международному стандарту было инициировано Минздравсоцразвития России только в 2009 г. с поэтапным внедрением нового алгоритма диагностики хромосомных патологий плода в субъектах страны в период с 2010 по 2014 [1].
Данный вид диагностики был разработан фондом медицины плода (FMF) и подразумевает под собой проведение ультразвукового исследования и анализа сывороточных маркеров материнской крови (бетта-ХГЧ и PAPP-A). Расчет риска, с учетом индивидуальных особенностей беременной (возраст матери и срок беременности) происходит с помощью унифицированной программы “Astraia” (Астрайя).
Каждая беременная женщина, которая встает на учет знает, что данный вид скрининга предстоит ей в период с 11 до 14 недель. По результатам скрининга женщина может получить как низкий риск рождения ребенка с патологией, так и высокий (граница 1:100).
Какова же точность скрининга I триместра, который проводят каждой беременной женщине в России:
![Данные: Анализ результатов раннего пренатального скрининга в Российской Федерации АУДИТ – 2019. Информационно-справочные материалы. Письмо МЗРФ № 15-4/2963-07 от 11.10.2019 [2]](https://msk.medicalgenomics.ru/assets/components/directresize/cache/dr_unnamed%20(2)_w400_h266.png)
Стоит отметить что 20% детей рожденных с синдромом Дауна (с трисомией 21) были рождены в группе низкого риска. [3]
Также сравнительный анализ показал, что комбинированный скрининг эффективнее исследования только биохимических или ультразвуковых маркеров (87% вместо 71%) [4].
Инвазивная пренатальная диагностика
Данный вид диагностики включает в себя процедуру забора разного вида биоматериала (в зависимости от срока беременности) из полости матки с помощью пункции под контролем УЗИ. Среди беременных процедуру часто называют “прокол”, длительность процедуры (подготовки и самой пункции) от 5 до 7 минут.
У инвазивной пренатальной диагностики есть свои ограничения и риски осложнений [5]:
- Самопроизвольное прерывание беременности (выкидыш): после амниоцентеза — 0,81%; после биопсии ворсин хориона – 2,18%
- Внутриутробное инфицирование 0,001%
- У носителей хронических вирусных гепатитов, ВИЧ-инфекции, при острых инфекционных процессах – риск высокий.
- Наличие абсолютных противопоказаний к процедуре: истмико-цервикальная недостаточность, угроза прерывания (наличие кровотечения)
- Избыток подкожно-жировой клетчатки, возможные технические трудности при проведении процедуры
- Беременной с резус-отрицательным фактором необходим контроль уровня антител перед процедурой, при их отсутствии — введение антирезусного иммуноглобулина после процедуры.
По данным FMF риски < 1% — 1: 100 Т.е. у каждой 100 женщины, после процедуры случился выкидыш.
Несмотря на ограничения, противопоказания и возможные риски инвазивная пренатальная диагностика является признанным методом в России. В случае выявления высокого риска хромосомных аномалий, пациентке рекомендуется проведение инвазивного обследования (плацентоцентез, амниоцентез, кордоцентез) [6].
Точность инвазивной диагностики свыше 99%.
Однако есть ограничение метода, связанное с редким явлением плацентарного мозаицизма: в 1-2% биопсии ворсин хориона (плацентозентезе) [5]. Это два или более клона клеток с разным хромосомным набором. Может быть ложный результат диагностики или выявление мозаицизма. При этом мозаицизм у плода выявляется в 30-40% случаев.
При амниоцентезе может быть ложный результат в случае тканевого мозаицизма у плода. В амниотической жидкости представлены не все клеточные линии плода: только клетки кожи, ЖКТ, мочевого пузыря и легких.
Неинвазивная пренатальная диагностика
Неинвазивный пренатальный тест (НИПТ) — это скрининговый метод. Сегодня в России проводят около 30-40 тысяч НИПТ в год, всего НИПТ сделали от 4 до 6 млн женщин (по состоянию на 2017 год) [1].
Само исследование представляет собой технологически сложный и затратный по времени процесс, включающий такие этапы как:
- взятие образца крови у пациента и получение плазмы,
- выделение ДНК и пробоподготовка,
- секвенирование,
- биоинформатические анализ,
- подготовка заключения.
Точность НИПТ
Во всех метаанализах сделан вывод, что НИПТ с помощью анализа внеклеточной ДНК плода в материнской плазме является высокоэффективным методом скрининга частых хромосомных аномалий — трисомии 21,18 и 13 [8-11] как при одноплодной беременности, так и для близнецов.
В связи с низким процентом ложноположительных результатов специфичность НИПТ в подавляющем большинстве публикаций была высокой и колебалась в пределах 98-99,9%.
Авторы исследований отмечают, что скрининг на трисомию 21 (синдром Дауна) с помощью анализа фетальной внеклеточной ДНК в материнской крови превосходит все другие традиционные методы скрининга с более высокой чувствительностью и более низким процентом ложноположительных результатов [8].
Доля ложноположительных результатов исследований по пяти хромосомам оценивается от 0,1 до 0,9% [7].
У данного метода тоже есть ограничения и противопоказания:
- Синдром исчезающего близнеца
- Хромосомные аномалии или хромосомный мозаицизм у матери
- Не проводится ранее 10-ти недель беременности
- Для беременностей двойней не проводится тест на анеуплоидии половых хромосом
- Не проводится для беременности тройней и большим количеством плодов
- Не предназначен и клинически не подтвержден для определения мозаицизма, частичной трисомии или транслокаций, а также для выявления хромосомной патологии по незаявленным хромосомам
- Опухоли у женщины на данный момент или в прошлом, трансплантация органов или костного мозга, стволовых клеток в прошлом (в этих случаях повышен риск ложного результата тест).
Получить консультацию специалиста
Хотите пройти тест НИПТ?
Оставьте заявку, мы постараемся вам помочь!
Список литературы:
- Современное значение неинвазивного пренатального исследования внеклеточной ДНК плода в крови матери и перспективы его применения в системе массового скрининга беременных в Российской Федерации © Е.А. Калашникова, А.С. Глотов , Е.Н. Андреева, И.Ю. Барков , Г.Ю. Бобровник, Е.В. Дубровина, Л.А. Жученко
- Анализ результатов раннего пренатального скрининга в Российской Федерации АУДИТ – 2019. Информационно-справочные материалы. Письмо МЗРФ № 15-4/2963-07 от 11.10.2019
- Жученко, Л. А., Голошубов, П. А., Андреева, Е. Н., Калашникова, Е. А., Юдина, Е. В., Ижевская, В. Л. (2014). Анализ результатов раннего пренатального скрининга, выполняющегося по национальному приоритетному проекту «Здоровье» в субъектах Российской Федерации. Результаты российского мультицентрового исследования «Аудит-2014». Медицинская генетика, 13(6), 3-54.
- S Kate Alldred, Yemisi Takwoingi, Boliang Guo, Mary Pennant, Jonathan J Deeks, James P Neilson, Zarko Alfirevic First trimester ultrasound tests alone or in combination with first trimester serum tests for Down’s syndrome screening
- Queenan, J. T. et al. (2010). Protocols for high-risk pregnancies: an evidence-based approach. John Wiley & Sons. – 661 p. R. AKOLEKAR, J. BETA, G. PICCIARELLI, C. OGILVIE and F. D’ANTONIO. Procedure-related risk of miscarriage following amniocentesisand chorionic villus sampling: a systematic review and meta-analysis. Ultrasound Obstet Gynecol 2015; 45: 16–26.
- Приказ Минздрава России от 20.10.2020 N 1130н «Об утверждении Порядка оказания медицинской помощи по профилю «акушерство и гинекология» (Зарегистрировано в Минюсте России 12.11.2020 N 60869)
- Lui X. Mils. «Financing reforms of public health services in China: Lessons for other nations». Social Science and Medicine, 2002; 54:1691-1698. «Non-invasive prenatal testing for fetal aneuploidy: charting the course from clin- ical validity to clinical utility». Ultrasound Obstet Gynecol 2013; 41: 2-6.
- Gil MM, Quezada MS, Revello R, et al. Analysis of cell-free DNA in maternal blood in screening for fetal aneuploidies: updated meta-analysis. Ultrasound Obstet Gynecol. 2015;45:249–266. doi: 10.1002/uog.14791
- Gil MM, Accurti V, Santacruz B, et al. Analysis of cell-free DNA in maternal blood in screening for aneuploidies: updated meta-analysis. Ultrasound Obstet Gynecol. 2017;50:302–314. doi: 10.1002/uog.17484
- Mackie FL, Hemming K, Allen S, et al. The accuracy of cellfree fetal DNA-based non-invasive prenatal testing in singleton pregnancies: a systematic review and bivariate meta-analysis. BJOG. 2017;124:32–46. doi: 10.1111/1471-0528.14050
- Taylor-Phillips S, Freeman K, Geppert J, et al. Accuracy of non-invasive prenatal testing using cell-free DNA for detection of Down, Edwards and Patau syndromes: a systematic review and meta-analysis. BMJ Open. 2016;6(1):e010002. doi: 10.1136/bmjopen-2015-010002
ПРАКТИКА
Что такое НИПТ и почему
о нем все говорят?
Генетики отвечают на самые важные вопросы о неинвазивном пренатальном тесте (НИПТ): почему его делают всем на Западе, а в России до сих пор предпочитают биохимический скрининг, правда ли, что эффективность теста — 99% или это маркетинговый ход, и почему врачи все еще практикуют «проколы пузыря»: амниоцентез, кордонцентез и биопсию хориона.
В настоящий момент НИПТ — неинвазивный пренатальный тест — это самый удобный способ получить информацию о возможных хромосомных нарушениях у плода начиная с 10 недели беременности. Он безопасен для будущего ребенка: ДНК плода выделяется из венозной крови матери. Рассказываем, как это происходит технически и каких неприятностей позволяет избежать.
до 12 дней
выполняется анализ
10 неделя
срок, начиная с которого можно сдать тест
Зачем нужен НИПТ?
Сегодня это самый удобный и безопасный тест, который может пройти беременная женщина, чтобы выяснить, здоров ли ее будущий ребенок. Он позволяет избежать волнений и не поддаваться тревожным мыслям. НИПТ с 99% точностью выявляет трисомию 13, 18 и 21 хромосом на раннем сроке беременности. Для тестирования не обязательно иметь направление или справку от врача: НИПТ делается по желанию женщины.
Почему НИПТ безопасен для будущего ребенка?
Небольшое количество ДНК плода всегда присутствует в кровотоке, составляя от 5 до 15% всей свободно циркулирующей ДНК в крови матери. Поэтому для НИПТ процедура сдачи крови из вены матери такая же, как для обычного анализа. Благодаря использованию крови матери, проведение теста не может стать причиной самопроизвольного прерывания беременности, что является достаточно частым осложнением инвазивных методов (амниоцентеза или анализа ворсин хориона).
Чем НИПТ отличается от биохимического скрининга (двойного или тройного теста)?
Пренатальный скрининг (двойной или тройной тест) входит в комплекс процедур по ведению беременности и включен в ОМС. Его можно пройти бесплатно, прикрепившись к женской консультации при поликлинике по месту жительства. Анализы сдаются дважды: в 12-13 недель беременности и в 16. Первый скрининг исследует два биохимических маркера: ХГЧ и РАРР-А. Параллельно проводится УЗИ, на котором измеряется толщина воротникового пространства. На основе результатов этих исследований и информации о возрасте матери скрининг рассчитывает вероятные риски трисомии по 13, 18 и 21 хромосоме. Точность оценки риска по разным источникам составляет 70-80%.
НИПТ — это более точное исследование. Для того, чтобы его пройти, не нужно дожидаться 12 недели беременности: НИПТ информативен уже начиная с десятой. Проведение НИПТ включено в федеральные рекомендации по ведению беременности в России, однако этот тест не оплачивается из средств ОМС.
Врач-генетик
Отличия НИПТ от биохимического скрининга в том, что НИПТ — это прямой метод, мы четко определяем количество ДНК, а биохимический или ультразвуковой — это косвенные методы. Биохимический скрининг имеет точность около 70-80%, а НИПТ — 99% и даже более.
Синдромы Дауна, Эдвардса и Патау сопровождаются тяжелыми множественными пороками развития и не поддаются излечению.
Заменит ли НИПТ инвазивные методы диагностики хромосомных патологий?
НИПТ — информативный способ узнать, есть ли у плода хромосомные нарушения. Точность результата составляет более 99%, поэтому ему можно доверять. Только в случае выявления хромосомного нарушения у плода врач может настаивать на подтверждении результатов инвазивными методоми, которые считаются «золотым стандартом»: амниоцентезом или кордоцентезом. Такая процедура определена стандартами оказания медицинской помощи в России и других странах.
Какие еще синдромы и состояния может выявить НИПТ?
Помимо синдромов Дауна, Эдвардса и Патау, которые связаны с утроением хромосом, НИПТ может выявить аномалии половых хромосом (например, синдром Клайнфельтера) и наиболее частые микроделеции (они являются причиной, например, синдрома Ди Джорджи, Ангельмана, «кошачьего крика», Прадера — Вилли).
Врач-генетик
НИПТ рекомендуется делать всем женщинам, вне зависимости от возраста. После 35 лет риск синдрома Дауна возрастает. Но микроделеционные синдромы могут возникнуть у плода, когда матери 20, 30, 40 лет — здесь нет коррелляции с возрастом.
Как быстро делается НИПТ?
Сам забор крови обычно длится меньше минуты, а исследование полученного биоматериала проводится в течение 12 рабочих дней. После этого можно получить результаты и консультацию генетика.
Есть ли у этого исследования противопоказания?
Проведение НИПТ не имеет противопоказаний. До и после теста беременной женщине может быть полезна консультация врача-генетика, который сможет пояснить возможность, ограничения и результаты теста. Точность НИПТ может быть снижена, если женщина перенесла лечение стволовыми клетками, пересадку костного мозга или беременность многоплодная.
О чем еще расскажет НИПТ?
Тест не сможет дать информацию о внешности, характере или талантах будущего ребенка, но у него есть приятный бонус — пол можно узнать сразу, не дожидаясь визуализации первичных признаков на УЗИ.
В процессе выполнения анализа мы определим пол будущего ребенка и сообщим его вам по вашему желанию.
Возможно, вы только что узнали о своей беременности. Врач говорит, что скоро нужно будет пройти какой-то скрининг, а еще давным-давно вы читали статью о том, что на свете есть особые дети, и вот именно сейчас в сердце закралась тревога.
А может быть, вы уже сделали скрининг, и врач говорит, что у малыша, скорее всего, синдром Дауна. Что делать дальше? Какие еще исследования пройти?
Или же вы только планируете беременность и вас растревожили сообщениями о том, что есть такая «болезнь» – синдром Дауна. Поневоле возникают мысли: вдруг и у нас будет такой малыш?
Кто бы вы ни были, эта статья – для вас. Надеемся, она поможет вам сориентироваться в вопросах пренатальной диагностики и даст понимание, куда двигаться дальше.
Что такое пренатальная диагностика?
Во время беременности каждой женщине предлагают пройти комплексную диагностику. С ее помощью можно определить, могут ли у будущего малыша быть проблемы со здоровьем или генетические отклонения, в том числе синдром Дауна. Эти исследования дают информацию, которая помогает семье принять взвешенное решение о судьбе своего будущего ребенка.
Очень важно вовремя встать на учет по беременности, для того чтобы не пропустить важные исследования, так как все они проводятся на определенных сроках беременности.
Выделяют два типа пренатальной диагностики: скрининговую и подтверждающую. Само слово «скрининг» переводится как «просеивание», потому что это массовое исследование – все беременные женщины могут пройти его бесплатно, в рамках финансирования ОМС.
Скрининговые тесты помогают определить группу будущих мам, у которых есть высокая вероятность развития хромосомных отклонений у плода, – в этом случае назначаются дополнительные подтверждающие исследования.
Одновременно с этим анализы выявляют те беременности, для которых повышенной угрозы нет. В этом случае их результаты отрицательные, и необходимости в дополнительных исследованиях (кроме скринингов, проводимых 1 раз в триместр) – нет.
Первый скрининг при беременности проводят между 11 и 13 неделями. Исследование включает в себя УЗИ и анализ крови.
Второй скрининг при беременности проводят на сроке 18–20 недель. В него включены те же два этапа – УЗИ и анализ крови, однако последний сдается только в том случае, если женщина не делала первый скрининг.
Третий скрининг при беременности проводят на 30–34 неделе. Основа третьего скрининга – УЗИ, основная цель которого – определить стратегию родов.
По результатам скринингов в случае необходимости могут назначаться дополнительные исследования.
Как понять, возможен ли у будущего ребенка синдром Дауна?
Есть несколько методов пренатальной диагностики, которые могут дать ответ, родится малыш с синдромом Дауна или нет. Они бывают неинвазивными и инвазивными. Анализ крови и УЗИ – это неинвазивные методы, т.к. их проведение не требует особого вмешательства в организм матери. Никакого риска для будущего ребенка они не несут. Но их результатам далеко не всегда можно доверять. Если вам по результатам УЗИ сказали, что у малыша возможен синдром Дауна, – не воспринимайте это как окончательный диагноз. Это лишь сигнал, что желательно провести дополнительные инвазивные исследования. Их смысл – получить для исследования клетки самого плода. Врачи-генетики, рассматривая эти клетки в микроскоп, смогут увидеть в них лишнюю хромосому и тогда уже поставить точный диагноз – есть ли у будущего малыша синдром Дауна или нет.
Как получить клетки эмбриона? Они есть в околоплодных водах. Чтобы их исследовать, нужно сделать прокол оболочки околоплодного пузыря. Такая медицинская процедура, к сожалению, бывает довольно дискомфортна для мамы, а кроме того, она может быть опасной и для малыша, ведь в результате ее проведения возрастает вероятность выкидыша.
Дальше мы подробнее ответим на вопросы о каждом методе пренатальной диагностики.
Первый скрининг предлагают пройти в первом триместре, в период с 11 до 13 недель и 6 дней беременности. У будущей мамы берут кровь для анализа (измеряют уровень определенных биологических маркеров) и делают УЗИ (оценивают анатомию плода). В результате врач может понять, есть ли у плода риск каких-то болезней и отклонений, в том числе синдрома Дауна. Обратите внимание: результат первого скрининга – это только оценка рисков, а ни в коем случае не окончательный диагноз! Это лишь первое предположение, что, возможно, что-то может пойти не так. По статистике, ребенок с синдромом Дауна появляется лишь в одном из 150 случаев «беременности высокого риска».
Что оценивает врач в процессе первого скрининга, чтобы не пропустить синдром Дауна?
Врач во время УЗИ визуально оценивает некоторые показатели: в первую очередь, есть ли у плода увеличенная воротниковая зона и гипоплазия (укороченность, недоразвитие) носовой кости. Подробнее про определение толщины воротникового пространства вы можете прочитать по ссылке. Если коротко, то на задней поверхности шеи любого малыша есть скопление подкожной жидкости, но у многих детей с синдромом Дауна ее количество сильно увеличено. Понятно, что этот показатель не может говорить о точном диагнозе «синдром Дауна», – он лишь помогает определить, нужно ли назначить более глубокие исследования. Что касается гипоплазии носовой кости (уменьшение размеров косточки носа), то этот показатель тоже выступает лишь сигналом о возможных проблемах.
Кроме УЗИ плода, скрининг включает в себя и анализ крови матери. Врач обращает внимание на значения белков материнской сыворотки. При этом он также учитывает такие факторы, как возраст матери (чем она старше, тем риск больше) и историю беременностей (если таковые уже были). Результаты УЗИ и анализа крови врач анализирует комплексно – так результаты будут точнее.
Если первый скрининг показал, что повышен риск рождения ребенка с синдромом Дауна, – что делать дальше?
Может оказаться, что беременная женщина по результатам скрининга попадает в так называемую группу риска. Это сигнал, что желательно провести дальнейшие исследования, чтобы точно установить диагноз. На данном этапе важно, какую позицию занимает консультирующий врач. Именно он должен объяснить женщине и ее семье ситуацию и риски, правильно сориентировать и помочь выбрать тактику дальнейших действий. Кто-то из беременных этой группы предпочитает оставить всё как есть, не проводить дополнительных исследований и ожидать рождения малыша, а кто-то соглашается на инвазивную процедуру.
Что такое инвазивная процедура? Это опасно?
Инвазивная процедура – это метод, позволяющий с высокой степенью точности ответить на вопрос: есть у малыша синдром Дауна или нет. Инвазивные тесты позволяют практически в 99 % случаев выявить хромосомные аномалии у плода.
Существует несколько инвазивных процедур, из которых самые распространенные – биопсия ворсин хориона и амниоцентез. Подробно о каждом из них вы можете прочитать по ссылкам ниже, а здесь мы обозначим их сущность вкратце.
Для проведения амниоцентеза
из матки женщины берется для исследования образец околоплодной жидкости. Зачем это делается? Дело в том, что в этой жидкости находятся клетки эмбриона, т.е. врач через микроскоп видит клетки будущего ребенка и может определить, есть ли в них дополнительная хромосома, которая говорит о наличии синдрома Дауна.
Биопсия ворсин хориона (БВХ) – это анализ эмбриональной ткани (хориона). Процедура похожа на амниоцентез и тоже предполагает прокол стенки матки. В отличие от амниоцентеза, биопсию хориона проводят несколько раньше по срокам.
Решение о том, делать ли инвазивные исследования, могут принять только сами будущие родители, т.к. эти процедуры сопровождаются риском выкидыша.
Что такое «тест на синдром Дауна по крови»?
Так иногда называют новый метод неинвазивного пренатального тестирования (НИПТ). Это анализ крови матери, но не тот, который делают при обычном скрининге. Дело в том, что в конце XX века ученые обнаружили, что в крови беременной женщины обязательно есть фрагменты ДНК ее будущего ребенка – так называемая внеклеточная ДНК. Суть НИПТа проста – эта внеклеточная ДНК выделяется из крови матери и затем «читается» с помощью сложных компьютерных программ. Этот метод тестирования сейчас активно развивается, и у него очень высокая точность – до 99 % и даже более.
Если этот анализ дает такой точный результат, почему его не делают всем?
Основная причина в том, что НИПТ – довольно дорогостоящий анализ. Кроме того, одни лаборатории имеют необходимое для него оборудование (сложное и очень дорогостоящее), а другие выступают как посредники, которые отсылают биоматериал для проведения анализа за границу.
К тому же НИПТ является скрининговым методом, и в случае выявления высокого риска хромосомной патологии у плода всё равно потребуется проведение уточняющей инвазивной диагностики.
Если я сделаю НИПТ, какие возможны варианты действий дальше?
Ситуации возможны разные.
Если у женщины отрицательный результат по НИПТ, это говорит о низких рисках с вероятностью до 97 %, но не исключает синдром Дауна полностью. Поскольку НИПТ – это неинвазивный тест (для него не используют ни биопсию ворсин хориона, ни амниоцентез), то, несмотря на статистическую точность, следует иметь в виду, что это всё-таки расчетные, а не объективные данные.
Если по предыдущим неинвазивным скринингам риск наличия синдрома Дауна выше, чем 1:100, НИПТ не показан, поскольку в этом случае также не стоит надеяться на расчетные данные. Велика вероятность ошибки: возможны не только ложноотрицательные, но и ложноположительные результаты, что повлечет за собой опасность избавиться от здорового плода.
Еще одна сложность при использовании НИПТ заключается в следующем: если тест проводился после 12 недель беременности и показывает положительный результат – это не будет считаться основанием для перывания беременности. В таком случае для принятия решения всё-таки придется сделать инвазивный тест.
С другой стороны, результаты НИПТ достаточно точные, и в тех случаях, когда предыдущие неинвазивные тесты показывают риск ниже, чем 1:100, женщина для собственного спокойствия может пройти это исследование.
Можно ли отказаться от всех скринингов и исследований?
Да, можно. Будущей маме лишь рекомендуется сделать скрининг – обязанности у нее нет. Врач не может заставить вас делать те или иные тесты и анализы.
Зачем мне заранее знать, будет ли у моего ребенка синдром Дауна или нет?
Все решения, которые касаются судьбы будущего ребенка, принимают исключительно его родители. Ни ваш гинеколог, ни генетик, ни родственники – никто не имеет права склонять вас к тому или иному решению. Но при этом семье очень важно владеть достоверной информацией. Зная, что у будущего малыша, вероятнее всего, синдром Дауна, родители могут поступить по-разному. Кто-то принимает решение о прерывании беременности. Кто-то старается узнать побольше о синдроме, чтобы подготовиться к рождению особого малыша и сразу оказать ему необходимую помощь – и медицинскую, если это нужно, и педагогическую. Кто-то ищет и находит семьи, в которых растут дети с синдромом Дауна, знакомится с ними, общается, заранее занимается поиском профильных организаций и получает там полезную информацию и поддержку. В таком случае рождение особого ребенка не становится для семьи неожиданным ударом, а остается запланированным и таким же долгожданным событием, как рождение любого ребенка, – просто уже с учетом его особенности. Знание о диагнозе малыша помогает будущим родителям перестать жить в пассивной тревоге и отчаянии: ведь когда ты знаешь, чего ожидать, ты можешь начать действовать.
У кого больше всего вероятность родить ребенка с синдромом Дауна?
Ребенок с синдромом Дауна может появиться в любой семье. В данном случае не имеют значения ни социальное положение родителей, ни их состояние здоровья, ни экономическое благополучие, ни национальность, ни место проживания, ни что-либо другое. Единственное, что считается фактором риска для рождения ребенка с синдромом Дауна, – это возраст матери. Чем старше женщина, тем выше вероятность, что у нее может появиться ребенок с синдромом Дауна. Поэтому женщинам старше 35 лет настоятельно рекомендуется проходить пренатальную диагностику. Впрочем, не стоит забывать о том, что дети с синдромом Дауна рождаются у женщин любого возраста.
Можно ли еще до наступления беременности узнать, есть ли вероятность генетических нарушений у будущего ребенка?
В подавляющем большинстве случаев синдром Дауна – это генетическая случайность, но бывают случаи сбалансированной хромосомной перестройки (транслокация, инверсия) или мозаичный кариотип (наличие клеточного клона с аномальным числом хромосом) у кого-либо из родителей. Их поможет обнаружить генетическое исследование
Врач предлагает мне сделать аборт, потому что у малыша синдром Дауна. Он прав?
Еще раз подчеркнем, что решение о судьбе будущего ребенка могут принимать только его родители. Никто не имеет права склонять вас к прерыванию беременности. Единственная задача специалистов, будь то гинеколог, генетик, психолог и т.д., – дать вам достоверную информацию: рассказать обо всех возможных трудностях и радостях жизни с особым ребенком и показать возможные пути действий – ведь у родителей всегда есть возможность выбора. К сожалению, до сих пор многие врачи не могут избежать оценочных высказываний; в ряде случаев они могут навязывать будущим родителям свою точку зрения, рассказывая о жизни с ребенком с синдромом Дауна только с негативной стороны. Знайте, что такие врачи нарушают этические нормы своей профессии! В целом ряде российских регионов существуют официальные протоколы сообщения диагноза ребенка будущим родителям, которые запрещают врачам склонять семью к проведению аборта и оказывать психологическое давление. Если врач убеждает вас сделать аборт, а вы этому сопротивляетесь, – смело меняйте врача!
Мы надеемся, что эта краткая информация в форме ответов на самые частые вопросы, которые задают родители, поможет вам разобраться в тех тестах, которые вы уже прошли или только собираетесь пройти.
ГБУЗ Москвы «Городская клиническая больница №24 Департамента здравоохранения Москвы»
Баранова Е.Е.
ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России;
ООО «Эвоген»
Сагайдак О.В.
ООО «Эвоген»
Кузнецова Е.С.
ООО «Эвоген»
Галактионова А.М.
ООО «Эвоген»
Капланова М.Т.
ООО «Эвоген»
Беленикин М.С.
ООО «Эвоген»
Зобкова Г.Ю.
ООО «Эвоген»
Гнетецкая В.А.
ООО «Эвоген»;
ООО «Мать и дитя»
Макарова М.В.
ООО «Эвоген»
Сонголова Е.Н.
ГБУЗ Москвы «Городская клиническая больница №67 им. Л.А. Ворохобова Департамента здравоохранения Москвы»
Результаты пренатального скрининга на трисомии по 21-й, 18-й и 13-й хромосомам с использованием неинвазивного пренатального тестирования в г. Москве
Авторы:
Оленев А.С., Баранова Е.Е., Сагайдак О.В., Кузнецова Е.С., Галактионова А.М., Капланова М.Т., Беленикин М.С., Зобкова Г.Ю., Гнетецкая В.А., Косова Е.В., Макарова М.В., Сонголова Е.Н.
Журнал:
Проблемы репродукции. 2021;27(1): 114‑123
Как цитировать:
Оленев А.С., Баранова Е.Е., Сагайдак О.В., Кузнецова Е.С., Галактионова А.М., Капланова М.Т., Беленикин М.С., Зобкова Г.Ю., Гнетецкая В.А., Косова Е.В., Макарова М.В., Сонголова Е.Н.
Результаты пренатального скрининга на трисомии по 21-й, 18-й и 13-й хромосомам с использованием неинвазивного пренатального тестирования в г. Москве. Проблемы репродукции.
2021;27(1):114‑123.
Olenev AS, Baranova EE, Sagaydak OV, Kuznetsova ES, Galaktionova AM, Kaplanova MT, Belenikin MS, Zobkova GY, Gnetetskaya VA, Kosova EV, Makarova MV, Songolova EN. First results of non-invasive prenatal testing adoption in Moscow. Russian Journal of Human Reproduction. 2021;27(1):114‑123. (In Russ.).
https://doi.org/10.17116/repro202127011114

?>
Во всем мире прилагаются большие усилия для снижения детской смертности. В России смертность от хромосомных аномалий и врожденных заболеваний достигает 20—23% в структуре младенческой смертности [1]. Частота выявления хромосомной патологии в популяции — 1:300—1:250 [2], чаще всего встречаются трисомии по 21-й, 18-й и 13-й хромосомам. Одним из ключевых инструментов снижения младенческой и перинатальной смертности является пренатальный скрининг, направленный на выявление и оценку рисков хромосомных аномалий плода.
В настоящее время пренатальный скрининг первого триместра включает ультразвуковое исследование (УЗИ) в сроке 11—14 недель беременности с определением материнских сывороточных маркеров крови, на основании которого производится комплексный программный расчет индивидуального риска рождения ребенка с хромосомной патологией [3]. Расчет индивидуального риска рождения ребенка с хромосомной патологией, проведенный на основании данных ультразвукового исследования и показателей материнских сывороточных маркеров, является непрямым методом, в связи с чем может приводить к получению значительного количества ложноположительных и ложноотрицательных результатов.
Развитие молекулярных технологий во всем мире предоставляет возможность пересмотра существующей системы пренатального обследования беременных женщин. Известно, что в крови беременной женщины циркулирует внеклеточная ДНК хориона (вкДНК), по которой можно оценить весь хромосомный набор плода. Анализ вкДНК по крови беременной получил название неинвазивный пренатальный тест (НИПТ) и с 2011 г. стал применяться во всем мире [4]. НИПТ показывает высокую точность для наиболее распространенных трисомий: по 21-й, 18-й и 13-й хромосомам, а также используется для выявления аномалий других аутосом и половых хромосом.
Изначально Американская коллегия акушеров-гинекологов (ACOG) предлагала использовать НИПТ только для обследования женщин с высоким риском хромосомной патологии. Вместе с тем показана эффективность НИПТ также в группах женщин среднего и низкого риска. В связи с этим на сегодняшний день современные международные рекомендации предлагают проведение НИПТ всем беременным женщинам [5].
Существует два наиболее распространенных сценария внедрения НИПТ в структуру пренатального скрининга: первый — в качестве теста первой линии, когда НИПТ назначается всем беременным женщинам до проведения экспертного УЗИ в первом триместре беременности, второй — в качестве теста второй линии, когда НИПТ проводится женщинам в группах высокого или среднего риска, определенного по результатам комбинированного пренатального скрининга [6]. Ряд европейских стран внедряют НИПТ в качестве теста первой линии вместо стандартного пренатального скрининга первого триместра. В Нидерландах и Бельгии провели общенациональные клинические исследования перед внедрением теста. Результаты исследований демонстрируют основные преимущества НИПТ: увеличение выявляемости наиболее частых анеуплоидий (до 99%), уменьшение доли ложноположительных результатов (до 0,08%), а также уменьшение доли женщин, которым требуется проведение инвазивной пренатальной диагностики (ИПД) [7]. Для проведения НИПТ необходим стандартный забор венозной крови женщины — неинвазивная, относительно безболезненная и безопасная процедура. Проведение НИПТ не несет риска для течения беременности.
Большинство стран, включившие НИПТ в государственные программы пренатального скрининга, используют его в качестве теста второй линии из-за высоких экономических затрат. Этот сценарий внедрения приводит к снижению частоты ложноположительных результатов и снижению частоты инвазивных процедур. Если НИПТ в качестве теста второй линии охватывает группы беременных женщин высокого риска и группы с более низким риском, это также помогает увеличить частоту выявления частых анеуплоидий. Подобный сценарий выбран и в Москве.
До недавнего времени в России НИПТ оставался преимущественно дополнительным исследованием по индивидуальному желанию и на коммерческой основе. С 13 марта 2020 г. в Российской Федерации НИПТ включен в структуру пренатальной диагностики в Москве в рамках пилотного проекта согласно приказу Департамента здравоохранения Москвы от 13.03.20 №199 «Об организации проведения неинвазивного пренатального теста в Москве» (№199 ДЗМ) [8], что является важным этапом в разработке руководств и практических рекомендаций по внедрению теста на территории этого субъекта Российской Федерации. На сегодняшний день доступны результаты внедрения НИПТ в течение 6 мес.
Цель исследования — проанализировать результаты пренатального скрининга с применением неинвазивного пренатального тестирования (НИПТ) в Москве за период с 01.04.20 по 30.09.20. Оценить преимущество использования НИПТ перед комбинированным пренатальным скринингом в первом триместре беременности.
Материал и методы
Согласно приказу №199 ДЗМ, всем беременным жительницам Москвы с риском хромосомной патологии 1:101—1:2500 по результатам пренатального скрининга первого триместра предлагается дополнительно пройти НИПТ [8]. Это исследование также выполняется пациенткам группы высокого риска (1:100 и выше), согласившимся на проведение инвазивной диагностики. Взятие крови на НИПТ обычно осуществляется в день проведения ИПД. НИПТ проводится пациенткам и по решению городского пренатального консилиума при наличии показаний независимо от показателя индивидуального риска, по результатам скрининга первого триместра. При получении данных о наличии высокого риска хромосомной патологии по результату НИПТ беременные женщины направляются на консультацию к врачу-генетику для решения вопроса о проведении ИПД (рис. 1). В период с 01.04.2020 по 30.09.2020 проанализированы образцы крови беременных женщин (n=5181).

Рис. 1. Схематическое изображение алгоритма обследования пациенток в первом триместре беременности с учетом приказа №199 ДЗМ.
* — ИПД (инвазивная пренатальная диагностика) обязательна для беременных из группы высокого риска и является дополнительной для группы промежуточного риска. НИПТ — неинвазивное пренатальное тестирование.
Для проведения исследования забор крови осуществлялся в специализированные пробирки типа STRECK, обеспечивающие сохранность вкДНК, объемом 10 мл, с нанесенными на них идентификационными номерами пациентов. Транспортировку образцов и хранение пробирок до обработки проводили при температуре (6—37 °C). Процедура выполнения теста разделена на несколько последовательных этапов: отделение плазмы крови (все манипуляции с пробирками, количество и скорость откручивания проводили в соответствии с протоколом производителя пробирок) и выделение вкДНК; создание библиотек для секвенирования; секвенирование библиотек ДНК и анализ полученных данных. После центрифугирования бесклеточную плазму крови хранили при температуре –80 °C. Оценку распределения по размерам библиотек проводили с помощью Qiagen QIAxcel. Все экспериментальные этапы подготовки к секвенированию проводили в соответствии с оригинальным протоколом BGI NIFTY, для одноконцевого секвенирования (SE50) использовали валидированную для проведения исследований платформу BGISEQ-500 (BGI Group, Китай). Для обсчета результатов секвенирования использовали оригинальное программное обеспечение BGI HALOS NIFTY 2.3.2.1011 (BGI). В отчет включены риски по наиболее частым трисомиям (хромосом 21-й, 18-й и 13-й).
Для подтверждения положительных результатов НИПТ (с высоким риском хромосомных аномалий плода) женщинам рекомендовано медико-генетическое консультирование и направление на ИПД (преимущественно амниоцентез). Последующий генетический анализ материала плода осуществляли с помощью цитогенетического исследования, в некоторых случаях дополнительно проводилось молекулярно-генетическое исследование на чипах.
Перед забором крови все участницы исследования подписали добровольное информированное согласие.
Статистический анализ
Описательные данные представлены в виде медианы и межквартильного размаха для непрерывных переменных и в процентах для категориальных переменных. Сравнение между группами проводилось с использованием U-критерия Манна—Уитни для непрерывных переменных, а для категориальных переменных — критерия хи-квадрат (χ2) или точного критерия Фишера. Значения p≤0,05 считались статистически значимыми. Расчеты проводились с использованием пакета для статистической обработки Wizard Ver.1.9.47(275).
Результаты
За период с 01.04.20 по 30.09.20 проанализированы образцы крови беременных женщин (n=5181) — жительниц Москвы. Средний возраст всех пациенток, которые прошли НИПТ, составил — 34,4±4,3 года. В 2746 (53,0%) из 5181 случаев возраст беременных женщин составил 35 лет и старше. Средний индекс массы тела (ИМТ) обследуемых женщин — 24,6 кг/м2, в 1907 (36,8%) из 5181 случаев ИМТ составил 25 кг/м2 и более. Большинство беременностей были спонтанными и одноплодными (табл. 1). На основании комбинированного пренатального скрининга беременные женщины разделены на группы риска: в группе высокого риска (1:100 и выше) оказалось 208 пациенток, в группе риска 1:101—1:2500 — 4973 пациентки.
Таблица 1. Характеристика беременных женщин, прошедших неинвазивное пренатальное тестирование, и типы беременности
|
Параметр |
Количество женщин, n (%) |
|
Возраст, лет: |
|
|
Моложе 20 |
37 (0,7) |
|
20—24 |
203 (3,9) |
|
25—29 |
684 (13,2) |
|
30—34 |
1511 (29,2) |
|
35—39 |
1915 (37,0) |
|
40 и старше |
831 (16,0) |
|
Индекс массы тела, кг/м2: |
|
|
<18,5 |
260 (5,0) |
|
18,5—24,9 |
3015 (58,2) |
|
25—30 |
1200 (23,2) |
|
>30 |
706 (13,6) |
|
Тип беременности: |
|
|
Одноплодная |
5106 (98,6) |
|
Двуплодная |
64 (1,2) |
|
Исчезающий близнец |
11 (0,2) |
|
Тип оплодотворения: |
|
|
Самопроизвольный |
5016 (96,8) |
|
Экстракорпоральный |
165 (3,2) |
|
Результаты пренатального скрининга: |
|
|
Группа высокого риска (≥1:100) |
208 (4,0) |
|
Группа промежуточного риска (1:101—1:2500) |
4973 (96,0) |
Результаты неинвазивного пренатального тестирования для группы высокого риска по комбинированному пренатальному скринингу (1:100 и выше)
Из 208 проанализированных образцов крови женщин из группы высокого риска по результатам скрининга результаты НИПТ, свидетельствующие о наличии хромосомной патологии (далее по тексту — положительный результат НИПТ), получены в 57 (27,40%) случаях (табл. 2). Из 208 случаев 138 образцов крови расценены как имеющие низкий риск наличия хромосомных аномалий (далее по тексту — отрицательный результат). В 6 случаях проведение НИПТ не удалось ввиду низкой фетальной фракции (ФФ), составившей менее 3,5%.
Таблица 2. Результаты неинвазивного пренатального тестирования по частым анеуплоидиям (трисомии 21-й, 18-й и 13-й хромосом)
|
Результат |
Число образцов |
Частота выявления в популяции |
|
|
группа высокого риска ≥1:100 |
группа промежуточного риска 1:101—1:2500 |
||
|
Трисомия 21 (синдром Дауна): |
1:650—1:1000 |
||
|
Выявленная патология |
38 |
12 |
|
|
Подтвержденная патология |
38 |
8 |
|
|
Ложноположительный результат |
0 |
1 |
|
|
В работе/нет данных* |
0 |
3 |
|
|
Трисомия 18 (синдром Эдвардса): |
1:6000—1:8000 |
||
|
Выявленная патология |
17 |
0 |
|
|
Подтвержденная патология |
17 |
0 |
|
|
Не подтвержденная патология |
0 |
0 |
|
|
В работе/нет данных* |
0 |
0 |
|
|
Трисомия 13 (синдром Патау): |
1:10 000—1:16 000 |
||
|
Выявленная патология |
2 |
3 |
|
|
Подтвержденная патология |
2 |
2 |
|
|
Не подтвержденная патология |
0 |
1 |
|
|
В работе/нет данных* |
0 |
0 |
Примечание. *— пациентка отказалась от проведения ИПД; НИПТ — неинвазивный пренатальный тест; ИПД — инвазивная пренатальная диагностика.
Положительный результат НИПТ по наличию у плода трисомии 21-й хромосомы (синдром Дауна) получен в 38 случаях, в 17 случаях получен положительный результат по наличию у плода трисомии 18-й хромосомы (синдром Эдвардса) и в 2 случаях — положительный НИПТ по наличию у плода трисомии 13-й хромосомы (синдром Патау). Все случаи частых анеуплоидий подтверждены по результатам ИПД.
Отрицательные результаты НИПТ у женщин группы высокого риска получены в 138 (66,3%) из 208 случаев. В 129 случаях по результатам ИПД получен нормальный кариотип плода, в 3 случаях — мозаицизм по половым хромосомам, обусловленный, вероятно, контаминацией материнской кровью при получении материала для исследования, в 1 случае — триплоидия у плода женского пола, и в 5 случаях нет данных о результате ИПД.
Результаты неинвазивного пренатального тестирования для группы риска 1:101—1:2500 по комбинированному пренатальному скринингу
Из 4973 проанализированных образцов крови женщин из группы риска 1:101—1:2500 по результатам скрининга положительный результат НИПТ для частых анеуплоидий получен в 15 (0,3%) случаях (см. табл. 2). Расценены как имеющие низкий риск наличия хромосомных аномалий 4750 (95,5%) из 4973 образцов крови. В 170 (3,4%) из 4973 случаев проведение НИПТ не удалось ввиду низкой ФФ (ниже 3,5%).
Положительный результат по наличию у плода трисомии 21-й хромосомы (синдром Дауна) выявлен в 12 случаях, из которых 8 подтверждены и 1 случай не подтвержден при ИПД (ложноположительный результат). От проведения ИПД 3 пациентки отказались.
В 3 случаях выявлен положительный результат наличия у плода трисомии 13-й хромосомы (синдром Патау). По результатам ИПД у 2 пациенток подтверждена патология, в 1 случае получен нормальный кариотип у плода (ложноположительный результат).
Отрицательный результат НИПТ у женщин группы промежуточного риска получен в 4750 случаях. В данной группе риска ИПД проведена 14 пациенткам, показаниями к проведению инвазивной диагностики были пороки развития у плода или ультразвуковые маркеры хромосомной патологии, выявленные при УЗИ второго триместра. По результатам ИПД: 13 получили нормальный кариотип у плода, в 1 случае выявлена патология — 46,ХХ,del(18)(p11.2) — делеция короткого плеча 18 хромосомы.
Всего выявлено 50 случаев положительных результатов НИПТ по трисомии 21-й хромосомы (синдром Дауна): 38 в группе высокого риска и 12 — в группе риска 1:101—1:2500. Всем пациентам из группы высокого риска проведена ИПД, во всех 38 случаях патология подтверждена. В группе риска 1:101—1:2500 из 12 случаев патология подтверждена в 8 случаях и не подтверждена только в одном случае. Возможной причиной одного ложноположительного результата является плацентарный мозаицизм. От проведения ИПД отказались 3 пациентки. Новорожденному одной из них проведено кариотипирование, выявлена трисомия 21-й хромосомы (синдром Дауна).
Положительные результаты НИПТ по трисомии 18-й хромосомы (синдром Эдвардса) выявлены в 17 случаях среди женщин группы высокого риска. Все 17 положительных результатов НИПТ подтверждены ИПД.
Положительные результаты НИПТ по трисомии 13-й хромосомы (синдром Патау) получены у 5 пациенток. Из 5 случаев патология подтвердилась у четверых (2 беременные из группы высокого риска и 2 — из группы риска 1:101—1:2500). В одном случае результат оказался ложноположительным. Причиной ложноположительного результата в данном случае также является высокая вероятность плацентарного мозаицизма.
Доля ложноположительных результатов для НИПТ по частым анеуплоидиям составила 2 из 4888 (0,04%), что значительно ниже, чем доля ложноположительных результатов для комбинированного пренатального скрининга первого триместра, которая составляет 2,5% (139) из 5181.
Из 5181 образцов повторный анализ крови рекомендован в 3,4% (176) случаев из-за низкой фетальной фракции (ФФ) (ниже 3,5%).
В случае низкой ФФ чаще наблюдали более высокие значения массы тела и индекса массы тела (ИМТ) беременных: 70,5 кг [60; 83] для низкой ФФ и 65 кг [58; 74] для ФФ выше 3,5%, p<0,001; ИМТ — 25,7 кг/м2 [22,2; 30,8] для низкой ФФ и 23,4 кг/м2 [20,9; 26,8] для ФФ выше 3,5%, p<0,001.
Выявлены факторы, предрасполагающие к увеличению уровня ФФ. Это высокий риск трисомии 21-й хромосомы и мужской пол плода. Отмечено, что положительные результаты НИПТ для трисомии 21-й хромосомы чаще выявляются при более высоких значениях ФФ, чем в образцах с отрицательными результатами: 11,1 [7,8; 14,2]% и 8,6 [6,3; 11,4]%, p<0,001 (рис. 2). Пороговое значение ФФ составило 10%. Однако такой зависимости для трисомий по 18-й и 13-й хромосомам не наблюдали, вероятно, из-за недостаточного количества выявленных случаев положительных результатов для данных хромосом. Показано, что для плодов мужского пола величина ФФ статистически значимо выше, чем для женского: 10,2 [7,6; 13,4]% и 7,2 [5,3; 9,2]%, p<0,001 (см. рис. 2).

Рис. 2. Средний уровень фетальной фракции для пациенток в зависимости от результатов неинвазивного пренатального тестирования: риска трисомии 21 и пола плода.
Не обнаружено статистически значимой зависимости между возрастом беременных женщин и положительными и отрицательными результатами НИПТ по трисомии 21-й хромосомы, p=0,457 (рис. 3). Но анализ положительных результатов НИПТ по всем аномалиям показал, что аномалии чаще встречались у женщин в возрасте 39 лет и старше: 6,9% положительных результатов у женщин старше 39 лет и 5% у женщин до 39 лет, p=0,009. Для спонтанных беременностей и беременностей, возникших в результате применения вспомогательных репродуктивных технологий, не было статистически значимой разницы по частоте положительных результатов НИПТ, p=0,728.

Рис. 3. Доля случаев с положительным результатом неинвазивного пренатального тестирования беременных женщин разных возрастных групп.
Следует отметить, что в рамках исследования НИПТ проводили полногеномным методом, это позволило также выявлять аномалии других хромосом, микроделеции и микродупликации. Описанию полученных результатов и находок посвящена отдельная работа.
Обсуждение
Мировой опыт
Открытие в 1997 г. циркуляции вкДНК в материнской плазме положило начало эре неинвазивного пренатального тестирования [9]. НИПТ впервые внедрен в пренатальную диагностику Китая в 2010 г. [10]. Уже в 2011 г. он нашел клиническое применение в Гонконге и США [11, 12]. С тех пор технология НИПТ быстро распространяется и становится все более доступной для беременных женщин во всем мире как в коммерческих, так и в государственных клиниках.
В некоторых европейских странах, таких как Нидерланды и Бельгия, НИПТ включен в государственную программу пренатального тестирования беременных женщин в качестве теста первой линии [7]. Эти страны провели большое количество исследований и доказали, что внедрение НИПТ в качестве теста первой линии является не только клинически, но и экономически эффективным. Авторы исследований утверждают, что НИПТ улучшает общую выявляемость частых трисомий с 81 до 99%, снижает количество инвазивных процедур на 72% у женщин группы высокого риска и на 60% у всех беременных женщин, а также снижает количество пропущенных случаев с 77 до 5 [13, 14].
В России первый шаг внедрения НИПТ сделан в апреле 2020 г. в Москве, когда этот метод был интегрирован в существующий пренатальный скрининг в качестве теста второй линии. Несмотря на непродолжительный период проекта (6 месяцев), его эффективность уже отмечена: в дополнение к результатам скрининга первого триместра с помощью НИПТ выявлено 10 случаев частых анеуплоидий (синдром Дауна, синдром Эдвардса, синдром Патау). Из 208 женщин, отнесенных к группе высокого риска по результатам скрининга в первом триместре, только у 57 получен положительный результат НИПТ по частым анеуплоидиям. Данный тест снижает частоту ложноположительных результатов до 0,04% (для частых анеуплоидий) и, соответственно, потребность в ИПД. В настоящее время снижение числа ИПД является лишь потенциальным, поскольку регулирование пренатального скрининга в России не учитывает результаты НИПТ, и все женщины с высоким риском после пренатального скрининга первого триместра должны проходить инвазивные процедуры [15].
Ложноположительные и ложноотрицательные результаты неинвазивного пренатального тестирования
НИПТ показывает более высокую чувствительность и специфичность и в целом более эффективен в выявлении частых анеуплоидий (до 99%) по сравнению с традиционным пренатальным скринингом, который составляет не более 96%, но обычно его точность около 85—90% [16, 17]. Несмотря на высокую точность, возможны ложноположительные и ложноотрицательные результаты. Известно, что основными биологическими причинами ложных результатов являются фетоплацентарный мозаицизм, злокачественные новообразования матери, феномен исчезающего близнеца [18]. Вместе с тем, несмотря на эти ограничения, считается, что НИПТ более точен, чем комбинированный пренатальный скрининг с гораздо меньшим процентом ложноположительных результатов. Частота ложноположительных результатов для частых анеуплоидий всех аномалий составила 0,04%. Этот показатель значительно ниже, чем в других публикациях. Ложноотрицательные результаты являются крайне редким феноменом для НИПТ и составляют в целом 0,01% [18].
Влияние фетальной фракции на результаты неинвазивного пренатального тестирования
Точность НИПТ зависит от множества технических и биологических факторов, которые взаимосвязаны друг с другом и влияют друг на друга. К ним относятся число прочтений при секвенировании, показатель ФФ, GC-содержание в геноме и другие. Поскольку вкДНК представляет собой смесь фрагментов геномной ДНК материнского и фетального (плацентарного) происхождения, точность НИПТ напрямую связана с уровнем ФФ [19]. В нашем исследовании для 176 (3,4%) случаев выявлена низкая ФФ (ниже 3,5%), и для этих пациенток рекомендован повторный забор материала. При повторном тестировании результат удалось получить у 136 пациенток. В 2 случаях после повторного забора материала обнаружен положительный результат НИПТ по трисомии 13, подтвержденный результатами ИПД. У 4 (2,4%) пациенток потребовалось 2—3 повторных взятия крови. От дальнейшего обследования отказались 8 пациенток.
До настоящего времени в различных исследованиях показано, что такие характеристики женщины и беременности, как ранний гестационный возраст, избыточная масса тела, многоплодная беременность, низкий уровень ХГЧ и тип зачатия, связаны со снижением ФФ [20]. В нашем исследовании проанализированы все эти параметры, за исключением данных ХГЧ, которые были недоступны. Статистически значимых различий между уровнем ФФ и возрастом матери, типом зачатия и количеством плодов не было. Вместе с тем продемонстрирована статистически значимая зависимость уровня ФФ от ИМТ, а также от массы тела беременной женщины. Таким образом, по мере увеличения массы тела и ИМТ снижался уровень ФФ.
ИМТ беременной является наиболее значимой антропометрической переменной, влияющей на уровень ФФ. В исследовании G. Ashoor и соавт. показано существенное снижение медианы ФФ у женщин с ожирением: у беременных с массой тела 60 кг она составила 11,7%, а у женщин с массой тела 160 кг — 3,9% [21]. Ремоделирование жировой ткани у беременных с ожирением связано с двукратным увеличением уровня маркера общей ДНК — GAPDH (glyceraldehyde-3-phosphate dehydrogenase) в сыворотке крови. Абсолютная концентрация ДНК плода не изменяется, но увеличение доли материнской ДНК приводит к относительному снижению ФФ. В совокупности масса тела матери и гестационный возраст плода составляли 27% индивидуальных вариаций, наблюдаемых при снижении ФФ [22].
В нашем исследовании также показано, что более высокий уровень ФФ чаще встречается у плодов мужского пола и у плодов с высоким риском трисомии 21 (см. рис. 2). Подобные наблюдения описаны в некоторых других исследованиях, которые показывают, что эуплоидные беременности мужского плода с высоким риском трисомии 21 имеют более высокий уровень ФФ [23]. В ряде исследований продемонстрировано снижение уровня ФФ для трисомий по хромосоме 18 и хромосоме 13, а также моносомии хромосомы X. В нашем исследовании не наблюдалось подобной зависимости уровня ФФ и положительных результатов для трисомий 13, 18 и моносомии X, что, вероятно, связано с низкой представленностью данных результатов. Анализ вышеупомянутых связей требует дополнительно изучения.
Возраст матери
Считается, что беременность женщин в позднем репродуктивном возрасте (старше 35 лет) связана с различными осложнениями, включая генетические аномалии у детей. Проанализирована частота положительных результатов НИПТ в зависимости от возраста матери. В большинстве опубликованных исследований пороговый возраст для повышенных рисков хромосомных аномалий составляет 35 лет, однако в нашем исследовании наблюдалась значительно более высокая частота положительных результатов НИПТ для женщин в возрасте 39 лет и старше (см. рис. 3). В ряде публикаций сообщалось, что частота таких хромосомных аномалий плода, как трисомия 21-й хромосомы, трисомия 18-й хромосомы, трисомия 13-й хромосомы, трисомия хромосомы X и XYY-синдром, возрастает с увеличением материнского возраста [14]. В августе 2020 г. ACOG предложила проводить НИПТ для всех беременных женщин независимо от возраста или других факторов риска [24].
Преимущества и ограничения неинвазивного пренатального тестирования
Несомненно, главным преимуществом НИПТ является его высокая чувствительность и специфичность в отношении распространенных анеуплоидий [25]. НИПТ обладает самой высокой точностью среди всех скрининговых методов выявления синдрома Дауна. Чувствительность для трисомии по 21-й хромосоме составляет 99,17%, а специфичность — 99,94%. Также НИПТ показывает высокую точность выявления других частых аномалий (синдром Эдвардса, синдром Патау): чувствительность теста в отношении трисомии 18 и трисомии 13 составляет 97,80 и 95,92% соответственно, тогда как специфичность — 99,94%. Прогностическая ценность положительного результата составляет 96,07, 88,97 и 65,73% для трисомии 21, трисомии 18 и трисомии 13 соответственно [26].
Суммируя, можно сказать, что полногеномный НИПТ следует рекомендовать всем беременным женщинам как в группе высокого, так и в группе промежуточного риска. Более того, в перспективе целесообразно рассматривать НИПТ в качестве теста первой линии [27].
Выводы
1. Полученные результаты исследования продемонстрировали эффективность использования неинвазивного пренатального тестирования в пренатальной диагностике в Москве в качестве теста второй линии.
2. Высокая чувствительность метода позволила снизить долю ложноположительных результатов и увеличить частоту выявления наиболее частых анеуплоидий в группе промежуточного риска по сравнению с комбинированным пренатальным скринингом в первом триместре беременности.
Участие авторов:
Концепция и дизайн исследования — Оленев А.С., Сагайдак О.В., Баранова Е.Е., Кузнецова Е.С.
Сбор и обработка материала — Беленикин М.С., Косова Е.В., Зобкова Г.Ю., Капланова М.Т., Галактионова А.М., Макарова М.В.
Статистический анализ данных — Сагайдак О.В., Кузнецова Е.С., Галактионова А.М.
Написание текста — Кузнецова Е.С., Сагайдак О.В.
Редактирование — Оленев А.С., Сонголова Е.Н., Гнетецкая В.А., Сагайдак О.В., Баранова Е.Е., Галактионова А.М.
Финансирование: субсидии из бюджета Москвы №01-04-410 от 06.02.20.
Авторы заявляют об отсутствии конфликта интересов.

_w400_h273.png)