21
ОБЗОРЫ
© Т.С. Козлова, С.А. Кононова, 2013 УДК 340.6
Т.С. Козлова1, С.А. Кононова2
ЛОКАЛЬНЫЕ ПОСТИНЪЕКЦИОННЫЕ ОСЛОЖНЕНИЯ:
ПРИЧИНЫ ВОЗНИКНОВЕНИЯ, ИХ ТЕПЛОВИЗОРНАЯ ОЦЕНКА
1БУЗ УР «Городская клиническая больница № 1 МЗ УР» (гл. врач — к.м.н. М.Ю. Тихомирова); 2ГАУЗ «Республиканское бюро судебно-медицинской экспертизы МЗ РТ»
(и.о. начальника — д.м.н., доц. В.А. Спиридонов)
В статье приведены данные литературы о локальных постинъекционных осложнениях и методах их выявления с использованием тепловизорной диагностики.
Ключевые слова: локальные постинъекционные осложнения, судебно-медицинская экспертиза.
LOCAL POSTINJECTION COMPLICATIONS: CAUSES AND THEIR EVALUATION THERMAL IMAGING
T.S. Kozlova, S.A. Kononova
The paper presents the data in the literature on local postinjection complications and methods of detecting those using
Thermal Imaging diagnostics.
Key words: local post-injection complications, forensics.
Проблема исследования неблагоприятных исходов в медицинской практике, являясь острейшей социальной темой, представляется чрезвычайно многоплановой и разнообразной. Неблагоприятные исходы в медицинской практике наблюдаются от незначительных повреждений структуры и функции тканей и органов до таких, которые относятся к тяжким последствиям для здоровья пациента [4, 34, 54]. Среди них находятся локальные осложнения при парентеральном введении лекарственных препаратов, которым уделяется не всегда должное внимание.
Из истории появления инъекционного введения лекарственных препаратов известно, что еще в 1656 году английский архитектор Кристофер Рен (Christopher Wren, 1632-1723) начал проводить эксперименты по внутривенным введениям настойки опия, пива, вина, эля, молока, при этом в качестве инъекционной иглы использовалось птичье перо, вместо шприца — пузыри рыб, животных. Результаты исследований опубликованы в 1665 г. в «Философских трудах Лондонского Королевского общества». Широкое осознание медицинской общественностью возможностей парентерального введения лекарств наступило только после публикации работ Нормана Говарда-Джонса, изучавшего эффекты укусов ядовитых змей и насекомых и предположившего, что через подобный прокол можно вводить лекарства. Однако, несмотря на то, что почести за изобретение шприца (1855) историки отдают Александру Вуду (Alexander Wood, 1817-1884) секретарю Королевского колледжа врачей в Эдинбурге, ряд ученых считает его изобретателем только полой иглы, а создателями шприца называют A. Neuner (1827), создавшего «Стилет», F. Rynd (1844), сделавшего тонкий троакар с пружиной, C.G. Pravaz (1852), создавшего шприц и троакар с канюлей из золота, и наконец, британского производителя хирургических
инструментов D. Fegusson (1853), продемонстрировавшего стеклянный шприц с полым троакаром для введения жидкостей [43].
За длительную историю парентерального введения лекарств иглы и шприцы претерпели множество изменений. В работе H.M. Greene [цит. по 43], один из первых проводил эксперименты на трупах, испытывая иглы, и пришел к выводу: иглы разной формы острия оставляют различную величину и форму прокола, при этом, чем тоньше игла, тем меньше возникает побочных эффектов. Сегодня в арсенале медицины есть возможность сочетать разные преимущества игл и специальных шприцев, изготовленных из инертных для пациента пластика, металла и стекла и используемых однократно. Однако, несмотря на разные технические возможности парентерального введения лекарств, проблема локальных постинъекционных осложнений продолжает оставаться актуальной.
В течение года на территории субъекта РФ проводится около 8,4 — 9,1 млн. различных парентеральных вливаний лекарственных средств и 469 — 525 тыс. введений иммунобиологических препаратов. В 5,5% случаев населению проводится вакцинация, ревакцинация, туберкулинодиагностика. На каждого жителя региона, включая детей, ежегодно приходится по 12,4-13,0 инъекций. Удельный вес внутримышечных инъекций составляет 73,6% на амбулаторно-поликлиническом обслуживании и 50,2% — в условиях стационара. В стационаре приходится на 1 пациента 43,1 — 49,0 инъекций за одну госпитализацию [42]. Параллельно с увеличением числа инъекций нарастает и число постинъекционных осложнений. По данным научной литературы к постинфекционным осложнениям относят как местные, так и общие явления — головокружение, коллапс, нарушение ритма сердца вследствие
22
слишком быстрого введения лекарственного препарата, повреждения надкостницы (периостит), сосудов (флебит, некроз, эмболия воздушная или медикаментозная), нервов (паралич, неврит), аллергические реакции, некроз тканей, гематому, инфильтрат, абсцесс, сепсис, сывороточный гепатит, а также ВИЧ-инфекцию [13, 26, 32, 33, 36, 42]. Инфильтраты, гематомы в местах инъекций являются частым осложнением у госпитализированных пациентов и значительно снижают качество оказания медицинской помощи [32, 36, 47]. Наиболее часто встречаются в месте непосредственной инъекции локальные постинъекционные осложнения [4, 40, 42]. Это порождает судебные разбирательства и стимулирует поиск необходимых экспертных методик для объективной оценки деятельности медицинских работников [9, 12, 18, 31].
Юридическую оценку действий медицинских работников связанных с неблагоприятными исходами медицинской деятельности дают правоохранительные органы и суды, при этом всегда назначается судебно-медицинская экспертиза [9, 31]. Судебные медики оценивают постинъекционные осложнения и решают вопрос о причинной связи их появления с дефектами оказания медицинской помощи [39]. В случае постинъекционных осложнений деяния медицинских работников становятся противоправными с наступлением общественно опасных последствий при условии нарушения медицинских правил [25, 31].
Дискуссия об обязательном участии судебно-медицинской службы в контроле качества медицинской помощи, казалось бы, завершена с появлением 21 ноября 2011 года ФЗ № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», где выделена экспертиза качества медицинской помощи, но не решен вопрос о субъекте проведения такой экспертизы. Это явилось поводом для отдельных мнений, например В.А. Козырев, Р.В. Калинин [21], когда компетентность судебно-медицинского эксперта и патологоанатома при анализе летальных исходов в медицинской организации не только ставится под сомнение, но и указывается об их выходе за пределы своей компетенции при осуществлении своих должностных (трудовых) функций. Поэтому не потеряли актуальности работы судебных медиков, рассматривающих обязательность проведения судебно-медицинской экспертизы при возникновении дефектов лечения и их оценки [4, 12, 14, 32, 40, 41 и др.].
По поводу локальных постинъекционных осложнений проводятся судебно-медицинские комиссионные экспертизы, где решающая роль отводится эксперту бюро СМЭ. Качественное судебно-медицинское экспертное исследование случаев смерти пациентов осуществляется при составлении клинико-патоморфологического эпикриза и участия эксперта в работе клинико-патоморфологической конференции [21]. Объективное отражение причин дефектов и ятрогений возможно при сочетании нозологического, этиологического, патогенетического принципов, а также системности, стандартизации [31, 38, 39]. В то же время, значимость танатологического критерия является решающим аргументом при взаимодействии врачей клинического профиля и судебно-медицинских экспертов, клинических фармакологов [2, 14, 14].
Терминология является важным фактором в оценке медицинских происшествий. Так, В.В. Томилин [39] приводит 65 понятий «врачебная ошибка» носящих различный смысл: от небрежных, недобросовестных действий и приемов оказания медицинской помощи до телесных повреждений или смерти больного, или от заблуждений врача без элементов халатности и небрежности до профессионального невежества. В отношении локальных
постинъекционных осложнений А.А. Касаткин с соавт. [20] приводят определение и связывают с инъекционной болезнью с собственной этиологией, патогенезом, требующей проведения экспертизы безопасности растворов лекарственных препаратов перед их введением. В этой связи С.В. Ерофеев [17] предостерегает судебно-медицинских экспертов и предлагает исключать из лексикона термины, несущие юридический смысл.
Знание патогенеза различных вариантов постинъекционных осложнений позволяет более четко определить их причину и возможности профилактики. В случае многократного и многодневного введения растворов лекарственных средств посредством стандартных устройств для инфузии и сосудистых катетеров скорость введения однотипных растворов постепенно снижается. Поэтому даже при увеличении давления жидкости в системе за счет увеличения высоты штатива с флаконом, содержащим вводимый раствор, увеличение срока установки катетера прогрессивно снижает его пропускную способность вплоть до полного прекращения поступления препаратов в венозное русло [56].
Многократное введение лекарственных препаратов в одну точку интенсивно травмирует ткани мышц (иглой, лекарством) и может привести к развитию абсцесса даже при должном соблюдении правил асептики. Доза препарата, безвредная при однократном введении, при повторном введении в одно и то же место может вызвать некроз ткани даже при стерильной технике инъекции. Лекарственные препараты, предназначенные для введения внутримышечно, при инъекции под кожу вызывают асептический некроз ткани в месте введения, например, глюконат кальция, многие антибиотики, витамины группы В [40, 41, 44, 52]. Нередки постинъекционные осложнения при внутривенном введении, проявляющиеся флебитами и флеботромбозами, связанные как с внесением инфекции при выполнении этих манипуляций, так и с самим препаратом, раздражающим сосудистую стенку (калия хлорид, некоторые антибиотики и др.) [43, 50].
Дефекты лечения, обусловленные неблагоприятными лекарственными реакциями, в разных странах отмечаются в 5-10%, последствиями которых выступают смерть, состояния, угрожающие жизни [11, 30, 54]. Существенное место занимают дефекты, связанные с нарушением принципа безопасности применения лекарственных препаратов (несвоевременно, неправильно выбраны доза, способ, скорость, кратность введения либо техника исполнения, нерациональное сочетание, ошибочное применение) [1, 5, 24, 41]. Внутривенные инфузии и трансфузии представляют повышенную опасность без тщательного анализа физикохимических и биологических показателей качества используемых лекарственных препаратов разных серий и заво-дов-изготовителей [18, 37]. Так, «…малейшая неточность в их назначении может стать причиной неблагоприятных эффектов, пагубно отражающихся на состоянии пациентов» [41]. Ни одна врачебная манипуляция, по мнению И.В. Тимофеева, не сопряжена с такой степенью опасности возникновения дефектов и развития ятрогений как инъекции растворов лекарственных препаратов [38, 49, 51].
Vere D.W. [54] в 1976 г. первым описал способность неблагоприятных лекарственных реакций выступать под маской обычных заболеваний и указал причины, вследствие которых они в большинстве остаются незамеченными. Я.Я. Балткайс, В.А.Фатеев [3] указывают, что назначение 1-5 лекарств приводит к развитию неблагоприятных лекарственных реакций у 4% больных, а при назначении 1620 неблагоприятные лекарственные реакции наблюдаются у 54% больных. Ряд авторов указывают, что неблагоприят-
23
ные лекарственные реакции вызываются лекарствами, в применении которых не было необходимости [28, 40, 48]. Эндогенными факторами, изменяющими фармакодинамику и фармакокинетику лекарств, являются возраст, пол, вес, заболевания печени, почек, беременность [24, 30, 40, 41, 43]. Лекарственные препараты различаются по своим физико-химическим свойствам, что может отражаться на результатах лечения [10, 33, 34]. Так, П.Ю. Садиловой [37] выявлено местное влияние растворов лекарств с разной осмолярностью и кислотностью на морфофункциональный состав форменных элементов крови (эритроцитов) при их инъекционном и инфузионном введении.
Учитывая причастность медицинских работников к возникновению постинъекционных осложнений, следует обратить внимание на то, что основной организатор, исполнитель и ответственный контролер данной манипуляции — это медсестра [4, 8, 32, 44]. Однако изучение причин постинъекционных осложнений выявляет множество причин, не связанных с деятельностью медицинской сестры [18, 34]. Знание их во многих случаях дает возможность профилактики, защиты и доказательности невиновности медицинских работников. В этой связи актуальным представляется разработка методики, позволяющей проводить оценку локальных постинъекционных осложнений, что позволит выявлять их причину и осуществлять профилактику более грозных осложнений.
Активно развивающаяся на рубеже ХХ-XXI вв. биомедицина, приводит к переосмыслению накопленных медициной фактов на молекулярном уровне [19] и предлагает новые методики. О том, что температура человека является показателем его физиологического состояния, известно давно. Температуру кожи человека как диагностический показатель использовал Гиппократ (примерно 460-377 гг. до н.э.) [45].
Качественным скачком, приведшим к появлению дистанционных методов измерения температуры в первой четверти XX в., стало осознание того факта, что радиация в инфракрасной области спектра электромагнитных длин волн связана с температурой [46]. В тепловидении произошел качественный скачок, когда были открыты новые химические структуры, существенно изменяющие в зависимости от температуры свою проводимость, или требовали для внутренней эмиссии электронов невысоких значений энергии световых квантов. С их помощью можно было воспринимать сравнительно длинноволновую область спектра (длина волны более 6 мкм). Максимум теплового излучения тел при комнатной температуре приходится на длины волн около 10 мкм. Тепловизоры 1970-х годов обладали чувствительностью до нескольких долей градуса [55]. Поскольку тепловизоры обладали низким пространственным разрешением, попытки использовать их в медицине заканчивались неудачей. Тем не менее, области применения тепловизионных систем тех лет в науке и технике, а затем и в медицине постепенно расширялись.
На вопрос, кто и когда впервые применил тепловидение в клинической практике, ответить трудно. Известно, что R.N. Lawson в 1956 г. применил прибор ночного видения (использовавшийся в военных целях) для ранней диагностики опухолей молочных желез. В канадском медицинском журнале была опубликована его статья «Thermography — a new tool in the investigation of breast lesions» [22]. Достоверность определения рака молочной железы, особенно на ранней стадии, составила по данным Лоусона около 60-70%.
По наличию в теле человека зон с аномально высокой или низкой температурой можно распознать многие болезни (150 заболеваний) даже на ранних стадиях их возникновения [47].
Тепловизионная диагностика нашла применение в самых разных областях медицины: при диабетической ангиопатии, атеросклерозе, эндартериите сосудов конечностей, болезни Рейно, оценке кровоснабжения мозга при черепно-мозговых травмах и воспалительных процессов лица человека, гепатитах, нарушениях вегетативной регуляции, воспалении легких и придаточных пазух носа, заболеваниях почек и мочевого пузыря, поражениях периферических нервов, нарушениях и воспалительных заболеваниях позвоночника и крупных суставов различной этиологии, при маститах, раке молочной железы и раке кожи, в наблюдении приживления пересаженной кожи, в сосудистой хирургии и нейрохирургии и др. [7, 15, 23, 29, 35, 51, 47].
Температурные поля, выявляемые на термограммах, зависят в первую очередь от величины теплового потока, который передается на поверхность тела сердечно-сосудистой системой. Поэтому любой патологический процесс, так или иначе вовлекающий сосудистую систему, находит свое отражение на термограммах [53]. Тепловизионная картина той или иной области тела зависит от притока и оттока крови, т.е. от функционального состояния артерий, вен, а также связывающих их артериол, капилляров и венул. При наличии какого-либо патологического процесса, сопровождающегося воспалительными реакциями, нарушениями кровообращения, обмена веществ, происходит изменение нормальной картины распределения температуры по поверхности тела, что и фиксируется в виде температурной асимметрии [20].
В судебной медицине температуру кожи в области кровоподтека методом электротермометрии изучали А.А. Евстафьев [16], Н.Г. Маркелова [27], С.А. Кононова [22] и др. Тепловидение удачно совмещает визуализацию патологии и абсолютную безвредность для больного и медицинского персонала. Визуальная (качественная) оценка термографии позволяет определить расположение, размеры, форму и структуру очагов повышенного излучения, а также ориентировочно оценивать величину инфракрасной радиации [9]. В сочетании с цифровой термографией [19], исследователь в состоянии получить не только картину изменения теплового поля объекта, но и объективно судить о динамике изучаемого процесса.
Анализ данных термограмм включает их качественную (распределение «горячих» и «холодных» участков) и количественную (с определением показателей разности температур исследуемого участка по сравнению с симметричной зоной тела, окружающими тканями, условно выбранной областью) оценку, а также обработку изображения с помощью компьютера. Наличие патологического процесса может проявляться одним из трех термографических признаков: появлением аномальных зон гипертермии или гипотермии, нарушением нормальной термотопографии сосудистого рисунка, а также изменением градиента температуры в исследуемой зоне. Решая проблему локальных постинъекционных осложнений, тепловизорное мониторирование области инъекции лекарственных препаратов может обеспечить эффективное и безопасное выявление локальных постинъекционных осложнений, их профилактику и экспертную оценку.
Литература:
1. Арефьев Г.Н., Мурзин К.А., Белозеров Ю.А. Лекарственное лечение: ошибки, экспертное освидетельствование // Забайкальский медицинский вестник. — Чита, 1996. — №1. — С. 38-39.
24
2. Атлас по судебной медицине; под ред. Ю.И. Пиголкина, И.Н. Богомоловой. — М.: ООО Медицинское информационное агентство, 2006. — 312 с.
3. Балткайс Я.Я., Фатеев В.А. Взаимодействие лекарственных веществ (фармакотерапевтические аспекты). — М.: Медицина, 1991. — 304 с.
4. Баринов Е.Х. Судебно-медицинская экспертиза в гражданском судопроизводстве по медицинским делам. — М.:НП ИЦ «ЮрИн-фоЗдрав». — 2013. — 164 с.
5. Беликов Е.С. Медико-экспертная квалификация ятрогений по материалам патологоанатомических исследований: автореф. дис… д-ра мед наук. — Челябинск, 1999. — 38 с.
6. Беляева О.А., Толстых П.И. Постинъекционные инфильтраты и флегмоны. — К., 1986. — 236 с.
7. Богин Ю.Н., Стулин И.Д., Глориозова Т.Г. О применении тепловидения в диагностике некоторых заболеваний нервной системы //Журн. невропатологии и психиатрии им. С.С. Корсакова. — 1975. — № 5. — С. 663-867.
8. Внутрибольничные инфекции / Под ред. Р.П. Венцела; пер. с англ. — М.: Медицина. — 1990.- 656 с.
9. Возианов А.Ф., РозенфельдЛ.Г. Клиническая термодиагностика. Атлас термограмм. — Киев, Здоров’я, 1991. — 64 с.
10. Вопросы экспертизы фальсифицированных лекарственных средств в судебной медицине и фармации /В.И. Витер и [др.] //Проблемы экспертизы в медицине. — 2003. — т.3. — №3. — С. 7-10.
11. Врачебные ошибки как причина осложнений лекарственной терапии /В.К.Лепахин и [др.]//Качественная клиническая практика.
— 2002. — №1. — 71 — 77.
12. Гецманова И.В. Актуальные вопросы судебно-медицинских экспертиз по делам о дефектах оказания медицинской помощи // Судебная экспертиза. — 2007. — № 1. — С. 88-94.
13. Гостищев В.К., ШалчковаЛ.П. Гнойная хирургия таза: Руководство для врачей. — М.: Медицина, 2000. — 288 с.
14. Давыдовский И.В. Опыт сличения клинических и патологоанатомических диагнозов // Клиническая медицина. — 1928. —т. 1. — №19. — С. 2—19.
15. Дистанцшна тфрачервона термографiя в ортопеда та травматологи / Л. Г. Розенфельд [и др.] // Променева дiагностика, про-менева тератя. — № 1. — 2007. — С. 5-8.
16. Евстафьев А. А. Определение давности происхождения кровоподтеков электротермометрическим методом : автореф. дис… канд. мед. наук. — М., 2001. — 24 с.
17. Ерофеев С.В. Судебно-медицинская экспертиза неблагоприятных исходов при оказании медицинской помощи: автореф. дис… д-ра мед. наук. — М., 2000. —43 с.
18. Значение определения физико-химических показателей качества лекарств в клинико-фармакологической оценке степени безопасности инфузионной терапии /А.Л. Ураков и [др.]. //Нижегородский медицинский журнал. — 2004. — №1. — С. 9-12.
19. Иваницкий Г. Р. Современное матричное тепловидение в биомедицине // Успехи физических наук, 2006. — T. 176. — Ns 12. — С. 12931320.
20. Касаткин А.А., Уракова Н.А, Решетников АП. Экспертиза безопасности растворов натрия цефоперазона при внутримышечных инъекциях // Проблемы экспертизы в медицине, 2013. №2. — С.13-15.
21. Козырев В.А., Калинин Р.В. Выход за пределы компетенции при работе судебного медика и патологоанатома с клиническими случаями //Медицинская экспертиза и право, 2012. — №3. — С. 3-6.
22. Кононова С.А. Диагностика давности телесных повреждений бесконтактным термометрическим методом: дис. канд. мед наук. — М., 2010. — 151 с.
23. Краснов Д.Б. Диагностические возможности функционального тепловидения при повреждениях нервов плеча и предплечья: автореф. дис… канд. мед. наук. — М.: Институт нейрохирургии им. акад. Н. Н. Бурденко АМН СССР, 1989. — 24 с.
24. Лазарян, АГ. Использование антибиотиков: ошибки и пути оптимизации // Фармация, 1999. — №1. — т. XLVIII. — С. 39—40.
25. Леонтьев О.В. Нарушения норм уголовного права в медицине: практическое руководство. — СПб.: СпецЛит, 2002. — 67 с.
26. Ломонци Д. Внутрибольничные инфекции. — М.:Медицина, 1978. — 452 с.
27. Маркелова Н.Г. Комплексная биофизическая диагностика давности кровоподтеков у живых лиц: автореф. дис… канд. мед. наук.
— М, 2008. — 24 с.
28. Мякотный В.С., Боровкова Т.А. Сравнительные аспекты монотерапии и полипрагмазии у неотложных больных //Клиническая геронтология, 2001. — №10. — т. 7. — С. 38-41.
29. Новые возможности дистанционной инфракрасной термографии в оториноларингологии / Д. И. Заболотный [и др.] // Журн. вушних, носових i горлових хвороб, 2006 — № 5. — С. 2-5.
30. Основы клинической фармакологии и рациональной фармакотерапии: рук. для практикующих врачей /Ю.Б.Белоусов и [др.].; под общ. ред. Ю.Б.Белоусова, М.В.Леоновой. — М.: Бионика, 2002. — 368 с.
31. Пашинян Г.А, Ившин И.В. Судебно-медицинская экспертиза профессиональных правонарушений медицинских работников // Актуальные проблемы криминалистики и судебных экспертиз. — Ижевск: Экспертиза, 2007. — С. 66-74.
32. Покровский В.И., Семина Н.А Внутрибольничные инфекции — проблемы и пути решения // Эпидемиология и инфекционные болезни, 2000. — № 5. — С. 12-24.
33. Постмортальная клинико-фармакологическая оценка влияния введенных в вену растворов лекарственных средств на процесс прижизненного развития ацидоза или алкалоза / Н.С.Стрелков и [др.] // Проблемы экспертизы в медицине, 2002. — т.3. — №2. — С.12-15.
34. Постмортальная клинико-фармакологическая оценка влияния инфузионно введенных в стационаре растворов лекарственных средств на процесс прижизненного развития гипо— или гиперосмолярной комы /А.Л.Ураков и [др.] //Проблемы экспертизы в медицине, 2001. — № 2. — С. 22-24.
35. Применение цифровой контактной термомаммографии в диагностике рака молочной железы /В.В. Приходченко [и др.] // Онкология, 2007. — т. 9. — № 2. — С. 115-119.
36. Профилактика внутрибольничных инфекций : Руководство для врачей /Под ред. Е.П.Ковалевой, Н.А.Семиной. — М.:ТОО “Раро-гъ ”, 1993. — 228 с.
37. Садилова П.Ю. Влияние уровней осмолярности и кислотности лекарственных средств для инъекций на состояние некоторых форменных элементов крови человека при их взаимодействии in vitro: дис… канд. мед. наук. — Ижевск, 2003. — 162 с.
38. Тимофеев И. В. Патология лечения. Руководство для врачей. — СПб: Северо-Запад, 1999. — 656 с.
39. Томилин В.В., Пашинян Г.А Руководство по судебной медицине. — М.: Медицина, 2001. — С. 559-560.
40. Ураков АЛ. Основы клинической фармакологии. — Ижевск: Ижевский полиграфкомбинат, 1997. — 237 с.
41. Харкевич Д. А. Фармакология: Учеб. для студ. мед.; 4 изд. — М.: Медицина, 1993. — 544 с.
42. Чернова О. Э. Эпидемиология и профилактика постинъекционных осложнений: автореф. дис… канд. мед. наук. — М., 2006. — 53 с.
43. Шифман Е.М., Филиппович Г.В. Спинномозговая анестезия в акушерстве. — Петразаводск: ИнтелТек, 2005. — 558 с.
44. Якунская Т.В. Сестринское вмешательство на центральной вене //Медицинская помощь. — 1996. — № 9. — С. 33-35.
45. Adams F. “Hippocratic writings”, in Great Books of the Western World (Editor-in-ChiefR M Hutchins). — Hippocrates. Galen (Chicago: W.Benton, Encyclopedia Britannica Inc., 1952). Vol. 10 — P. 66.
25
46. Anbar M. Quantitative Dynamic Telethermometry in Medical Diagnosis and Management. Boca Raton: CRC Press, 1994. — Ch. 4. — Р. 99.
47. Anbar M., Gratt B.M., Hong D. Thermology and facial telethermography. Part I: History and technical review // Dentomaxillofac Radiology. — 1998, №. 2 — P. 61.
48. Benumof J.L. Clinical procedures in anesthesia and intensive care. — Philadelphia: Lippincott, 1992. — 600 p.
49. Blackshear R.H., Crosson K.C. Reduction in Pulmonary Embolism after Total Joint Arthroplasty: Three Years of Experience with Extended-Release Epidural Morphine //Pain Pract., 2010. — May/June. — Vol. 10, Issue 3, p. 235-244.
50. Diagnosis of catheter-related infections / F. Blot [et al.] // Catheter related infections. 2-nd ed. New York. — 2004. — P. 37-72.
51. Gualeri E., Deppe S.A., Sipperly M.E. Катетеризация подключичной вены: ультразвуковой контроль позволяет менее опытным врачам добиться лучших результатов //Вестник интенсивной терапии. — 2006. — №4. — С. 77-81.
52. Pharmacokinetic evaluation of linezolid in patients with major thermal injuries /R. Le Floch [et al.] //Pathol Biol. — 2010. — Apr; 58(2): p. 27-31.
53. Sarpal N. Drag administration — Infusion Devices’, in Dougherty L. and Lister S (editors). — 2008. — The Royal Marsden Hospital Manual of clinical nursing procedures (7th edition), Oxford: Blackwell Publishing. (III).
54. Vere D.W Drug adverse reactions as masqueraders //Adverse Drug Reaction Bull., 1976. — 60: 208-211.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
55. Vincen J. D. Radiometry —fundamentals of infrared detector operation and testing. — New York: Wiley, 1990. — Ch. 3.
56. Zingg W., Pittet D. Peripheral venous catheters: an under-evaluated problem // Int J Antimicrob Agents., 2009. — 34. Suppl 4. — S. 38-42.

Главный редактор, заведующий хирургическим отделением
Задать вопрос
Врач-хирург высшей квалификационной категории, доктор медицинских наук, профессор кафедры общей хирургии АГМУ.
Инъекции внутрикожные, подкожнык, внутримышечные, внутривенные.
Инъекция — способ введения в организм неких растворов (например, лекарственных средств) с помощью шприца и пустотелой иглы или впрыскиванием под высоким давлением (безыгольная инъекция).
Содержание
- Виды инъекций
- Внутримышечные инъекции
- Подкожные инъекции
- Внутривенные инъекции
- Внутривенное капельное введение растворов: выбор системы и проведения процедуры
- Показания и противопоказания
- Оптимальный выбор
- Необходимая оснастка
- Подготовительный этап
- Алгоритм выполнения
- Завершение инъекции
- Возможные осложнения
- Введение лекарств в барабанную полость
- Суть манипуляции
- Когда используется транстимпанальный метод введения лекарств?
- Методика процедуры
- Схема введения медикаментов в барабанную полость
- Для чего нужна данная процедура?
- Ограничения после транстимпанального введения в барабанную полость уха лекарств
- Осложнения местной анестезии
- МКБ-10
- Общие сведения
- Причины
- Патогенез
- Классификация
- Симптомы
- Диагностика
- Лечение осложнений местной анестезии
- Прогноз и профилактика
Виды инъекций
К основным видам инъекций относят следующие:
- внутрикожная (или интрадермальная) — (intracutaneous или intradermal)
- подкожная (subcutaneous)
- внутримышечная (intramuscular)
- внутривенная (intravenous)
- внутриартериальная
- внутрикостная
Внутримышечные инъекции
Внутримышечная инъекция — один из наиболее распространённых способов введения небольших объёмов лекарственных веществ. Мышцы обладают разветвлённой сетью кровеносных и лимфатических сосудов, что создаёт хорошие условия для всасывания лекарств. При внутримышечной инъекции создаётся депо, из которого препарат постепенно всасывается в кровеносное русло, что позволяет поддерживать примерно одинаковую концентрацию действующего вещества в крови в течение нескольких часов и тем самым обеспечить его длительное действие.
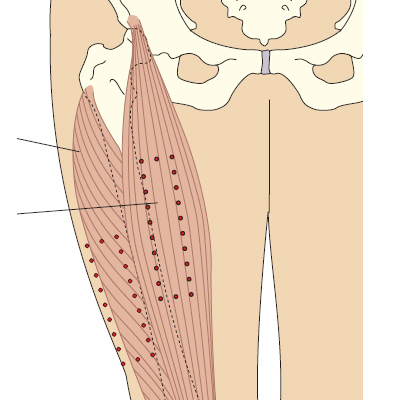
Для предотвращения осложнений, внутримышечные инъекции рекомендуется производить в местах тела, где имеется значительный слой мышечной ткани, и близко не располагаются крупные сосуды и нервные стволы. Длина применяемой иглы зависит от толщины слоя подкожно-жировой клетчатки, так как необходимо, чтобы при введении игла прошла подкожную клетчатку и срез её располагался непосредственно в мышце. Инъекции производят обычно в ягодичные мышцы, реже — в мышцы передней поверхности бедра или дельтовидную мышцу.
Возможные осложнения внутримышечных инъекций
При внутримышечных инъекциях возможны следующие осложнения:
- Попадание иглы в кровеносный сосуд, что может привести к эмболии, если вводятся масляные растворы или взвеси, которые не должны попадать в непосредственно в кровоток. При применении подобных препаратов после введения иглы в мышцу оттягивают поршень назад и убеждаются в отсутствии крови в шприце.
- Инфильтраты — болезненные уплотнения в толще мышечной ткани на месте укола. Могут возникнуть на второй-третий день после инъекции. Причинами их возникновения может быть как несоблюдение правил асептики (нестерильный шприц, плохо обработанное место укола), так и многократное введение препаратов в одно и то же место, или повышенная чувствительность тканей человека к вводимому препарату (характерно для масляных растворов и некоторых антибиотиков).
- Абсцесс — проявляется гиперемией и болезненностью кожи над инфильтратом, повышенной температурой тела. Требует срочной хирургической обработки и лечения антибиотиками.
- Аллергические реакции на введённый препарат. Для избежания данных осложнений перед введением препарата собирается анамнез, выясняется наличие аллергических реакций на какие-либо вещества. При любом проявлении аллергической реакции (независимо от способа предыдущего введения) целесообразна отмена препарата, поскольку повторное введение данного лекарственного средства может привести к анафилактическому шоку.
Подкожные инъекции
Применяется, например, при введении инсулина.
Подкожно-жировой слой обладает густой сосудистой сетью, поэтому введённые подкожно лекарственные вещества оказывают действие быстрее по сравнению с введением через рот — они минуют желудочно-кишечный тракт, попадая непосредственно в кровоток. Подкожные инъекции производят иглой самого малого диаметра и вводят до 2 мл лекарственных препаратов, которые быстро всасываются в рыхлой подкожной клетчатке, не оказывая на неё вредного воздействия.
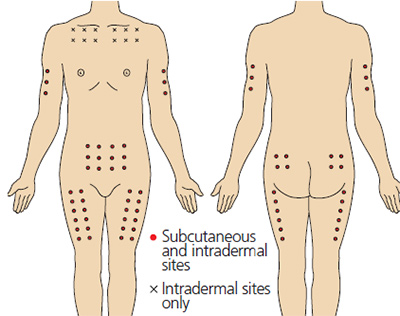
Наиболее удобными участками для подкожного введения являются:
- наружная поверхность плеча;
- подлопаточное пространство;
- передне-наружная поверхность бедра;
- боковая поверхность брюшной стенки;
- нижняя часть подмышечной области.
В этих местах кожа легко захватывается в складку и минимальна опасность повреждения кровеносных сосудов, нервов и надкостницы.
Не рекомендуется производить инъекции:
- в места с отёчной подкожно-жировой клетчаткой;
- в уплотнения от плохо рассосавшихся предыдущих инъекций.
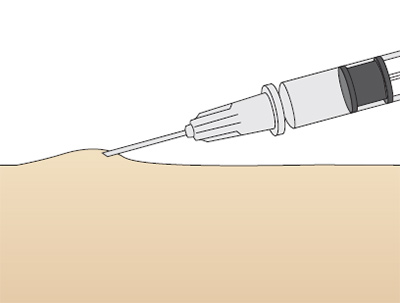
Кожа над местом введения собирается в складку, игла под углом 45° вводится в кожу, затем плавно в подкожно-жировую клетчатку вводится раствор лекарственного препарата.
Внутривенные инъекции
Внутривенные инъекции предусматривают введение лекарственного вещества непосредственно в кровяное русло. Наиболее важным правилом при этом является строжайшее соблюдение правил асептики (мытьё и обработка рук, кожи больного и т. п.).
Особенности строения вен
Для внутривенных инъекций чаще всего используют вены локтевой ямки, поскольку они имеют большой диаметр, лежат поверхностно и сравнительно мало смещаются, а также поверхностные вены кисти, предплечья, реже вены нижних конечностей. Теоретически, внутривенная инъекция может быть произведена в любую из вен человеческого организма. Также аналогом внутривенной инъекции является введение препарата через диафрагму рта в корень языка. Это связано с особенностями анатомического строения языка человека.
Подкожные вены верхней конечности — лучевая и локтевая подкожные вены. Обе эти вены, соединяясь по всей поверхности верхней конечности, образуют множество соединений, самое крупное из которых — средняя вена локтя, наиболее часто используемая для пункций. В зависимости от того, насколько чётко вена просматривается под кожей и пальпируется (прощупывается), выделяют три типа вен:
- Хорошо контурированная вена. Вена хорошо просматривается, чётко выступает над кожей, объёмна. Хорошо видны боковые и передняя стенки. При пальпации прощупывается почти вся окружность вены, за исключением внутренней стенки.
- Слабо контурированная вена. Очень хорошо просматривается и пальпируется только передняя стенка сосуда, вена не выступает над кожей.
- Не контурированная вена. Вена не просматривается, и очень плохо пальпируется, или вена вообще не просматривается и не пальпируется.
По степени фиксации вены в подкожной клетчатке выделяют следующие варианты:
- Фиксированная вена — вена смещается по плоскости незначительно, переместить её на расстояние ширины сосуда практически невозможно.
- Скользящая вена — вена легко смещается в подкожной клетчатке по плоскости, её можно сместить на расстояние больше её диаметра. При этом нижняя стенка такой вены, как правило, не фиксируется.
По выраженности стенки можно выделить следующие типы:
- Толстостенная вена — вена толстая, плотная.
- Тонкостенная вена — вена с тонкой, легко ранимой стенкой.
Используя все перечисленные анатомические параметры, определяют следующие клинические варианты:
- хорошо контурированная фиксированная толстостенная вена — такая вена встречается в 35 % случаев;
- хорошо контурированная скользящая толстостенная вена — встречается в 14 % случаев;
- слабо контурированная, фиксированная толстостенная вена — встречается в 21 % случаев;
- слабо контурированная скользящая вена — встречается в 12 % случаев;
- неконтурированная фиксированная вена — встречается в 18 % случаев.
Наиболее пригодны для пункции вены первых двух клинических вариантов. Хорошие контуры, толстая стенка позволяют довольно легко пунктировать вену.
Менее удобны вены третьего и четвёртого вариантов, для пункции которых наиболее подходит тонкая игла. Следует только помнить, что при пункции «скользящей» вены её необходимо фиксировать пальцем свободной руки.
Наиболее неблагоприятны для пункции вены пятого варианта. При работе с такой веной применяют предварительную пальпацию (прощупывание), пункция «вслепую» не рекомендуется.
Осложнения при внутривенных инъекциях
Одной из наиболее часто встречающихся анатомических особенностей вен является так называемая ломкость. Визуально и пальпаторно ломкие вены ничем не отличаются от обычных. Пункция их, как правило, также не вызывает затруднения, но в месте прокола очень быстро появляется гематома, которая нарастает, несмотря на то, что все приёмы контроля подтверждают правильное попадание иглы в вену. Считается, что, вероятно, происходит следующее: игла является ранящим агентом, и в одних случаях прокол стенки вены соответствует диаметру иглы, а в других из-за анатомических особенностей происходит разрыв по ходу вены.
Нарушения техники фиксации иглы в вене также могут привести к осложнениям. Слабо фиксированная игла наносит дополнительную травму сосуду. Данное осложнение встречается, почти исключительно, у лиц пожилого возраста. При данной патологии введение лекарственного средства в эту вену прекращают, пунктируют другую вену и проводят инфузию, обращая внимание на фиксацию иглы в сосуде. На область гематомы накладывают тугую повязку.
Довольно частым осложнением бывает поступление инфузионного раствора в подкожную клетчатку. Наиболее часто после пункции вены в локтевом сгибе недостаточно устойчиво фиксируется игла, при движении больного рукой игла выходит из вены и раствор поступает под кожу. Иглу в локтевом сгибе рекомендуется фиксировать не менее чем в двух точках, а у беспокойных больных фиксировать вену на протяжении конечности, исключая область суставов.
Другая причина поступления жидкости под кожу — сквозной прокол вены, это чаще бывает при применении одноразовых игл, более острых, чем многоразовые, в этом случае раствор поступает частично в вену, а частично под кожу.
В случае нарушения центрального и периферического кровообращения вены спадаются. Пункция подобной вены крайне сложна. В этом случае больного просят более энергично сжимать и разжимать пальцы и параллельно похлопывают по коже, просматривая вену в области пункции. Как правило, этот приём более или менее помогает при пункции спавшейся вены. Первичное обучение медперсонала на подобных венах недопустимо.
Внутривенное капельное введение растворов: выбор системы и проведения процедуры
Чтобы пациенты смогли получить большую дозу лекарственных средств, в медицине долгое время практикуется техника введения препаратов внутрь вены. Даная методика имеет весомые достоинства:
- Во-первых, лекарство попадает в кровяное русло, не меняя состав и свойства.
- Во-вторых, обеспечивается точность дозировки.
- В-третьих, достигается высокая скорость терапевтического эффекта.
- В-четвертых, активными веществами насыщаются все ткани. В особенности это относится к органам, которые обильно пронизаны сосудами.
Введение лекарств в вену врачи назначают больным в тех случаях, когда лекарственные вещества не всасываются в кишечнике либо обладают сильным местнораздражающим эффектом.
Показания и противопоказания
При помощи венепункции снимаются признаки интоксикации организма, восстанавливается количество кровяных клеток. Кроме того, равновесие электролитов и кислотно-щелочной баланс приходят в норму. В список показаний можно включить обеспечение парентерального питания, обеспечение общей анестезии.
Процедура выполняется с использованием шприцев, если количество разового приема лекарства небольшое. При больших дозировках обычно назначается капельница (система) со скоростью подачи от 20 до 60 капель за минуту.
Но при всех неоценимых достоинствах присутствуют противопоказания, которые нельзя игнорировать. В частности повреждение кожи, а также подкожно-жировой клетчатки в месте укола. Другой случай – флебит кровеносного сосуда. При выявлении противопоказаний прокол делается в другую вену.
Внутривенное введение капельницы
Оптимальный выбор
При выборе той или иной системы первым делом обратить внимание на размеры ячеек фильтрующего элемента. Микронабор может иметь маркировку:
- «ПК» – ячейки крупного размера, чтобы пропускать цельную кровь, компоненты и препараты крови, кровезаменители.
- «ПР» – диаметр ячеек не превышает 15 микрон. Такой фильтр пропускает аминокислоты, моносахариды, электролиты. Вредные взвеси не пройдут через фильтр в кровяное русло. Для полезных веществ не создается препятствий.
Другой не менее важный критерий – это материал изготовления игл, а также их диаметр. В случае назначения длительного курса или частых процедур выбрать полимерные наконечники с катетерами. При использовании емкостей из стекла, которые закрываются резиновыми пробками, нужно выбирать металлические наконечники.
Касательно диаметра игл – маркировка также устроена по-своему. Параметр в сторону увеличения обозначается по убывающей, а чем показатель меньше, тем больше цифра. Обозначение толстого острия для оказания первой помощи при шоковых состояниях – 14, а детского – 22.
Необходимая оснастка
Вначале готовится манипуляционный столик – накрывается стерильной пленкой. Потребуется два лотка – в одном будут находиться стерильные инструменты с материалами, во втором – все отработанное. Помимо специального набора понадобятся шарики из ваты, ножницы, перчатки, пинцет.
Чтобы подвесить емкость с лекарством, нужен штатив, но дома вместо него подойдут переносные, а также разборные аналоги или приспособления. К примеру, подойдет обычная пластиковая бутылка с крючком, за который она подвешивается. Также потребуется жгут для перетяжки сосуда, пластырь, а под локоть нужно положить скатанную подушку либо валик. Для дезинфекции подойдет Этиловый спирт (70%).
Подготовительный этап
Чтобы инъекция прошла максимально безопасно, медицинский персонал должен придерживаться четких инструкций. В частности речь идет о соблюдении правил асептики. Подготовительный этап выполняется в процедурном кабинете:
- Проверка. Комплектующие осматриваются на предмет герметичности и срока годности. Убедиться в наличии колпачков на иголках. При выявлении завершения срока действия запрещается его использовать. То же самое относится к нарушению герметичности.
- Обеспечение стерильности. Перед открытием упаковки медицинский работник моет руки с мылом, а после надевает перчатки. Далее нужно постелить на столе стерильную пленку. Пакет с оснасткой вытереть салфеткой либо шариком из ваты, предварительно смоченными в спирте, потом вскрыть его, разложить все компоненты на застеленном столе.
- Проверка лекарственных препаратов. Провести осмотр флакона, где должна присутствовать этикетка с названием вещества и сроком годности. Стоит встряхнуть емкость, чтобы определить, поменяется вид раствора либо нет. При необходимости внести дополнительно несколько препаратов, проверяются ампулы на предмет пригодности, а также соответствия названий согласно рецепту. При малейшем расхождении по какому-либо пункту от процедуры необходимо отказаться.
- Распаковка флакона. Смочить ватный шарик спиртом, затем протереть алюминиевый колпачок флакона, после чего снять. Под ним находится резиновая пробка, которую тоже протереть смоченным спиртом шариком.
- Подготовка игл. С острия воздуховода снимается защитный колпачок, потом оно вводится в резиновую пробку до конца. Протирать ее предварительно спиртом не требуется, если на этапе вскрытия набора она была простерилизована. То же самое относится к иголке инфузионной трубки. Убедиться, что роликовый зажим находится в положении «закрыто». Емкость с лечебным раствором переворачивается и фиксируется на штативе.
- Манипуляция с капельной камерой. Сдавить два раза – она должна наполниться жидкостью наполовину. Для выпуска воздуха из трубки открывается зажим. Далее снимается колпачок с другого наконечника, чтобы система начала заполняться раствором из основного флакона. Когда воздух полностью вытиснится, закрывается зажим и на иголку надевается колпачок. Теперь система готова к дальнейшему применению.
Введение лекарства в вену выполняется только согласия пациента либо его близких. То есть предварительно берется их согласие.
Алгоритм выполнения
Для начала больному принять удобное лежачее положение, поскольку определенный промежуток времени ему придется лежать и не двигать рукой. До крепления капельницы игла вводится в вену. Желательно выбирать темные кровеносные сосуды для легкого контроля процесса. В частности это срединная либо медиальная вена. К ним хорошо фиксируются катетеры. В редких случаях медперсонал выбирает сосуды ладони с внешней стороны.
Чтобы можно делать больше одного укола, первый ставится вблизи кисти. Для следующей венепункции выбирать другую точку, поскольку повторный прокол в то же место неизбежно заканчивается серьезным повреждением стенки сосуда.
Когда кровеносный сосуд выбран, на руку накладывается жгут выше точки укола, после чего затянуть до прекращения пульсации вен. Для максимального разгибания локтя под него лучше положить небольшую подушку. В целях создания искусственного венозного застоя пациента просят «поработать кулачком».
Перед процедурой медицинский персонал должен надевать перчатки. Кожу в месте прокола необходимо обработать спиртом не менее трех раз:
- зона вокруг места укола;
- малая область;
- непосредственная зона прокола.
Такая обработка позволяет получить необходимое обеззараживание на участке прокола.
На следующем этапе с иглы снять колпачок, острие разворачивается срезом кверху. Левым большим пальцем фиксируется вена для обездвиживания. Острие вводится под наклоном в 30-45°. В канюле должна появиться кровь, пластиковая головка закрывается стерильным шариком, снимается жгут. Теперь можно открыть зажим и слить несколько капелек, затем система подсоединяется к канюле. Положение металлического наконечника фиксируется на руке лейкопластырем.
Емкость с лекарственной жидкостью, а также капельная камера должна располагаться сверху нижней канюли системы. Иначе в вену попадет воздух, чего следует избегать. Скорость поступления препарата регулируется зажимом. Во время внутривенного капельного вливания ведется наблюдение за пациентом и капельницей. При необходимости ввести дополнительные вещества прокалывается инфузионная трубка. Но перед этим продезинфицировать место укола.
Завершение инъекции
Когда процедура будет завершена, нужно закрыть зажим, убрать лейкопластырь, потом закрыв куском ватки точку венепункции, вытащить иглу. Далее пациенту следует согнуть руку, не забыв удерживать ватный шарик (3-5 минут будет достаточно).
Далее система отсоединяется от флакона. Трубка разрезается ножницами – она хранится отдельно от иголок, чтобы соблюсти правила инфекционной безопасности. Напоследок в специальном журнале делается соответствующая запись.
Возможные осложнения
В ходе внутривенных инъекций может возникнуть ряд различных осложнений:
- Спазмирование вены – риск связан с повреждением противоположной стенки кровеносного сосуда, из-за чего в паравазальную область начинает проникать кровь и лекарственный раствор. В месте входа иглы образуется гематома, а ряд медикаментов способен вызывать местное раздражающее воздействие на ткани рядом с сосудами.
- Экстравазация – околососудистое пространство наполняется большим количеством препарата. Это явный факт нарушения техники инъекции со стороны персонала, что может привести к некрозу тканей (тяжелое осложнение).
- Флебит – процесс воспаления стенок вен от вводимых раздражающих веществ. В поврежденном сосуде могут образоваться тромбы. – это прямое следствие несоблюдение правил антисептики и асептики в ходе процедуры.
- Эмболия – бывает жировая и воздушная. Первый тип возникает при попадании жира в кровяное русло. Воздушная эмболия является следствием попадания пузырьков воздуха в кровоток, что указывает на нарушения подготовки, а также постановки системы.
- Пирогенность – ответная реакция организма на просроченные лекарства либо вследствие индивидуальной непереносимости больного на некоторые активные вещества. Это ведет к резкому повышению температуры либо ознобу. Если медицинский работник быстро вводит раствор, у пациента начинается головокружение, нарушается ритм работы сердца, вплоть до коллапса.
- Аллергические проявления – также ответная реакция организма на непереносимость вводимых препаратов. Это приводит к кожной аллергической реакции, сыпи, зуду, включая и тяжелые случаи.
При выявлении локальных последствий больным оказывается лечение местного характера – йодные сетки, компрессы. При тяжелых осложнениях процесс незамедлительно прекращается, а пациентам персонал оказывает неотложную помощь.
Внутривенная инъекция – это частая и ответственная процедура в медицине и поэтому персонал должен обладать соответствующей квалификацией. Иначе все может закончиться разными осложнениями, вплоть до тяжелых последствий.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Введение лекарств в барабанную полость
Транстимпанальное введение лекарственных препаратов – это способ доставки медикаментозных средств в пораженную область через перфорацию в барабанной перепонке.
Транстимпанальный способ закапывания лекарственных средств в ухо эффективно применяется при лечении серозного отита (для подачи антибиотиков), сенсоневральной тугоухости (для внесения глюкокортикоидов), а также других болезней уха. Эффективный транстимпанальный метод и в ситуациях, когда отсутствует возможность транспортировать активную лекарственную субстанцию к барабанной полости сквозь евстахиеву трубу. Благодаря этому способу упрощается проникновение препарата в место поражения.
Манипуляция транстимпанального введения медикаментов безболезненна, поскольку проводится под местным обезболиванием. Она создаёт наилучший лечебный результат по сравнению с местным внесением лекарственных средств посредством турунд либо в виде капель. Соответствующие лекарственные препараты вносятся в барабанную полость с помощью шприца по факту преждевременного бережного очищения слухового прохода.
Суть манипуляции
Изначально больного подготавливают к тимпанопункции. В случае диагностирования разрыва мембраны барабанной перепонки патологическую жидкость из неё аспирируют длинной утончённой иглой. В дальнейшем производят замену шприца и последующее введение в барабанную полость подогретого до 36,6 °С лекарственного раствора. В случае имеющихся естественных отверстий в барабанной перегородке лекарственное средство вводится в ухо после выявления участка воздействия. В редких случаях доктора создают искусственные отверстия (перфорации). Чтобы предотвратить вестибулярные реакции после подачи в ухо медикамента пациенту рекомендуется отдых.
Когда используется транстимпанальный метод введения лекарств?
Чаще всего к транстимпанальному способу подачи лекарственных препаратов прибегают при необходимости лечения экссудативной разновидности отита среднего уха. Признаками данного заболевания являются:
- снижение функции слуха;
- тиннитус (шумы) при наклонах и резких поворотах головы;
- чувство распирания, тяжести, заложенности;
- одностороннее восприятие слуха;
- серозно-гнойные выделения;
- слабоинтенсивные болевые ощущения.
В случае проявления какого-либо из выше перечисленных симптомов следует обратиться за консультацией к лор-специалисту. Если запустить болезнь и своевременно не начать лечение, патология может перейти в хроническую стадию. Одной из наиболее распространённых и неоднократно возникающих патологий при отсутствии обращения к врачу за помощью в случае заболеваний ушей является снижение слуха. Воспалительный процесс в среднем ухе приводит к неизлечимой глухоте, а также тормозит речевую функцию у детей.
- серозный отит;
- болезнь Меньера;
- острая сенсоневральная тугоухость.
При лечении серозной формы отита в барабанную полость вводят антибиотики. При нейросенсорной тугоухости – кортикостероиды. Оптимальную частоту введения лекарственных средств, их дозировки подбирает врач исходя из диагноза пациента.
Методика процедуры
Существует несколько методик интратимпанального введения лекарственных средств – при помощи инъекции, через шунт или постоянный катетер. Эффективность процедуры не зависит от пути введения препарата. Простейший способ – инъекция. Такая манипуляция проводится амбулаторно.
Специализированной подготовки не требуется. Пациент ложится на кушетку. Врач должен иметь свободный доступ к пораженному уху.
- Обеззараживание барабанной перепонки раствором антисептика по выбору врача.
- Обезболивание – с использованием препаратов для обработки слухового прохода либо подкожных инъекций анестетиков. Препаратами выбора являются раствор фенола, раствор лидокаина, крем «EMLA» местно в виде аппликации.
- Перфорация барабанной перепонки и удаление гнойного или серозного содержимого.
- Введение препарата, подогретого до температуры тела. Объем лекарственного средства составляет от 0,5 до 0,8 мл.
После процедуры пациент должен оставаться в положении лежа 15–30 минут. Это снижает риск развития головокружения, дезориентации в пространстве.
Схема введения медикаментов в барабанную полость
Накануне осуществления манипуляции проводится подготовка. Врач осматривает пациента, составляет анамнез. Следующим шагом является оценка состояния мембраны барабанной перепонки (выполняется проверка её реакции в ответ на звуковые волны).
При необходимости проведения транстимпанального метода впрыскивания препарата следует обеспечить беспрепятственный доступ к повреждённому уху. Больной располагается на кушетке. Ушная полость обрабатывается антисептиком и противовоспалительной субстанцией, после чего обезболивается. Как только начинается действие анестетика, производится перфорация барабанной перепонки. Накопленное полостное содержимое выводится наружу сквозь истончённую иглу. Вход в слуховое отверстие тщательно очищается. По окончанию очищения слуховой проход прикрывают ватным тампоном, пропитанным адреналином, и закапывают в него дезинфицирующий фенольный раствор. Поэтапное выполнение данной процедуры позволяет достичь эффекта полного обезболивания. Затем в барабанную полость шприцом подаётся лекарство. Во избежание головокружения пациенту рекомендуется оставаться несколько минут в лежачем положении.
ВАЖНО! Процедура транстимпанального введения медикаментов в ухо должна проводиться лишь опытным врачом. Специалист подбирает лекарственное средство, учитывая общее состояние здоровья пациента и индивидуальные особенности его организма. Обращаясь за помощью в медицинское учреждение, человек максимально минимизирует вероятность возникновения каких-либо осложнений.
Для чего нужна данная процедура?
Транстимпанальная процедура внесения медицинских препаратов в барабанную полость проводится с терапевтической целью при устранении патологий острой, хронической форм среднего отита, иных болезней ушей, а также с целью подачи в полость уха контрастного вещества накануне рентгенографического исследования, анализа дренажной функции слуховых труб.
Внесение в ухо лекарств посредством прокола барабанной перепонки обеспечивает лучшую результативность в лечении гнойной формы отита. Как правило, это заболевание сопровождается сильной болью, лихорадкой, ознобом, внешним изменением форм барабанной полости. В подобных ситуациях возникает высокая вероятность интоксикации организма и развития осложнений. С целью купирования патологии показан ввод медикаментов (антибиотиков) непосредственно внутрь барабанной полости.
Ограничения после транстимпанального введения в барабанную полость уха лекарств
После назначенного лечения следует исключить вертикальное использование наушников, пребывание на сквозняке, посещение бани, бассейна. Также стоит воздержаться от переохлаждения.
Для быстрого восстановления врач рекомендует общеукрепляющие медикаменты и комплексные витамины. В некоторых случаях очень эффективна физиотерапия.
Прокол барабанной перепонки с целью введения лекарственных препаратов в большинстве случаев назначают однократно. При тяжелых формах заболеваний ушей может потребоваться выполнить тимпанопункцию повторно. Постманипуляционные осложнения возникают крайне редко, в основном они связаны с неправильным проведением процедуры.
Осложнения местной анестезии
Осложнения местной анестезии – это ежелательные реакции, возникающие в результате введения местных анестезирующих препаратов. В зависимости от вида осложнения у пациента могут отмечаться такие симптомы, как удушье, нарушение гемодинамики и внутрисердечной проводимости, изменения со стороны ЦНС, кожная сыпь. Диагноз устанавливается на основании анамнеза и клинических проявлений, в отдельных случаях назначается ЭКГ, КТ, рентгенография, УЗИ. Специфическое лечение включает введение антигистаминных средств и кортикостероидных гормонов, инфузионную терапию, прекращение использования анестетика. В тяжелых случаях требуется реанимационное пособие.
МКБ-10
Общие сведения
Опасные реакции на введение местноанестезирующих средств достаточно распространены. Частота их встречаемости составляет 1 случай на 150-200 использований препаратов этой группы. У 90% больных определяются признаки кожной аллергии (крапивница). Около 6% пациентов отвечают на инъекцию медикамента отеком лица, шеи, дыхательных путей. Анафилактический шок выявляется в 3% случаев. На долю общетоксических реакций, сопровождающихся поражением центральной нервной системы и проводящего аппарата сердца, приходится не более 1%. Зависимость от пола и возраста отсутствует, осложнения одинаково часто обнаруживаются у всех категорий населения. До 70% нежелательных реакций возникает у жителей развитых стран, в странах «третьего мира» аллергия диагностируется значительно реже.
Причины
Основной причиной аллергических реакций является гиперчувствительность к компонентам раствора. Препарат, попавший в организм, трансформируется в неполноценный антиген – гаптен. Далее гаптен образует комплекс с белком и воспринимается организмом как чужеродный агент. Провоцирующим фактором становятся особенности обмена веществ конкретного больного. Биотрансформация препарата может несколько отличаться от нормальной, что приводит к образованию комплексов, вызывающих аллергию. Интенсивность симптоматики зависит от степени сенсибилизации организма. Помимо реакций гиперчувствительности осложнения при введении местных анестетиков возникают по следующим причинам:
- Врачебная ошибка. Включает неправильный выбор обезболивающего или его дозировки, отказ от использования сосудосуживающих веществ в составе лекарственного раствора, нарушение техники манипуляции. Все это преимущественно приводит к токсическому воздействию препаратов на сердце и головной мозг, инфекционным процессам. При неправильном проведении процедуры могут иметь место повреждения нервных стволов, сосудов, других структур.
- Неадекватная реакция. Чрезмерная двигательная активность пациента в ответ на действия специалиста порой становится причиной отлома инъекционной иглы. Подобное чаще происходит с тонкими иглами диаметром 0,6 мм (23G). Кроме того, при резких движениях больного возможна излишняя травматизация мягких тканей, поражение сосудов и нервов (если инфильтрация производится вблизи сосудисто-нервных пучков).
- Длительная анестезия. При необходимости обеспечения продолжительной спинальной анестезии раствор подают в эпидуральное пространство через тонкий катетер. Анестетик депонируется вокруг нервов, его концентрация становится токсической. Развивается стойкий неврологический дефицит – синдром конского хвоста. Одномоментное введение большой дозы препарата провоцирует тотальную спинальную анестезию с двигательной блокадой и угнетением продолговатого мозга.
Патогенез
Патогенез негативных последствий местной анестезии различается по типам нежелательных явлений. При аллергиях отмечается чрезмерная активизация иммунных механизмов, которая приводит к развитию неадекватных по силе защитных процессов. Эти процессы провоцируют региональную пролиферацию жидкости из сосудистого русла, расстройства гемодинамики (анафилактический шок), гиперемию кожи на отдельных участках. Токсические реакции характеризуются нарушением поляризации и деполяризации клеток, изменением работы клеточных натриевых каналов. Токсическое действие на ЦНС заключается в нарушении проводимости нервных импульсов за счет прекращения их передачи в ганглиях нервной системы. Инфекционные осложнения возникают как результат попадания в рану и размножения патогенной флоры, с которой организм не может справиться самостоятельно.
Классификация
Осложнения местной анестезии могут систематизироваться по причинам, однако такой способ деления более важен при профилактике патологических состояний, а не в случаях, когда необходимо купировать уже развившуюся реакцию. Для устранения последствий манипуляции необходимо четкое понимание процессов, происходящих в организме больного, поэтому наиболее используемой является классификация по типу нежелательных явлений и их распространенности:
- Поражение ЦНС. Диагностируется как при всасывании большого количества анестетика из места его введения, так и при ошибочном внутрисосудистом вливании. Характеризуется тяжелыми нейротоксическими явлениями, может быть спинальным и церебральным. При спинальной разновидности патологии отмечается тотальное угнетение рефлекторных дуг, работы продолговатого мозга. Церебральная интоксикация приводит к нарушению сознания, коммуникативных функций, координации.
- Поражение проводящей системы. Особенно часто наблюдается при использовании высоких доз мекаина, лидокаина. Эти препараты подавляют электрическую активность сердца, в токсических дозах замедляют AV-проводимость, усугубляют атриовентрикулярную блокаду при ее наличии. Все перечисленное может стать причиной брадикардии и нарушений сердечного ритма вплоть до остановки сердца.
- Аллергии. Протекают в виде крапивницы, ангионевротического отека, анафилактического шока. Последний считается наиболее тяжелой формой гиперчувствительности к препарату. Иногда аллергия на м/а развивается в виде неспецифических явлений: головокружения, общего ухудшения самочувствия, незначительного угнетения дыхания, вариативной кожной сыпи.
- Травматизация. Возникает при нарушении техники процедуры или резких движениях пациента. При повреждении нервного ствола определяется выраженный болевой синдром, нарушение функции конечности. При попадании в кровеносный сосуд формируется гематома. Возможно появление контрактур, участков ишемии кожи, явлений парестезии.
- Инфекционные осложнения. Могут протекать в виде регионального воспаления, абсцесса, флегмоны мягких тканей. Наиболее тяжелой разновидностью является систематизированный септический процесс (сепсис), относящийся к жизнеугрожающим состояниям и требующий экстренной госпитализации. При остальных бактериальных процессах обычно показано амбулаторное лечение, которое может быть консервативным или оперативным.
Симптомы
Аллергическая реакция в форме крапивницы сопровождается образованием множества красных пятен, несколько возвышающихся над неизмененными участками кожи. Отмечается выраженный зуд. При ангионевротическом отеке наблюдается одностороннее или двухстороннее увеличение размера ушей, губ, мягких тканей лица. Наиболее опасен АНО дыхательных путей, который проявляется в форме удушья, инспираторной одышки, свистящего дыхания, лающего кашля, акроцианоза губ, мочек ушей, ногтей. При отсутствии своевременной помощи развивается выраженная системная гипоксия, больной погибает от недостатка кислорода. К числу симптомов анафилактического шока относят бледность или мраморность кожи, резкое снижение АД, тахикардию, расширение зрачков, нарушение сознания, чувство удушья.
При поражении ЦНС наблюдаются головокружения, судороги, звон в ушах, металлический привкус во рту. Может выявляться нистагм, нарушения речи, головокружения, тремор, онемение полости рта, языка. Реакция со стороны ССС включает брадикардию, аритмию, расширение периферических сосудов, снижение АД, коллапс. Возможна фибрилляция и асистолия. Типичным симптомом травматизации сосудов является быстрое увеличение гематомы в пораженной области. При пальпации обнаруживается умеренная болезненность, отек. Попадание иглы в нервный ствол провоцирует резкий приступ боли, иррадиирующей по ходу поврежденной структуры. Впоследствии у некоторых больных отмечается тугоподвижность конечности, боли в спине, локальное нарушение чувствительности.
Для инфекционных процессов характерна местная и общая симптоматика. Местными симптомами являются отек тканей, локальная гиперемия, повышение температуры тела в области воспаления. При накоплении гноя определяется флюктуация, визуально в очаге может просматриваться беловатая зона (скопление гнойных масс). К системным проявлениям относят общую гипертермию, ухудшение самочувствия, боли в мышцах и костях, изменение психоэмоционального фона. При тяжелых процессах наблюдается угнетение сознания, бред, судороги. Развивается инфекционно-токсический шок, приводящий к централизации кровообращения, нарушению гемодинамики, гибели пациента.
Диагностика
Обычно осложнения развиваются вскоре после введения препарата, поэтому их диагностику осуществляет лечащий врач, чаще всего хирург или анестезиолог-реаниматолог. Отсроченные последствия (инфекция) могут быть выявлены поликлиническим хирургом или врачом общей практики при обращении пациента в поликлинику. В большинстве случаев тип и характер патологии определяется с учетом анамнеза и внешних признаков. Иногда для подтверждения диагноза требуется проведение лабораторных и инструментальных исследований. К числу диагностических методик относятся:
- Сбор анамнеза, осмотр. Врач выясняет, какие вмешательства выполнялись в недавнем прошлом, какой анестетик использовался. Если постановкой диагноза занимается специалист, проводивший манипуляцию, этот пункт исключают. При осмотре выявляют характерные клинические признаки того или иного патологического состояния.
- Лабораторные анализы. При инфекционных процессах в крови больного обнаруживают лейкоцитоз, увеличение СОЭ. При токсическом влиянии анестетика может отмечаться сдвиг pH в кислую сторону, поскольку водородный показатель анестетиков колеблется от 3,5 до 6 единиц. Тяжелые нарушения работы сердца приводят к росту активности КФК, КФК МВ, появлению специфических маркеров. При аллергии в крови увеличивается содержание иммуноглобулинов.
- Инструментальное обследование. При аллергии не назначается. Признаки поражения ЦНС требуют исключения органических заболеваний путем проведения компьютерной томографии. На ЭКГ определяют AV-блокаду, брадикардию. При гнойных процессах может потребоваться сонография, рентгенография, КТ для уточнения границ воспалительного очага.
Лечение осложнений местной анестезии
При крапивнице пациенту назначают системные антигистаминные препараты. Как правило, этого оказывается достаточно для устранения проявлений болезни. Отек дыхательных путей требует внутривенного вливания кортикостероидов, оксигенотерапии. В тяжелых ситуациях прибегают к экстренной коникотомии или трахеостомии для обеспечения проходимости дыхательных путей. При анафилактическом шоке показана инфузионная терапия с использованием коллоидных растворов, введением кардиотоников для поддержания работы сердца и артериального давления. Применяются гормональные, антигистаминные средства, адреналин.
При нарушениях деятельности ЦНС рекомендуются противосудорожные препараты. При необходимости больного вводят в наркоз с использованием инъекционных средств. Осуществляют дыхательную поддержку вплоть до ИВЛ. Для ускорения экскреции анестетика производят объемные инфузии солевых растворов с последующим введением петлевых диуретиков. Реакции со стороны сердца купируют с помощью атропина, прессорных аминов. При фибрилляции проводят химическую или электрическую дефибрилляцию. При остановке сердца показана сердечно-легочная реанимация.
При инфекционных осложнениях назначают антибактериальные средства. Выполняют санацию патологического очага с его вскрытием, удалением гнойных масс, установкой дренажей. Для устранения болевого синдрома применяют ненаркотические анальгетики. Под окклюзионную повязку накладывают противомикробные и ранозаживляющие мази. Гематомы, образующиеся при повреждении сосуда, обычно не требуют вмешательства, при сдавлении соседних анатомических структур осуществляют удаление скопившейся крови. При травмах нервных стволов используют препараты для улучшения нервно-мышечной проводимости, физиотерапию.
Прогноз и профилактика
Прогноз при большинстве реакций благоприятный, при своевременно оказанной помощи негативные явления удается полностью устранить. Гибель или инвалидизация возможна при развитии анафилактического шока, отека Квинке, брадиаритмии вне стен лечебного учреждения. Тяжелые осложнения инфекционных процессов наблюдаются крайне редко. Профилактика заключается в правильном подборе вида и дозы анестетика, владении техникой манипуляции, информировании пациента о целях и ходе процедуры. Необходимо строго соблюдать правила асептики и антисептики. Больному следует заранее сообщить врачу о наличии аллергии на лекарственные препараты, максимально сдержанно вести себя во время вмешательства, избегать резких движений.
2. Местные осложнения при проведении местной инъекционной анестезии/ Чудаков О.П., Максимович Е.В. — 2012.
Этот вид медицинской манипуляций осуществляется в условиях дневного стационара нашего центра.
Показания к подкожному введению лекарственных средств

В некоторых ситуациях это может оказаться преимуществом. Небольшие порции лекарства плавно всасываются из подкожного слоя в кровь. Благодаря этому обеспечивается продолжительное действие, но без передозировок. В качестве примера можно привести инсулин. Быстрое поступление этого препарата чревато грозным осложнением – гипогликемией, резким падением уровня сахара крови. А при подкожном введении инсулин действует сравнительно медленно, и постепенно снижает сахар.
Вводим подкожно мы и масляные растворы, предварительно подогретые до температуры человеческого тела. Правда, объем вводимых подкожно средств ограничен. Инъекции больших объемов свыше 5 мл чреваты возникновением инфильтратов и их последующим инфицированием.
Нельзя подкожно вводить раздражающие средства и препараты, вызывающие спазм капилляров и некроз кожи. В этой связи запрещены растворы кальция хлорида, норадреналина. А вот адреналина гидрохлорид в качестве неотложной помощи подкожно мы вводим. В любом случае, выбирает средства для инъекций под кожу и определяет показания к ним врач нашего центра.
Методика подкожного введения лекарственных препаратов

Инъекция может осуществляться в обширные участки тела на спине, животе, голенях, бедрах, ягодицах. Но самое удобное место – верхняя треть наружной поверхности плеча. Это место обрабатывается антисептиком.
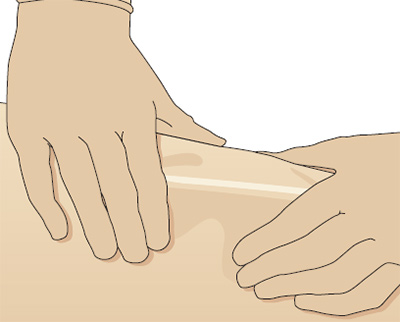
Здесь медсестра формирует треугольную складку. Для этого она захватывает кожу большим и указательным пальцами. Эти пальцы соответствуют сторонам получившегося треугольника, а его основание – месту для инъекции.
Укол делается под углом 40-450 к поверхности кожи. При этом игла погружается в кожу на 23 ее длины. После этого медсестра, плавно надавливая на поршень, вводит препарат. Затем игла извлекается, и место укола вновь обрабатывается антисептиком. Во избежание гематомы пациент в течение нескольких минут прикладывает смоченный антисептиком тампон к месту укола.
В зависимости от показаний врач может назначить подкожные инъекции однократно или многократно, курсом. Назначения и отметки об их исполнении отображаются в медицинской документации.
Возможные осложнения после подкожной инъекции
Важно помнить, что любое инъекционное введение лекарственных средств должно быть выполнено медицинским специалистом, владеющим определенными навыками! Самостоятельное выполнение инъекций приводит к возникновению нежелательных осложнений:
1. Инфильтрата – болезненного уплотнения в подкожно-жировой клетчатке на месте укола, которое возникает спустя 2-3 дня в результате:
- несоблюдения требований асептики – использования нестерильного инструментария либо недостаточной обработки кожных покровов;
- превышения максимального объема подкожной инъекции;
- многократного введения препаратов в одно и то же место;
- гиперчувствительности тканей пациента к действующему веществу медикаментозного средства (чаще всего это явление характерно для некоторых антибактериальных препаратов и не подогретых до оптимальной температуры масляных растворов).
Для устранения инфильтрата необходимо наложить гепариновую мазь, йодную сеточку либо согревающий полу-спиртовой компресс. Также пациенту назначают курс физиотерапевтических процедур.

3. Аллергической реакции – неадекватного ответа иммунной системы на вводимое лекарство. Может протекать в легкой форме (в виде заложенности носа, зудящих высыпаний на коже, гиперемии и отечности век) и тяжелой, сопровождающейся бронхо-спазмом, отеком Квинке, анафилактическим шоком. Чтобы предотвратить появление лекарственной аллергии, перед непосредственным введением препарата у пациента выясняют наличие повышенной чувствительности к каким-либо веществам.
4. Флегмоны – разлитого гнойного воспаления клетчаточных пространств, которое возникает при:
- нарушении требований асептики и антисептики;
- не пролеченном инфильтрате.
В этом случае пациенту требуется помощь врача-хирурга.
5. Подкожных кровоизлияний – следствия проникновения в подкожную клетчатку кровяного пигмента из поврежденного сосуда (чаще всего это происходит при использовании во время инъекции деформированной или тупой иглы). Чтобы избежать данного негативного эффекта следует приложить к месту укола стерильную салфетку, смоченную 70% медицинским спиртом, а спустя какое-то время – сделать полу-спиртовой компресс.
6. Повреждения нервных стволов – результата неправильного выбора места подкожной инъекции, при котором вблизи нерва создается депо лекарственного средства. Данное осложнение становится причиной пареза или паралича, лечебные мероприятия будут зависеть от клинических проявлений и тяжести их течения.
7. Формирования участка липо-дистрофии – рассасывания подкожно-жировой клетчатки. Как правило это является следствием инсулинотерапии – длительных инъекций в одно и то же место. Для профилактики подобного осложнения необходимо вводить инсулин комнатной температуры и чередовать места уколов. Лечебные мероприятия заключаются во введении в участки патологически измененной жировой ткани 4-8 ЕД раствора Суинсулина, обладающего антидиабетической активностью.

9. Медикаментозной эмболии – очень тяжелого осложнения подкожной инъекции, спровоцированного нарушением техники ее проведения. Чаще всего может возникнуть в том случае, если медицинская сестра введет в сосуд масляный раствор (при попадании в него масла происходит закупорка). У пациента появляется синюшность кожных покровов, кашель, чувство сдавленности в грудной клетке и приступ одышки, прогрессирование патологического состояния может привести к летальному исходу. Лечение эмболии симптоматическое.
10. Периостита – воспаления надкостницы, возникающего вследствие неправильного выбора места инъекции, нарушения ее техники, поломки иглы (при использовании старого изношенного или дефектного инструментария, резком сокращении тканей во время укола), плохо рассасывающегося инфильтрата.
Преимущества выполнения подкожных инъекций в МКЦ «Проксима
Подкожно-жировой слой характеризуется наличием густой сосудистой сети, именно поэтому медикаментозные средства, введенные подкожно оказывают более быстрое действие по сравнению с пероральным приемом – препараты минуют пищеварительный тракт и сразу попадают в кровяное русло. Подкожные инъекции выполняются иглой самого малого диаметра, вводится не более 2,0 мл лекарственного средства. Чтобы избежать негативных эффектов от инъекций, необходимо довериться настоящим профессионалам! В клинике «Проксима» работают высококвалифицированные медсестры, имеющие многолетний практический опыт. Чтобы записаться на подкожные манипуляции, позвоните нам по телефону, указанному в разделе «Контакты» или оставьте на сайте заявку.
Версия для печати
Безопасная техника инъекций
Safe injection techniques
Article 498. Workman B (1999) Safe injection techniques. Nursing Standard. 13, 39, 47-53.
В данной статье Barbara Workman описывает правильную методику внутрикожных, подкожных и внутримышечных инъекций.
Цели и предполагаемые результаты обучения
Поскольку знания о процедурах ежедневной сестринской практики медсестер растут, разумно пересмотреть некоторые рутинные процедуры.
В данной публикации приведен обзор принципов проведения внутрикожных, подкожных и внутримышечных инъекций. Показано, как правильно выбрать анатомическую область инъекции, предусмотреть возможность непереносимости лекарственных препаратов, а также особые потребности пациента, которые могут повлиять на выбор места выполнения инъекции. Освещены аспекты подготовки пациента и кожи, а также особенности оснащения, и способы уменьшения дискомфорта у пациента во время выполнения процедуры.
Основная цель статьи — побудить медицинскую сестру критически пересмотреть собственную технику выполнения инъекций, исходя из принципов медицины, основанной на доказательствах, и обеспечить пациенту эффективную и безопасную помощь.
После прочтения данной статьи медсестра должна знать и уметь следующее:
- Определять безопасные анатомические области для проведения внутрикожных, подкожных и внутримышечных инъекций;
- Определять мышцы — анатомические ориентиры для выполнения внутримышечных инъекций, и объяснять, почему их для этого используют;
- Объяснять, на чем основан тот или иной метод обработки кожи пациента;
- Обсудить способы уменьшения дискомфорта у пациента во время инъекции;
- Описать действия медсестры, направленные на профилактику осложнений инъекций.
Введение
Проведение инъекций — это рутинная, и пожалуй, самая частая работа медсестры, и хорошая техника инъекций может сделать эту манипуляцию относительно безболезненной для пациента. Однако, техническое мастерство без понимания манипуляции подвергает пациента ненужному риску осложнений. Изначально выполнение инъекций было врачебной манипуляцией, но, с изобретением пенициллина в сороковые годы, обязанности медсестры значительно расширились (Beyea and Nicholl 1995). В настоящее время большинство медсестер выполняют эту манипуляцию автоматически. Поскольку сейчас сестринская практика становится основанной на доказательствах, то вполне логично пересмотреть эту фундаментальную процедуру с позиций доказательной медицины.
Лекарственные препараты вводят парентерально потому, что обычно они так всасываются быстрее, чем из желудочно-кишечного тракта, или же, как инсулин, разрушаются под действием пищеварительных ферментов. Некоторые препараты, как например, медокси-прогестерона ацетат или флуфеназин, высвобождаются в течение длительного времени, и требуется такой путь введения, который бы обеспечил постоянное всасывание препарата.
Существуют четыре главных характеристики инъекции: место введения, путь введения, техника инъекции и оснащение.
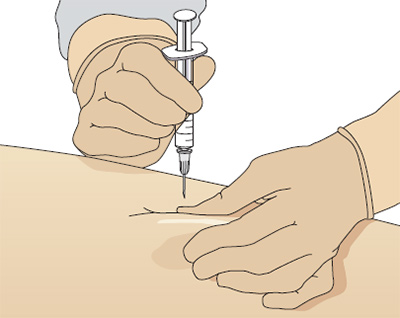
Внутрикожный путь введения
Внутрикожный путь введения предназначен для обеспечения скорее местного, а не системного действия препаратов, и, как правило, применяется в основном для диагностических целей, например аллерготестов и туберкулиновых проб, или для введения местных анестетиков.
Для выполнения внутрикожной инъекции иглу калибра 25G срезом кверху вводят в кожу под углом 10-15°, исключительно под эпидермис и вводят до 0.5 мл раствора, до появления на поверхности кожи так называемой «лимонной корочки» (Рис. 1). Такой путь введения применяется для выполнения аллерготестов, и место инъекции должно быть обязательно отмечено, чтобы отследить аллергическую реакцию через определенный промежуток времени.
Места для выполнения внутрикожных инъекций аналогичны таковым для выполнения подкожных инъекций (Рис. 2), но также их можно выполнять на внутренней стороне предплечья и под ключицами (Springhouse Corporation 1993).
При проведении аллергопроб очень важно обеспечить наличие противошокового набора в ближайшем доступе, если у пациента будет реакция гиперчувствительности или анафилактический шок (Campbell 1995).
Рис. 1. «Лимонная корочка», которая образуется при внутрикожной инъекции.
ВАЖНО (1):
Вспомните симптомы и признаки анафилактических реакций.
Что вы будете делать при анафилактическом шоке?
Какие препараты, которые вы применяете, могут спровоцировать аллергическую реакцию?
Подкожный путь введения
Подкожный путь введения препаратов используется, когда необходимо медленное равномерное всасывание медикамента в кровь, при этом 1-2 мл препарата вводят под кожу. Этот путь введения идеален для таких лекарственных препаратов, как инсулин, который требует медленного равномерного высвобождения, он относительно безболезненный и подходит для частых инъекций (Springhouse Corporation 1993).
На Рис. 2 представлены места, пригодные для выполнения подкожных инъекций.
Традиционно, подкожные инъекции проводятся путем вкола иглы под углом 45 градусов в складку кожи (Thow и Home 1990). Однако с введением в практику более коротких инсулиновых игл (длиной 5, 6 или 8 мм), инъекции инсулина сейчас рекомендуется выполнять со вколом иглы под углом 90 градусов (Burden 1994). Следует обязательно брать кожу в складку, для того, чтобы отделить жировую ткань от подлежащих мышц, особенно у худых пациентов (Рис. 3). Некоторые исследования с применением компьютерной томографии для отслеживания направления движения инъекционной иглы, показали, что иногда при подкожном введении препарат непреднамеренно оказывается в мышце, особенно при инъекциях в переднюю брюшную стенку у худых пациентов (Peragallo-Dittko 1997).
Инсулин, введенный внутримышечно, всасывается намного быстрее, и это может привести к нестабильной гликемии, и возможно, даже к гипогликемии. Гипогликемические эпизоды могут отмечаться и в том случае, если меняется анатомическая область проведения инъекции, так как инсулин из разных участков всасывается с разной скоростью (Peragallo-Dittko 1997).
По этой причине должна проводиться постоянная смена мест введения инсулина, например, в течение нескольких месяцев используется область плеча или живота, затем место введения меняется (Burden 1994). Когда госпитализируется пациент с диабетом, надо посмотреть, нет ли в местах введения инсулина признаков воспаления, отека, покраснения или липоатрофий, и обязательно отметить это в медицинской документации.
Проводить аспирацию содержимого иглы при подкожном введении в настоящее время признано нецелесообразным. Peragallo-Dittko (1997) сообщает о том, что прокол кровеносных сосудов перед подкожной инъекцией встречается очень редко.
Информацию о необходимости аспирации не содержат и обучающие материалы для пациентов с диабетом. Также было отмечено, что аспирация перед введением гепарина повышает риск образования гематомы (Springhouse Corporation 1993).
Внутримышечный путь введения
При внутримышечном введении лекарственный препарат оказывается в хорошо перфузируемой мышце, что обеспечивает его быстрое системное воздействие, и всасывание достаточно больших доз, от 1 мл из дельтовидной мышцы до 5 мл в других мышцах у взрослых (для детей эти значения следует делить пополам). Выбор места для инъекции должен быть основан на общем состоянии пациента, его возрасте и объеме раствора лекарственного препарата, который нужно ввести.
Предполагаемое место инъекции следует осмотреть на предмет признаков воспаления, отека и инфекции, следует избегать введения препарата в участки повреждений кожи. Аналогичным образом через 2-4 часа после манипуляции место проведения инъекции следует осмотреть, чтобы убедиться, что нет никаких нежелательных явлений. Если инъекции часто повторяются, то надо отмечать места введения, чтобы менять их.
Это снижает дискомфорт у пациента и уменьшает вероятность развития осложнений, например, атрофии мышц или стерильных абсцессов вследствие плохого всасывания препаратов (Springhouse Corporation 1993).
ВАЖНО (2):
При госпитализации пациентов с диабетом должна вестись специальная медицинская документация.
Как вы отмечаете места ротации инъекций?
Как вы мониторируете пригодность места инъекции?
Обсудите это со своими коллегами.
Рис. 2. Анатомические области для внутрикожных и подкожных инъекций. Красные точки — места подкожных и внутрикожных инъекций, черные крестики — места выполнения только внутрикожных инъекций.
Рис. 3. Захват складки кожи при выполнении подкожной инъекции.
У пожилых и истощенных людей мышечная масса меньше, чем у молодых, более активных людей, поэтому перед выполнением внутримышечной инъекции надо оценить, достаточна ли для этого мышечная масса. Если у пациента мало мышц, то можно взять мышцу в складку до того, как проводить инъекцию (Рис. 4).
Рис. 4. Как взять мышцу в складку у истощенных или пожилых пациентов.
Существует пять анатомических областей, пригодных для выполнения внутримышечных инъекций.
На Рис. 5(a-d) подробно показано, как определить анатомические ориентиры всех этих областей. Вот эти анатомические области:
- Дельтовидная мышца на плече, эта область используется в основном для введения вакцин, в частности вакцины от гепатита В и АДС-анатоксина.
- Ягодичная область, большая ягодичная мышца (верхний наружный квадрант ягодицы) — это традиционная область для проведения внутримышечных инъекций (Campbell 1995). К сожалению, существуют осложнения, при использовании данной анатомической области возможно повреждение седалищного нерва или верхней ягодичной артерии при неправильном определении точки введения иглы. Beyea и Nicholl (1995) в своей публикации приводят данные нескольких исследователей, которые использовали компьютерную томографию и подтвердили тот факт, что даже у пациентов с умеренным ожирением, инъекции в ягодичную область чаще приводят к тому, что препарат оказывается в жировой ткани, а не в мышечной, что безусловно замедляет всасывание лекарственного препарата.
- Передне-ягодичная область, средняя ягодичная мышца — это более безопасный способ выполнения внутримышечных инъекций. Он рекомендуется потому, что здесь нет крупных нервов и сосудов, и нет сообщений об осложнениях вследствие их повреждения (Beyea и Nicholl 1995). Вдобавок, толщина жировой ткани здесь более или менее постоянна, и составляет 3.75 см по сравнению с 1-9 см в области большой ягодичной мышцы, что позволяет утверждать, что стандартная внутримышечная игла калибра 21 G (зеленая) окажется в средней ягодичной мышце.
- Латеральная головка четырехглавой мышцы бедра. Эта анатомическая область чаще всего используется для инъекций у детей, при ней есть риск непреднамеренного повреждения бедренного нерва с дальнейшим развитием атрофии мышц (Springhouse Corporation 1993). Beyea и Nicholl (1995) предположили, что эта область безопасна у детей до семимесячного возраста, затем лучше всего пользоваться верхним наружным квадрантом ягодицы.
Рис. 5a. Определение положения дельтовидной мышцы.
Самая плотная часть мышцы определяется так: от акромиального отростка проводится линия до точки на плече на уровне подмышки. Игла вводится примерно на 2.5 см ниже акромиального отростка на глубину 90º.
Следует избегать лучевого нерва и плечевой артерии (Springhouse Corporation 1993).
Можно попросить пациента положить кисть на бедро (как это делают модели во время показов), что облегчает поиск мышцы.
Для определения большой ягодичной мышцы: пациент может лежать на боку со слегка согнутыми коленями, или направив большие пальцы ног вовнутрь. Если ноги слегка согнуты, то мышцы более расслаблены и инъекция менее болезненная (Covington и Trattler 1997).
Рис. 5b. Определение наружного верхнего квадранта ягодицы.
Проведите воображаемую горизонтальную линию от места начала межъягодичной щели до большого вертела бедра. Затем нарисуйте другую воображаемую линию вертикально в середине предыдущей, и вверху латерально будет верхний наружный квадрант ягодицы (Campbell 1995). Мышца, которая в нем лежит — это большая ягодичная мышца. При ошибке во время выполнения инъекции можно повредить верхнюю ягодичную артерию и седалищный нерв. Типичный объем жидкости для введения в этой области составляет 2-4 мл.
Рис. 5c. Определение переднее-ягодичной области.
Положите ладонь правой руки на большой вертел левого бедра пациента (и наоборот). Указательным пальцем нащупайте верхний передний гребень подвздошной кости и отодвиньте средний палец, чтобы образовалась буква V (Beyea и Nicholl 1995). Если у вас маленькие руки, то это получается сделать не всегда, поэтому просто сдвиньте руку в сторону гребня (Covington и Trattler 1997).
Иглу вводят в среднюю ягодичную мышцу в середине буквы V под углом 90º. Типичный объем раствора препарата для введения в этой области составляет 1-4 мл.
Рис. 5d. Определение латеральной головки четырехглавой мышцы бедра и прямой мышцы бедра.
У взрослых латеральную головку четырехглавой мышцы бедра можно определить на ладонь ниже и латеральнее большого вертела, и на ладонь выше колена, в средней трети четырехглавой мышцы бедра. Прямая мышца бедра находится в средней трети передней поверхности бедра. У детей и пожилых, или у истощенных взрослых, иногда эту мышцу приходится брать в складку, чтобы обеспечить достаточную глубину введения препарата (Springhouse Corporation 1993). Ого раствора препарата составляет 1-5 мл, для младенцев — 1-3 мл.
Прямая мышца бедра — это часть передней четырехглавой мышцы бедра, это место редко используется для инъекций медсестрами, но нередко используется при самостоятельном введении лекарственных препаратов, или у младенцев (Springhouse Corporation 1993).
ВАЖНО (3):
Научитесь определять анатомические ориентиры для каждой из этих пяти областей для внутримышечных инъекций.
Если вы привыкли вводить препараты только в верхне-наружный квадрант ягодицы, то научитесь использовать новые области и регулярно совершенствует свою практику.
Методика
От угла введения иглы зависит боль от инъекции. Иглу при внутримышечной инъекции следует вводить под углом 90° и убедиться, что игла достигла мышцы — это позволяет уменьшить боль от инъекции. Исследование Katsma и Smith (1997) выявило, что не все медсестры вводят иглу под углом 90°, считая, что именно такая методика делает инъекцию более болезненной, так как игла быстро проходит сквозь ткани. Растягивание кожи уменьшает вероятность повреждений от иглы и улучшает точность введения препарата.
Чтобы правильно ввести иглу, положите кисть нерабочей руки и натяните кожу над местом вкола указательным и средним пальцем, а запястье рабочей руки положите на большой палец нерабочей. Держите шприц между подушечками большого и указательного пальцев, именно так удается ввести иглу точно и под нужным углом (Рис. 6).
Рис. 6. Методика выполнения внутримышечной инъекции, угол вкола иглы 90º, переднее-ягодичная область.
В Великобритании проводилось мало исследований на эту тему, поэтому у медсестер могут быть совершенно разные навыки и технологии выполнения инъекций (MacGabhann 1998). Традиционная методика выполнения внутримышечных инъекций заключалась в растяжении кожи над местом ее прокола, чтобы снизить чувствительность нервных окончаний (Stilwell 1992) и быстрый укол иглой под углом в 90° к коже.
Однако в обзоре литературы, подготовленном Beyea и Nicholls’ (1995) указано, что использование Z-методики дает меньший дискофморт и сниженное количество осложнений по сравнению с традиционной методикой.
Z—методика
Эта методика изначальна была предложена для введения лекарственных препаратов, которые окрашивают кожу или являются сильными раздражителями. Сейчас она рекомендуется для внутримышечного введения любых медикаментов (Beyea и Nicholl 1995), так как считается, что ее применение уменьшает болезненность, и вероятность вытекания препарата (Keen 1986).
В этом случае кожу на месте инъекции оттягивают вниз или в сторону (Рис. 7). Это сдвигает кожу и подкожную клетчатку примерно на 1-2 см. Очень важно помнить, что при этом направление иглы меняется и можно не попасть в нужное место.
Поэтому, после определения места инъекции, нужно выяснить, какая мышца находится под поверхностными тканями, а не какие кожные ориентиры вы видите. После введения препарата подождите 10 секунд до удаления иглы, чтобы препарат всосался в мышцу. После удаления иглы, отпустите кожу. Ткани над местом инъекции закроют депозит раствора лекарственного средства и предотвратят его утечку. Считается, что если конечность после инъекции будет двигаться, то всасывание препарата ускорится, так как в месте инъекции увеличится кровоток (Beyea и Nicholl 1995).
Рис. 7. Z-методика.
Методика воздушного пузырька
Эта методика была очень популярна в США. Исторически она была разработана во времена использования стеклянных шприцев, в которых требовалось использовать пузырек воздуха для того, чтобы убедиться, что доза препарата правильная. Сейчас «мертвое пространство» в шприце не считается необходимым, так как пластиковые шприцы откалиброваны более точно, чем стеклянные и эта методика больше не рекомендуется производителями (Beyea and Nicholl 1995).
Недавно в Великобритании были проведены два исследования на муляжах (масляный раствор с медленным высвобождением препарата) (MacGabhann 1998, Quartermaine и Taylor 1995), в которых сравнивалась Z-методика и методика воздушного пузырька, предназначеная для предупреждения утечки раствора после инъекции.
Quartermaine и Taylor (1995) предположили, что методика воздушного пузырька более эффективна для предупреждения утечки по сравнению с Z-методикой, но результаты MacGabhann (1998) не позволили сделать каких-то определенных выводов.
Существуют вопросы, связанные с точностью дозировки при использовании данной методики, так как доза препарата в данном случае может существенно повышаться (Chaplin et al 1985). Требуются дальнейшие исследования данной методики, так как для Великобритании она считается относительно новой. Однако, если она используется, медицинская сестра должна убедиться, что она вводит пациенту правильную дозу препарата, и что методика используется строго в соответствии с рекомендациями.
Методика аспирации
Хотя в настоящее время методика аспирации не рекомендована для контроля при проведении подкожных инъекций, ее следует использовать при внутримышечных инъекциях. Если игла по ошибке попала в кровеносный сосуд, то препарат можно непреднамеренно ввести внутривенно, что иногда приводит к эмболии вследствие специфических химических свойств лекарств. При внутримышечном введении препарата, в течение нескольких секунд следует проводить аспирацию содержимого иглы, особенно если используются тонкие длинные иглы (Torrance 1989a). Если в шприце видно кровь, то его вынимают, и готовят свежий препарат для инъекции в другом месте. Если крови нет, то препарат можно вводить, со скоростью примерно 1 мл за 10 секунд, это кажется немного медленным, но позволяет мышечным волокнам раздвинуться для правильного распределения раствора. Перед тем, как удалять шприц, надо подождать еще 10 секунд, а потом убрать шприц и прижать место введения салфеткой со спиртом.
Массировать место инъекции не нужно, так как в этом случае может возникнуть утечка препарата из места введения и раздражение кожи (Beyea и Nicholl 1995).
Обработка кожи
Хотя известно, что очистка кожи салфеткой со спиртом до проведения парентеральных манипуляций снижает число бактерий, на практике имеются противоречия. Протирание кожи для подкожного введения инсулина предрасполагает к уплотнению кожи под действием алкоголя.
Ранее проведенные исследования позволяют предположить, что такое протирание не является необходимым, и что отсутствие подготовки кожи не приводит к инфекционным осложнениям (Dann 1969, Koivisto и Felig 1978).
Некоторые специалисты сейчас считают, что если пациент соблюдает чистоту, а медсестра четко выполняет все стандарты гигиены и асептику во время выполнения процедуры, то дезинфекция кожи при выполнении внутримышечной инъекции не является необходимой. Если практикуется дезинфекция кожи, то кожу нужно протирать не менее 30 секунд, потом давать ей высохнуть в течение еще 30 секунд, в противном случае вся процедура неэффективна (Simmonds 1983). Вдобавок, выполнение инъекции до высыхания кожи, не только увеличивается ее болезненность, но и в толщу тканей могут попасть еще живые бактерии с кожи (Springhouse Corporation 1993).
ВАЖНО (4):
Какие рекомендации по обработке кожи перед инъекциями существуют в вашем учреждении?
Уточните, какие рекомендации есть по проведению инъекций инсулина.
Соответствуют ли эти рекомендации данным исследований, приведенным в статье?
Как вы будете поступать?
ВАЖНО (5):
Представьте себе, что вы наблюдаете за студентом, который собирается выполнить свою первую инъекцию. Какие подсказки или советы вы будете использовать в этом случае, чтобы обучающийся правильно развивал навыки выполнения инъекций?
Оборудование
Иглы для внутримышечных инъекций должны быть такой длины, чтобы они достигли мышцы, и при этом не менее четверти иглы должны оставаться над кожей. Чаще всего для внутримышечных инъекций используются иглы калибра 21G (зеленые) или 23 (синие), длиной от 3 до 5 см. Если у пациента много жировой ткани, то для выполнения внутримышечных инъекций требуются более длинные иглы, чтобы они достигли мышцы. Cockshott et al (1982) обнаружили, что толщина подкожно-жировой клетчатки у женщин в ягодичной области может быть на 2.5 см больше, чем у мужчин, поэтому стандартная инъекционная игла 21 G длиной 5 см достигает большой ягодичной мышцы только у 5% женщин и 15% мужчин!
Beyea и Nicholl (1995) рекомендовали смену иглы при выполнении внутримышечной инъекции после набора препарата из ампулы или флакона, чтобы быть уверенными в том, что игла чистая, сухая и острая.
Если иглой уже прокалывали резиновую крышку флакона, то она тупится, и в этом случае инъекция будет более болезненной, так как кожу приходится прокалывать с большим усилием.
Размер шприца определяется объемом вводимого раствора. Для внутримышечного введения растворов в объеме менее 1 мл, применяются только шприцы малого объема, чтобы точно отмерить нужную дозу препарата (Beyea и Nicholl 1995). Для введения растворов объемом 5 мл и более, лучше разделить раствор на 2 шприца и вводить в разные участки (Springhouse Corporation 1993). Обратите внимание на наконечники шприцов — они имеют разное предназначение.
Перчатки и вспомогательные материалы
В некоторых учреждениях правила требуют использования перчаток и фартуков во время выполнения инъекций. Следует помнить, что перчатки защищают медицинскую сестру от выделений пациента, от развития лекарственной аллергии, но они не обеспечивают защиты от повреждений от игл.
Некоторые медицинские сестры жалуются, что в перчатках им работать неудобно, особенно если изначально они учились выполнять ту или иную манипуляцию без них. Если медицинская сестра работает без перчаток, то нужно проявлять осторожность, и следить за тем, чтобы на руки ничего не попало — ни лекарств, ни крови пациентов. Даже чистые иглы надо сразу же утилизировать, их ни в коем случае нельзя повторно закрывать колпачками, иглы сбрасывают только в специальные контейнеры. Помните, что иглы могут упасть из лотков для инъекций на кровать пациенту, что может привести к травмам как у пациентов, так и у персонала.
Для защиты спецодежды от брызгов крови или растворов для инъекций можно использовать чистые одноразовые фартуки, также это полезно в тех случаях, когда необходим особый санэпидрежим (для профилактики переноса микроорганизмов от одного больного к другому). Нужно аккуратно снимать фартук после процедуры, чтобы попавшие на него загрязнения не вступали в контакт с кожей.
ВАЖНО (6):
Составьте список из всех способов, которые помогают уменьшить болезненность инъекций. Сравните с Таблицей 1.
Как вы сможете использовать больше способов уменьшения болезненности инъекций в вашей практике?
Таблица 1. Двенадцать шагов к тому, чтобы сделать инъекции менее болезненными
| 1 | Подготовьте пациента, объясните ему сущность процедуры, так, чтобы он понял, что будет происходить, и четко выполнял все ваши инструкции |
| 2 | Поменяйте иглу после того, как вы набрали препарат из флакона или ампулы, и убедитесь, что она острая, чистая и достаточной длины |
| 3 | У взрослых и детей старше семи месяцев местом выбора для инъекций является передне-ягодичная область |
| 4 | Расположите пациента так, чтобы одна нога была слегка согнута — это уменьшает болезненность при инъекции |
| 5 | Если вы используете салфетки со спиртом, убедитесь, что до выполнения инъекции кожа полностью высохла. |
| 6 | Можно использовать лед или замораживающий спрей, чтобы обезболить кожу, особенно это важно для маленьких детей и пациентов, которые страдают фобией уколов. |
| 7 | Используйте Z-методику (Beyea и Nicholl 1995) |
| 8 | Меняйте стороны выполнения инъекций и отмечайте это в медицинской документации |
| 9 | Прокалывайте кожу аккуратно, под углом, близким к 90 градусам, чтобы предотвратить болезненность и смещение тканей |
| 10 | Аккуратно и медленно введите раствор, со скоростью 1 мл за 10 секунд, чтобы она распределилась в мышце |
| 11 | Перед тем, как убирать иглу, подождите 10 секунд, и вытаскивайте иглу под тем же углом, что и вводили |
| 12 | Не массируйте место инъекции после ее завершения, просто прижмите участок укола марлевой салфеткой |
Уменьшение боли
Пациенты очень часто боятся выполнения инъекций, поскольку предполагают, что это больно. Боль обычно возникает вследствие раздражения болевых рецепторов кожи, или рецепторов давления в мышце.
Torrance (1989b) привел список факторов, которые могут вызывать боль:
- Игла
- Химический состав раствора лекарственного препарата
- Методика выполнения инъекции
- Скорость введения препарата
- Объем раствора лекарственного препарата
В Таблице 1 перечислены способы уменьшения болезненности от введения препарата.
У пациентов может быть сильная боязнь уколов и игл, страх, беспокойство — все это значительно усиливает болезненность при инъекциях (Pollilio и Kiley 1997). Хорошая техника выполнения процедуры, адекватное информирование пациента и спокойная, уверенная медсестра — лучший путь к уменьшению болезненности манипуляции и уменьшению реакции больного. Можно также использовать методики модификации поведения, особенно в случае, когда пациенту предстоят длительные курсы лечения, а иногда приходится применять безыгольные системы (Pollilio и Kiley 1997).
Предполагается, что обезболивание кожи льдом или охлаждающими спреями до укола позволяет уменьшить боль (Springhouse Corporation 1993), хотя в настоящее время нет доказательств эффективности этой методики, полученных в исследованиях.
Медицинские сестры должны понимать, что пациенты могут даже переживать синкопальные состояния или обмороки после обычных инъекций, даже если в остальном они вполне здоровы. Нужно выяснить, было ли такое ранее, и желательно, чтобы рядом была кушетка, на которую больной может прилечь — это уменьшает риск травм. Чаще всего такие обмороки случаются у подростков и молодых мужчин.
ВАЖНО (7):
Оцените возможность возникновения осложнений, которые мы обсуждали.
Запишите, что вы можете сделать, чтобы их предотвратить.
Осложнения
Осложнения, которые развиваются в результате инфицирования, могут быть предупреждены строгим соблюдением мер асептики и тщательным мытьем рук. Стерильные абсцессы могут возникать в результате частых инъекций или плохого местного кровотока. Если место инъекции отечное или эта область тела парализована, то препарат будет плохо всасываться, и такие участки не стоит использовать для инъекций (Springhouse Corporation 1993).
Тщательный выбор места инъекции позволит избежать повреждения нерва, случайно внутривенной инъекции и последующей эмболии компонентами препарата (Beyea и Nicholl 1995). Систематическая смена места инъекции предупреждает такие осложнения, как инъекционная миопатия и липогипертрофия (Burden 1994). Подходящая длина иглы и использование для инъекций передне-ягодичной области позволяет ввести лекарственный препарат точно в мышцу, а не в подкожно-жировую клетчатку. Применение Z-методики уменьшает боль и окрашивание кожи, характерное для применения некоторых лекарственных препаратов (Beyea и Nicholl 1995).
Профессиональная ответственность
Если препарат введен парентерально, то «вернуть» его уже никак нельзя. Поэтому всегда надо проверять дозу, правильность назначения, и уточнять у пациента его фамилию, чтобы не перепутать назначения. Итак: нужное лекарство нужному пациенту, в нужной дозе, в нужное время, и нужным способом — это позволит избежать медицинских ошибок. Все препараты надо готовить исключительно по инструкции производителя, все медсестры должны знать, как действуют эти препараты, противопоказания к их применению и побочные действия. Медицинская сестра должна оценить, а можно ли вообще применять препарат у данного пациента в данное время (UKCC 1992).
Выводы
Безопасное выполнение инъекций — одна из основных функций медицинской сестры, оно требует знания анатомии и физиологии, фармакологии, психологии, навыков общения, и практического опыта.
Существуют исследования, которые доказывают эффективность методик выполнения инъекций для предупреждения осложнений, но до сих пор есть «белые пятна», которые нуждаются в дополнительных исследованиях. В данной статье акцент сделан на доказанных в исследованиях методиках, чтобы медицинские сестры могли включать данные процедуры в свою ежедневную практику.
Список литературы
Beyea SC, Nicholl LH (1995) Administration of medications via the intramuscular route: an integrative review of the literature and research-based protocol for the procedure. Applied Nursing Research. 5, 1, 23-33.
Burden M (1994) A practical guide to insulin injections. Nursing Standard. 8, 29, 25-29.
Campbell J (1995) Injections. Professional Nurse. 10, 7, 455-458.
Chaplin G et al (1985) How safe is the air bubble technique for IM injections? Not very say these experts. Nursing. 15, 9, 59.
Cockshott WP et al (1982) Intramuscular or intralipomatous injections. New England Journal of Medicine. 307, 6, 356-358.
Covington TP, Trattler MR (1997) Learn how to zero in on the safest site for an intramuscular injection. Nursing. January, 62-63.
Dann TC (1969) Routine skin preparation before injection. An unnecessary procedure. Lancet. ii, 96-98.
Katsma D, Smith G (1997) Analysis of needle path during intramuscular injection. Nursing Research. 46, 5, 288-292.
Keen MF (1986) Comparison of Intramuscular injection techniques to reduce site Koivisto VA, Felig P (1978) Is skin preparation necessary before insulin injection? Lancet. i, 1072-1073.
MacGabhann L (1998) A comparison of two injection techniques. Nursing Standard. 12, 37, 39-41.
Peragallo-Dittko V (1997) Rethinking subcutaneous injection technique. American Journal of Nursing. 97, 5, 71-72.
Polillio AM, Kiley J (1997) Does a needless injection system reduce anxiety in children receiving intramuscular injections? Pediatric Nursing. 23, 1, 46-49.
Quartermaine S, Taylor R (1995) A Comparative study of depot injection techniques. Nursing Times. 91, 30, 36-39.
Simmonds BP (1983) CDC guidelines for the prevention and control of nosocomial infections: guidelines for prevention of intravascular infections. American Journal of Infection Control. 11, 5, 183-189.
Springhouse Corporation (1993) Medication Administration and IV Therapy Manual. Second edition. Pennsylvania, Springhouse Corporation.
Stilwell B (1992) Skills Update. London, MacMillan Magazines.
Thow J, Home P (1990) Insulin injectiontechnique. British Medical Journal. 301, 7, July 3-4.
Torrance C (1989a) Intramuscular injection Part 2. Surgical Nurse. 2, 6, 24-27.
Torrance C (1989b) Intramuscular injection Part 1. Surgical Nurse. 2, 5, 6-10.
United Kingdom Central Council for Nursing, Midwifery and Health Visiting (1992) Standards for Administration of Medicine. London, UKCC.
Качество медицинских услуг за последние пару десятков лет заметно возросло. Люди сейчас могут обратиться и в частную клинику, чтоб не стоять в очередях, появилось много новых препаратов и, как результат, выросло общее число инъекций. Кроме положительного эффекта тут возможны и нежелательные побочные последствия и с ними лучше быть знакомым.
Что вызывает осложнения?
Нередко осложнения после уколов могут быть вызваны непрофессионализмом медсестры делающей уколы. Также к главным причинам появления постинъекционных флегмон и абсцессов относится нарушение правил асептики – инокуляция инфекции. Если кожа обработана плохо, патогенный возбудитель проникает в ткани. Тот же эффект получается, при недостаточно хорошей обработке игл шприцов или когда они пачкаются в процессе работы.
Самое главное для профилактики – соблюдение норм асептики при произведении уколов.
Тем не менее, в месте укола может образоваться абсцесс даже в случае соблюдения норм асептики. Так происходит, когда патогенный возбудитель проникает в очаг хронической или острой инфекции. Флегмоны и абсцессы появляются еще в результате неправильной техник произведения уколов, осложнений из-за побочных действий лекарственных препаратов.
В большинстве случаев уколы делают в ягодицы, и чаще всего абсцессов появляются как раз в этой области. Уколы в плечо делают реже, и абсцессы в этом участке появляются в 25% случаев, и т.д.
Для правильного выполнения укола при подборе игл должна учитываться топография нервно-сосудистых пучков области, куда будет делаться укол, толщина подкожного слоя жира.
Постинъекционные осложнения может вызвать привычка массировать место укола, из-за этого развивается эмболия сосудов, появляется некроз мышц. Поэтому не следует забывать об элементарных правилах безопасности.
Важно отметить, что средства для внутримышечного применения в случае подкожного их введения вызывают в месте укола асептический некроз ткани. К данным препаратам относятся антибиотики, глюконат кальция, витамины В.
Помимо этого, одной из самых частых причин постинъекционных осложнений является чрезмерно широкое использование масляных и концентрированных растворов, особенно при неверной технике выполнения уколов.
Как выбрать лучшее место для внутримышечного укола?
Следите за тем, куда вводятся инъекции. Составьте список место, подходящих для этого. Записывайте дату, время и место каждый раз, когда делаете укол.
Изменение места инъекции: важно использовать другое место каждый раз, когда вы вводите инъекцию. Это помогает предотвратить шрамы и повреждение кожи. Участки, куда делается укол, должны быть на расстоянии не менее 2,5 см друг от друга.
Какие предметы нужны для инъекций?
Нужны такие предметы:
- Одна спиртовая салфетка.
- Одна стерильная 2×,2 марлевая прокладка.
- Новая игла и шприц нужных размеров.
- Одноразовые перчатки, если есть.
Как делать внутримышечный укол?
Делать внутримышечный укол нужно следующим образом:
- Вымойте руки с мылом и полностью высушите их. При необходимости наденьте перчатки.
- Достаньте спиртовую салфетку: протрите область, где планируете сделать инъекцию. Дайте участку высохнуть. Не прикасайтесь к этой области, пока вы не вводите инъекцию.
- Подготовьте иглу. Удерживайте шприц рукой и приложите крышку другой рукой. Поместите шприц между большим пальцем и указательным пальцем. Позвольте стволу шприца опираться на ваш второй палец.
- Держите кожу вокруг, где вы сделаете инъекцию: свободной рукой аккуратно нажмите и потяните кожу так, чтобы она была слегка плотной.
- Вставьте иглу в мышцу: крепко держите ствол шприца и используйте свое запястье, чтобы ввести иглу через кожу и в мышцу под углом 90°.
- Проверьте иглу: отпустите кожу другой рукой. Держите шприц так, чтобы он оставался направленным прямо. Потяните назад на поршень немного, чтобы убедиться, что вы не попали в кровеносный сосуд. Если кровь вернется, немедленно удалите иглу. Не вводите лекарство. Утилизируйте шприц и лекарство. В новый шприц наберите больше лекарства. Вторую инъекцию делайте с другой стороны.
- Введите лекарство: нажмите на поршень, чтобы ввести лекарство. Не жмите сильно. Некоторые лекарства вызывают болевые ощущения. Вы можете медленно вводить лекарство, чтобы уменьшить боль.
- Удалите иглу: после того, как лекарство будет введено, удалите иглу под тем же углом, что и вводили. Поместите марлю на области, где сделали укол.
Как избавиться от использованных шприцев и игл?
Важно правильно распоряжаться использованными иглами и шприцами. Не бросайте их в общую мусорную корзину. Лучше поместить их в жесткий пластиковый контейнер, изготовленный специально для использованных шприцев и игл. Вы также можете использовать бутылку соды или другую пластиковую бутылку с винтовой крышкой. Удостоверьтесь, что игла не проткнула контейнер.
Загрузка…