Пренатальный скрининг на синдром Дауна был введен 20 лет назад без должного общественного и политического обсуждения, что обусловило многие социально-психологические и морально-этические проблемы в здравоохранении и обществе в целом. В ближайшие 5 лет может стать доступна новая технология, поэтому уже сейчас надо развернуть более широкие общественные дебаты по этой теме.
Пренатальный скрининг на синдром Дауна ежегодно охватывает миллионы беременных женщин во всем мире. Его разрешающая способность довольно низка, поэтому в случае положительного результата становится необходимым проведение инвазивных диагностических процедур, связанных с дополнительным риском для еще не родившегося ребенка. Прямым следствием их применения, наряду с выявлением генетических аномалий, является потеря многих детей, которые на самом деле не имели синдрома Дауна.
По нашим оценкам, современная практика скрининга в Англии и Уэльсе ежегодно предотвращает появление на свет примерно 660 детей с синдромом Дауна, но в то же время приводит к потере 400 детей, у которых нет этого синдрома. Хотя пренатальный диагноз стали ставить чаще, он не дает полной гарантии и по-прежнему рождается немало детей с синдромом Дауна (за 15 последних лет отмечен даже 25%-ный рост числа новорожденных с такой хромосомной аномалией).
Качество жизни людей с синдромом Дауна продолжает улучшаться. Во многих странах они стали жить дольше и достигать в жизни большего, чем когда-либо ранее. Количество новорожденных с синдромом Дауна продолжает расти, а средняя продолжительность жизни людей с данным видом генетической аномалии сейчас достигает 60 лет. В соответствии с этим приоритеты в научных исследованиях и практике должны быть сдвинуты с профилактики рождений людей с синдромом Дауна на улучшение медицинской помощи, образования, а также на их поддержку на протяжении всей жизни Мы полагаем, что генетический скрининг на умственные и физические способности должен пройти через широкое публичное обсуждение, прежде чем новые технологии пренатальной диагностики и секвенирования (расшифровки) генома станут доступными широкому кругу пациентов.
Согласно рекомендациям Американского колледжа акушеров и гинекологов, всем беременным женщинам в США должна быть предоставлена возможность пренатального скрининга на сроке беременности до 20 недель с предпочтением скрининга в первом триместре беременности. Ранее Национальный институт клинического мастерства Великобритании (NICE) рекомендовал обеспечить для всех женщины в первом триместре беременности возможность комбинированного тестирования, включая ультразвуковое обследование и анализы крови. В Шотландии недавно было объявлено, что комбинированный тест будет доступен для всех беременных женщин к марту 2011 года.
Пренатальный скрининг нацелен на то, чтобы оценить шансы конкретной женщины на рождение ребенка с синдромом Дауна и помочь родителям принять решение о том, надо ли проводить дополнительные диагностические обследования, которые сопряжены с некоторым риском для еще не родившегося ребенка. Этот процесс становится для большинства пар непростым, т. к. включает значительную долю неопределенности и подвергает испытанию их личностные ценности и установки.
Большинство исследований вплоть до настоящего времени было посвящено анализу точности оценок, получаемых на основе конкурирующих методик скрининга. Вместе с тем явно недостаточно изучено, в какой степени эти процедуры помогают людям принимать осознанное решение и как они влияют на общее благополучие родителей и детей. Проводились лишь отдельные исследования качества жизни людей с синдромом Дауна и тех дополнительных проблем, с которыми им приходится сталкиваться в жизни в связи с их состоянием
Национальный институт клинического мастерства Великобритании в обзоре по этой теме констатирует: «Высокодостоверные данные указывают, что беременные женщины не имеют достаточных знаний для того, чтобы принять осмысленные решения, которые необходимы в отношении скрининга на синдром Дауна». Некоторые специалисты-медики, по-видимому, неправильно понимают результаты тестов скрининга, так что вряд ли стоит удивляться тому, что многим беременным женщинам «особенно трудно осознать, какой смысл заключен в вычислении степени риска».
Кроме того, данные исследований, проведенных в США и Испании, подтверждают предположение, что во многих странах система медицинской помощи и поддержки, предоставляемых людям с данным диагнозом, явно недостаточна.
Консультирование может оказывать отсроченное влияние на качество жизни людей с синдромом Дауна и их близких. Современная практика скрининга потенциально способна отрицательно воздействовать на материнское отношение к ребенку, вызывая страх, пагубный для его развития. Не исключены и нежелательные психологические последствия для некоторых супружеских пар, остановивших свой выбор на селективном прерывании беременности. Эти неблагоприятные эффекты пренатального скрининга не подвергались таким суровым проверкам, как собственно различные его методики.
Гуманитарные и экономические издержки скрининга часто противопоставляются «бремени» и «стрессу», которые накладывает на семью наличие ребенка с синдромом Дауна. Однако исследования, проведенные в семьях, где воспитываются дети с синдромом Дауна, показали, что большинство родителей хорошо справляются с этой ситуацией и связывают с нею не только проблемы, но и позитивные моменты. В исследованиях такого рода обнаружены положительные воздействия на многих сиблингов, растущих в одной семье с ребенком, имеющим синдром Дауна.
Пренатальный скрининг представляет собой обширное поле деятельности для поставщиков соответствующих тестов и вспомогательных услуг. По расчетам специалистов в настоящее время синдром Дауна в Англии и Уэльсе при отсутствии скрининга с синдромом Дауна рождался бы в среднем 1 из 500 живорожденных детей. Потенциальный же рынок для тестов скрининга в Англии и Уэльсе ежегодно составляет почти 700 000 беременностей. Многие биохимические маркеры, используемые при скрининге, подлежат патентованию. И существует обеспокоенность по поводу влияния интересов определенного круга лиц на процесс исследований и формирование политики организаций, предоставляющих услуги и программное обеспечение, связанные со скринингом.
«Сегодня главная движущая сила расширения практики скрининга исходит от медицинских агентств, а не от простых людей и не является результатом демократических дебатов. По поводу скрининга в Великобритании не проводилось парламентских дискуссий и не принималось никаких законов. Политику формулируют консультативные советы, которые выпускают руководящие указания. В медицинской литературе подчеркивается необходимость профилактики страданий и предоставления родителям определенного выбора, связанного с возможностью прервать патологическую беременность. Оказывая давление на общество, органы здравоохранения приводят экономические аргументы: необходимо снизить “пожизненные расходы на медицинскую помощь” людям с синдромом Дауна, избежать дорогостоящих судебных разбирательств по поводу “нежелательного рождения” детей, которым не был поставлен диагноз, и разработать более дешевые, хотя также экономически рентабельные, технологии скрининга»[2]. [ Alderson, P. Prenatal screening, ethics and Down’s syndrome: a literature review // Nursing Ethics. 2001. Vol. 8, № 4. P. 360–-374.]
Итак, каким же образом обстоит дело в современной практике скрининга?
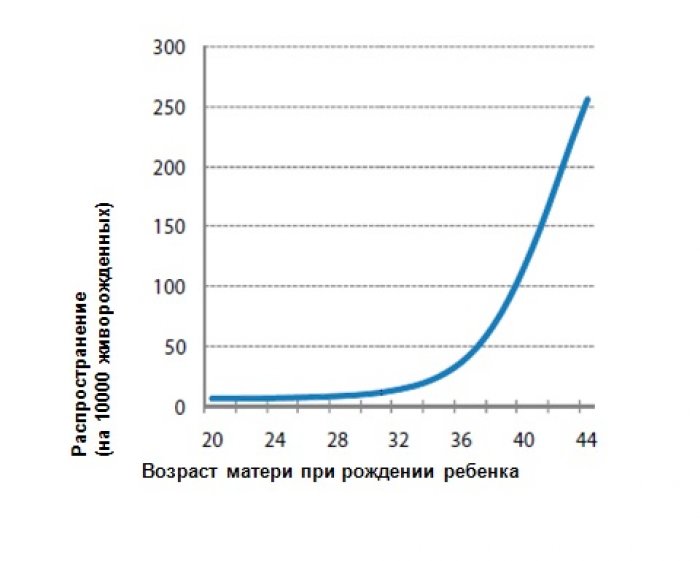
Рис. 1.| Зависимость распространения синдрома Дауна среди новорожденных от возраста матери
Вероятность рождения ребенка с синдромом Дауна увеличивается с возрастом матери, резко повышаясь у женщин старше 30 лет. Следовательно, возраст матери является ключевым фактором, определяющим распространенность синдрома Дауна среди новорожденных в любой конкретной популяции
Теоретическая модель пренатального скрининга
Возраст матери является четким предиктором рождения ребенка с синдромом Дауна (рис. 1). Исторически инвазивную диагностику предлагали матерям старше 35 лет, для которых только фактор возраста уже повышал вероятность рождения ребенка с синдромом Дауна (более чем до 1 на 350 живорожденных детей). Для таких матерей риск рождения ребенка с синдромом Дауна примерно соответствует риску потерять здорового ребенка в результате диагностических процедур. «Логическое обоснование» такого подхода состояло том, что риск рождения ребенка с синдромом Дауна, примерно соответствующий риску потери здорового ребенка или превышающий его, «оправдывает» инвазивные диагностические процедуры.
В 1980-е годы было выявлено, что в крови женщины, вынашивающей ребенка с синдромом Дауна, как правило, имеются определенного рода «маркеры», которые отсутствуют в крови женщин, вынашивающих здоровых детей. Это открытие привело к попыткам улучшить скрининг, основывая его не только на возрастных показаниях, но и на анализе этих «маркеров» в образцах крови матерей. С тех пор в попытках усовершенствовать скрининг беременности на синдром Дауна, сделать его более точным применялись разные комбинации маркеров в сочетании с ультразвуковыми измерениями плода.
Разрешающая способность тестов скрининга такова, что они дают возможность лишь оценить шансы рождения ребенка с синдромом Дауна. Полученные оценки разделяют на «положительные» (высокий риск) и «отрицательные» (низкий риск), причем на основании этих оценок обычно принимают решение о проведении инвазивной пренатальной диагностики. Возможны четыре исхода скрининга: истинноположительный, ложноположительный, истинноотрицательный и ложноотрицательный (рис. 2). Тем матерям, у которых скрининг дал положительный результат, рекомендуют рассмотреть вопрос о проведении пренатальной диагностики инвазивными методами. Поскольку инвазивные процедуры сопряжены с определенным риском прерывания беременности, стратегические установки скрининга направлены на сведение к минимуму ложноположительных результатов. В то же время желательно довести до максимума показатели выявления синдрома.

Рис. 2. | Процесс скрининга, возможные исходы и показатели точности
Степень выявления (доля случаев, когда тесты скрининга позволили точно идентифицировать состояние плода): ИПР / (ИПР + ЛОР) = 85 %. Степень ложноположительных результатов (доля случаев, когда тесты скрининга ошибочно дали положительный результат при отсутствии синдрома Дауна у ребенка): ЛПР / (ЛПР + ИОР) = 6,7 %. Шансы для плода быть фактически пораженным при положительном результате скрининга (ИПР / ЛПР)1 : 20 (цифры иллюстративные)
Таким образом, «граница отсечения риска», то есть рубеж, разделяющий результаты скрининга на положительные и отрицательные, представляет собой, по существу, произвольную величину, балансирующую между степенью выявления синдрома и степенью ложноположительных результатов (рис. 3, а). Более высокая граница отсечения риска уменьшает число ложноположительных результатов, но также снижает и степень выявления (и наоборот), то есть влияет как на число родившихся детей с синдромом Дауна, так и на число потерь здоровых детей (рисунок 3, b). При использовании этой модели предполагается, что процент женщин, которые выбирают инвазивные методы диагностики при положительном результате скрининга, держится на одном и том же уровне и не зависит от вычисленной степени риска.. Но на практике женщины, выбравшие пренатальный скрининг, более склонны к инвазивной диагностике в случае получения повышенной оценки риска.

Рис. 3. | Балансирование между выявлением и ложноположительными результатами при определении границы отсечения риска:
– более высокая степень выявления подразумевает и более высокую вероятность ложноположительных результатов. Равновесие выбирают, устанавливая «границу отсечения», отделяющую результаты с «высоким» риском от результатов с «низким» риском;
– правильное выявление отягощенной беременности имеет место в среднем только в одном из 20–-30 случаев, давших положительный результат при первичном скрининге. Это побуждает многих женщин, беременность у которых фактически не отягощена синдромом Дауна, решиться на процедуры инвазивной диагностики, чреватые возможностью потери здорового ребенка. Выбор границы отсечения – это, по существу, выбор между предупреждением появления на свет больных детей и потерей здоровых детей. (Частотные показатели распространения, выявления и ложноположительных результатов, предсказанные границей отсечения в начале второго триместра беременности и примененные в иллюстративных целях для выборки размером 100 000 беременностей, допускают 60% положительных результатов скрининга, 90% случаев прерывания беременности с синдромом Дауна и 23% случаев естественной потери плода.)
Разница между выявлением и предупреждением
При зачатии у человека необычный численный набор хромосом встречается на удивление часто, по-видимому, затрагивая около 20 % всех оплодотворенных яйцеклеток. Многие такие яйцеклетки теряют жизнеспособность уже на первых неделях беременности. Беременности, отягощенные синдромом Дауна, намного чаще заканчиваются самопроизвольным прерыванием по сравнению с неотягощенными. В публикациях приводятся разные количественные оценки невынашивания беременности. Суммарный показатель свидетельствует о том, что 43 % плодов с синдромом Дауна, диагностированным на сроке беременности от 11 до 13 недель, и 23 % плодов с этим синдромом, диагностированным на сроке от 16 до 18 недель, не доживают до родов. У матерей старшего возраста показатели невынашивания, по-видимому, выше. При отсутствии исследований, проведенных на обширных выборках беременностей, прошедших пренатальную диагностику и прослеженных вплоть до завершения, довольно трудно дать точные числовые оценки. Кажется вполне вероятным, что по сравнению с данными по медицинскому прерыванию беременности или живорождению цифры невыношенных беременностей, фигурирующие в отчетах, часто ниже, чем могли бы быть при отсутствии вмешательств. Беременности, отягощенные синдромом Дауна, не выявленным пренатально (ложноотрицательный результат скрининга), но не закончившиеся рождением живого ребенка, также не включаются в сводки и представляют еще один источник искажения при подсчете данных.
Показатель естественных потерь означает, что количество случаев пренатального выявления синдрома Дауна и медицинского прерывания беременности не соответствуют количеству предупреждений живорождения (поскольку во многих случаях медицинского аборта плод не дожил бы до родов и сам по себе). Показатель естественных потерь также означает, что смещение скрининга на более ранние сроки беременности (например, за счет введения комбинированного теста в первом триместре) позволит выявить больше отягощенных беременностей, при которых плод не выжил бы и без медицинского аборта, то есть во многих случаях искусственное прерывание беременности будет подменять самопроизвольный выкидыш.
Оценки риска для будущих детей
Согласно доступным объективным данным риск прерывания беременности вследствие амниоцентеза составляет 1 %, а вероятность такого исхода после биопсии ворсин хориона (CVS) в первом триместре беременности – около 2 %. Наблюдается выраженная изменчивость по степени осложнений после амниоцентеза под ультразвуковым контролем и после CVS. Исследования выявили, что показатель потерь в результате проведения амниоцентеза в 6–8 раз выше при выполнении процедур начинающими врачами по сравнению с более опытными специалистами.
Ориентация на смещение скрининга в сторону первого триместра беременности (то есть на диагностику через CVS) может существенно увеличить неоправданные потери здоровых детей (без соответствующего снижения доли ложноположительных результатов).
Медицинская практика
Многие опубликованные исследования конкурирующих технологий скрининга моделируют эффекты различных границ отсечения риска. Однако надо признать, что моделирование может оказаться нерепрезентативным в отношении практического осуществления скрининга. Например, прогнозируемая разрешающая способность скрининга с четверным тестом, показанная на рис. 3, при отсечении на уровне ≥1:300 соответствовала степени выявления 86 % и частоте ложноположительных результатов 6,6 %. В то же время проверка разрешающей способности четверного теста в 14 больницах Великобритании показала степень выявления 81 % и частоту ложноположительных результатов 7 % при отсечении риска на уровне ≥1:300. Эти скромные различия соответствуют дополнительной потере двух здоровых детей и уменьшению показателя предупреждения живорождений с синдромом Дауна на 5 случаев в расчете на каждые 100 000 обследованных беременностей.
Другие исследования также наглядно иллюстрируют, насколько реальная практика может могут отличаться от некоторых моделей.
В Великобритании и многих странах Европы пренатальный скрининг в настоящее время доступен для большинства женщин независимо от возраста. В Англии и Уэльсе пренатальный скрининг стал широко использоваться с конца 1980-х годов. Государственный цитогенетический регистр по синдрому Дауна (NDSCR) ведет записи диагнозов и исходов беременности с 1 января 1989 года, а недавно опубликовал данные за 2006 год. Мы проанализировали данные записей NDSCR, чтобы оценить действенность официальных установок по пренатальному скринингу в Англии и Уэльсе за период с 1992 по 2006 год (см. таблицу). NDSCR записывает данные по всем беременностям с диагностированным синдромом Дауна и всем родам в Англии и Уэльсе. Мы сделали поправку на неизвестные исходы, чтобы получить полную оценку случаев живорождения, невынашивания/мертворождения и искусственного прерывания беременности. Затем было оценено число предупрежденных случаев живорождения детей с синдромом Дауна посредством вычитания прогнозируемых естественных потерь из числа беременностей, прерванных искусственно (допуская естественные плодные потери на уровне 43 и 23 % для беременностей, диагностированных через CVS и амниоцентез соответственно).
Записи по исходам тех беременностей, когда по итогам скрининга был получен положительный результат, но диагноз синдрома Дауна не был подтвержден последующими (инвазивными) анализами, не велись. Таким образом, были рассчитаны предположительные потери 45 здоровых детей на каждые 100 случаев пренатального диагноза синдрома Дауна (1 : 2,2) по анализам сыворотки и/или данным ультразвукового обследования, а также потери 143 здоровых детей на каждые 100 случаев синдрома Дауна (1 : 0,7), когда обследование проводилось по показаниям, связанным только с возрастом матери. Для введения поправки на возможные усовершенствования в практике, связанные с более частым в последние годы применением комбинированного теста, мы допускаем, что в период с 2001 по 2006 год потери здоровых детей снизились до 31 случая на каждые 100 беременностей с пренатальным диагнозом синдрома Дауна, поставленным по анализам сыворотки и/или результатам ультразвукового обследования (1 : 3,2). Эти допущения были приняты на основе данных о частоте выявления синдрома Дауна и доле ложноположительных результатов с применением четверного скрининга в практической работе 14 больниц Великобритании (46 000 беременностей, в том числе 88 с синдромом Дауна), о прогнозируемых рабочих характеристиках скрининга по возрасту матерей в том же исследовании, а также по данным, полученным при комбинированном скрининге в исследовании с участием 15 медицинских центров в США (36 000 беременностей, в том числе 92 с синдромом Дауна). Оценивая эти потери, мы исходили из допущения о частоте потерь в результате инвазивных диагностических процедур (CVS или амниоцентеза) порядка 1 %.
Оценочные характеристики пренатального скрининга по Англии и Уэльсу за период 1991–2006 гг.[3] [Данные за 2006 г. носят предварительный характер]
Трудно сказать, насколько точно эти допущения отражают положение дел в современной практике за отчетный период. Точные данные об использованных тестах скрининга и решении матерей после положительного результата скрининга не записывались (хотя NDSCR недавно начал сбор данных о тестах скрининга). Принятие этих допущений было основано на показателях, наблюдаемых в практике при проведении наиболее эффективного (четверного) теста по крови. В то же время следует отметить, что в отчетный период широко использовались двойной и тройной тесты, обладающие меньшей разрешающей способностью. Ультразвуковой скрининг без анализа маркеров крови также обладает худшими характеристиками по сравнению с четверным скринингом.
Таким образом, возможна следующая трактовка результатов современных наблюдений. Во-первых, хотя политика в области здравоохранения пропагандирует пренатальный скрининг в целях селективного прерывания беременности, сейчас рождается больше детей с синдромом Дауна, чем 15 лет назад, в том числе в процентном отношении к общему количеству новорожденных (рис. 4). За этот период оценочное снижение живорождений детей с синдромом Дауна за счет политики массового скрининга составило 44 % (с 16 985 при отсутствии вмешательств до 9525). Без скрининга у родителей могли бы быть разные соображения относительно сохранения беременности, но, тем не менее, интересно отметить, что со сдвигом деторождения на более поздний возраст связан ожидаемый рост распространения синдрома Дауна среди живорожденных без вмешательств, исходя из оценочной цифры 50 % (увеличение с 14,0 до 21,8 на 10 000) в период с 1992 до 2006 г.
Рис. 4 | Число живых детей, рождающихся с синдромом Дауна, продолжает расти:
а – общий показатель живорождений достиг пика за последние 15 лет, несмотря на приблизительно трехкратное увеличение числа пренатально диагностированных случаев этого синдрома;
б – распространение среди живорожденных продолжает увеличиваться, поскольку деторождение происходит в более позднем возрасте. При отсутствии прерываний беременности по показаниям, связанным с пренатальным диагнозом синдрома Дауна, его распространение среди живорожденных в настоящее время можно было бы оценить на приблизительном уровне 22 : 10 000 (1 : 455). Эти цифры примерно соответствуют современным данным о распространении синдрома Дауна среди новорожденных в Ирландии (где аборты запрещены законом).
Мы делаем вывод о том, что современная политика скрининга, по-видимому, ежегодно снижает число живорожденных детей с синдромом Дауна в Англии и Уэльсе приблизительно на 660 новых случаев и одновременно ведет к потере 400 детей, у которых нет синдрома Дауна. Введение обязательного комбинированного скрининга в первом триместре (как это рекомендовано Национальным институтом клинического мастерства Великобритании, Американским колледжем акушеров и гинекологов и недавно принято в Шотландии) приведет к выявлению большего числа детей с синдромом Дауна, которые в естественных условиях не дожили бы до родов. Если на практике вероятность потерь после CVS выше, чем после амниоцентеза, то принятие комбинированного скрининга в первом триместре может увеличить потери детей, у которых нет синдрома Дауна.
Жизнь по праву
Качество жизни большинства людей с синдромом Дауна во многих экономически развитых странах за последние 40 лет значительно улучшилось, существенно изменилась поддержка этих людей со стороны общества. Их медицинские потребности по большей части поняты обществом и удовлетворяются. Хорошая медицинская помощь помогла увеличить среднюю ожидаемую продолжительность жизни людей с синдромом Дауна во многих развитых странах приблизительно до 60 лет (с 12 лет в 1949 году), и все большее число таких людей сейчас реально доживает до возраста старше 70 лет. Растет число молодых людей с синдромом Дауна, получивших доступ к эффективному образованию и лечению, благодаря чему они достигают более высокого уровня грамотности и навыков общения. Все больше взрослых людей с синдромом Дауна, которые имеют общественно полезную и хорошо оплачиваемую работу, а также достигают достаточно высокого уровня контроля над своей жизнью. Предстоит еще многое сделать, и в отношении этого важного меньшинства людей пока остается много нерешенных проблем, но прогресс, достигнутый людьми с синдромом Дауна, поистине впечатляет.
Прогнозирование качества жизни
Знание того, что кто-то имеет не 46, а 47 хромосом, еще не дает достаточных оснований для точного предсказания качества его жизни. Одни дети с синдромом Дауна рождаются с пороками сердца (около 44 %), а у других таких врожденных пороков развития нет, у одних взрослых развивается деменция (до 9 % в возрасте 49 лет, до 18 % в возрасте 50–54 и до 35 % в возрасте 55–59 лет), а у других она не развивается, одни дети обучаются с большими трудностями, а другие достаточно легко, хотя число хромосом у всех людей с синдромом Дауна совершенно одинаковое. Парадоксально, но синдром Дауна, по-видимому, дает защиту от некоторых раковых и сердечно-сосудистых заболеваний.
Некоторые люди с синдромом Дауна пишут книги, снимаются в кино и на телевидении, среди них есть компетентные музыканты и талантливые спортсмены. Однако другие люди с синдромом Дауна с большим трудом находят себе применение в профессиональной сфере, поскольку могут выполнять только работу низкой квалификации. Многие люди с синдромом Дауна способны вносить позитивный вклад в семейные и общественные отношения, нередко создавая в жизни прочные связи на основе преданности и заботы. Очень редко таким людям свойственно антиобщественное, насильственное или криминальное поведение.
Качество жизни и общество
Насколько нам известно, до сих пор не проводилось серьезных и масштабных исследований, посвященных взглядам людей с синдромом Дауна на качество их жизни. В порядке наблюдения можно отметить, что они не рассматривают свое физическое и умственное состояние как источник страданий. Качество жизни людей с синдромом Дауна во многом зависит от отношения к ним общества, а не от синдрома Дауна как такового.
Надо ли продолжать скрининг?
Авторы этой статьи не считают синдром Дауна достаточным основанием для прерывания беременности и поэтому не согласны с основной идейной предпосылкой скрининга на синдром Дауна. Более того, потери детей, не имеющих синдрома Дауна, которые неизбежны в этом процессе, представляются неоправданными. И эта обеспокоенность довольно широко распространена в кругах специалистов. Обзорный анализ 40 случайно отобранных комиссий по этике научных исследований показал, что 86 % экспертов не считают современную практику скрининга и сопряженный с ней риск этически приемлемыми для достижения главной цели – избежать рождения человека с синдромом Дауна.
Будущее
Политика в области здравоохранения, связанная с селективным прерыванием беременности, в настоящее время не нацелена на большинство других генетических причин интеллектуальных нарушений, или поддающихся лечению болезней
Идет интенсивный поиск способов надежного выделения плодной ДНК из образцов материнской крови. В то же время есть еще одна насущная задача, требующая решения, – это снижение стоимости секвенирования генома хотя бы до 1000 долларов. Когда в обоих этих направлениях произойдет существенный сдвиг, мы сможем дать будущим родителям всестороннюю информацию о значительных факторах риска и множестве возможных исходов, которые могут повлиять (но могут и не повлиять) на качество жизни.ребенка.
«Если ДНК плода можно будет получать неинвазивно, то в практике скрининга мы создадим огромный массив информации с неопределенным значением. Такая информация способна принести больше вреда, чем пользы…» [3] [Shuster, E. Microarray genetic screening: a prenatal roadblock for life? // The Lancet. 2007. № 369(9560). P. 526–-529.]
Как могут супружеские пары придти к осознанному решению, сталкиваясь (например) лицом к лицу с выбором между оценочным уровнем риска аутизма и деменции? Как много беременностей может быть отвергнуто супружескими парами в стремлении получить «наилучшего» ребенка? Какое влияние окажет подобная практика на людей, которые «проскользнули через сито» и родились с «нежелательными» признаками?
Пренатальный скрининг на синдром Дауна был введен 20 лет назад с недостаточным общественным и политическим обсуждением. Когда станет реальным и широко доступным скрининг всего генома, многие неприятные проблемы, возникшие в результате опыта, полученного при скрининге на синдром Дауна, еще больше обострятся. Новая технология может стать доступной для нас в ближайшие 5 лет, поэтому уже сейчас надо развернуть более широкие общественные дебаты по этой теме.
Взгляды, выраженные в этой статье, отражают мнение ее авторов, которое не обязательно совпадает с личным мнением всех членов редколлегии.
Перевод А. Н. Прыткова
Ранняя диагностика синдрома Дауна: распространенные заблуждения и статистика
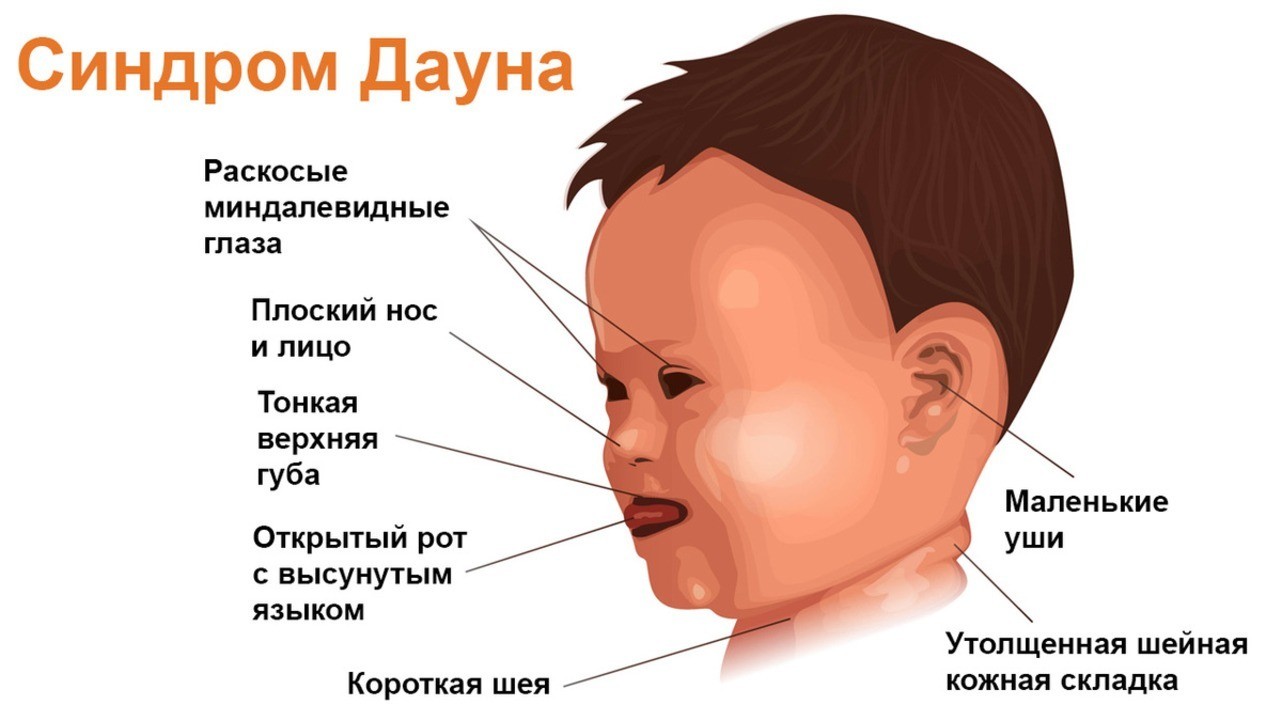
Еще в 1866 году Лэнгдон Даун заметил, что у пациентов с синдромом, которые получил название по фамилии ученого, маленький нос, плоское широкое лицо, толстая шейная складка. С возникновением ультразвука стали появляться более глубокие исследования в этой области, и диагностировать синдром Дауна стало возможным уже у эмбрионов. Главный врач Клиники МАМА Виктория Викторовна ЗАЛЕТОВА рассказывает об истории этих исследований и новейших достижениях.
Врачи всего мира работают в условиях определенной догматики: стопроцентной методики дородовой диагностики синдрома Дауна на данный момент не существует. Фактор риска присутствует всегда. И усилия специалистов разных областей во многих странах направлены на то, чтобы сделать его минимальным.
Одним из важнейших критериев — или ультразвуковых маркеров — при диагностировании синдрома Дауна у эмбрионов является толщина воротникового пространства (ТВП). У любого плода на сроке 11-14 недель можно ее измерить. Было замечено, что у 75% эмбрионов с синдромом Дауна ТВП больше, чем у обычных плодов. Позже были открыты не менее важные ультразвуковые маркеры: длина носовых костей, оценка кровотока в венозном протоке и на трикуспидальном клапане.
Риск, что у ребенка будут присутствовать какие-либо хромосомные аномалии, есть всегда. По синдрому Дауна он составляет порядка 1 на 500. Чем старше мама, тем больше риск (риск резко возрастает после 35 лет).
Доктор Николаидес, основатель Фонда Медицины Плода, и его коллеги в Лондоне в первом триместре беременности выявляют до 95% плодов с синдромом Дауна. Но есть так называемые «нечувствительные дауны» — они «нечувствительны» к этой диагностике. Их количество по данным Фонда Медицины Плода порядка 5%. Это те эмбрионы, которые пройдя биохимический и ультразвуковой скрининг показали абсолютно нормальные значения.
В последние годы пренатальная диагностика хромосомных патологий плода совершенствуется. Был разработан метод ДНК секвенирования клеток плода из крови матери. На 9-ой—10-ой неделе беременности пациентка сдает кровь, из которой «вылавливаются» клеточки эмбриона. И эти клетки анализируются на присутствие основных хромосомных патологий. Данный метод тоже имеет погрешность и не может поставить окончательный диагноз. Но ДНК секвенирование позволяет определить необходимость инвазивной диагностики.
Проведение преимплантационной генетической диагностики эмбрионов (ПГД) в рамках программ ЭКО так же является высокотехнологичной методикой выявления основных хромосомных аномалий, в том числе синдрома Дауна. Исследование позволяет заподозрить проблему на самом раннем этапе и не переносить в полость матки эмбрионы с заведомо лишней хромосомой. Но ПГД как и ДНК-секвенирование имеет свой процент ложно-положительных и ложно-отрицательных результатов. Поэтому в последствии для исключения риска хромосомных патологий требуется проведение комбинированного скрининга с дальнейшей инвазивной диагностикой. Инвазивная методика несет определенные риски по потере беременности, но только это исследование дает более точные результаты.
Комбинированный скрининг в первом триместре позволяет заподозрить патологию плода. Это вспомогательный метод, целью которого является выявление группы риска на основе ультразвуковых и биохимических маркеров. У 75% плодов с синдромом Дауна может быть расширено воротниковое пространство, у 25% оно будет нормальное. У 35-40% плодов с хромосомной патологией наблюдается аномальный венозный кровоток — у остальных он будет нормальный. Поэтому нужна комплексная оценка. Чем больше маркеров рассматривается, тем больше вероятность правильного заключения по этому эмбриону. По-прежнему во всем мире идет поиск новых маркеров. Все врачи пренатальной ультразвуковой диагностики очень этим озабочены, каждый год появляются новые исследования на эту тему.
На основе первого скрининга формируется группа риска. Но это еще не означает наличие синдрома Дауна у эмбриона, речь о подозрении. При расчете индивидуального риска отнесение к группе с высокой вероятностью присутствия заболевания в том числе может произойти из-за возрастного фактора, могли сказаться сывороточные маркеры, отражающие гормональный фон. Что касается расширения воротникового пространства, помимо синдрома Дауна, порядка 50-ти патологий сопровождаются этим признаком.
Практика такова: ложно-положительные и ложно-отрицательные результаты присущи любому скрининговому исследованию. Стопроцентная точность невозможна, это вспомогательный метод для выявления группы риска. Последующие исследования — консультация генетика, инвазивные методики и консилиум врачей разных специальностей — дают возможность подтвердить или опровергнуть диагноз.
У специалистов в этой области существует профессиональное определение «российские плоды с синдромом Дауна очень сложны для диагностики». В отличие от европейских плодов с синдромом Дауна они очень часто попадают в окно нормальных значений толщины воротникового пространства, длины носовой кости и пр. Их сложно выявить. Дело в том, что на территории нашей страны смешалось много наций. В наших жилах течет очень разная кровь, велико присутствие генов монголоидной расы. А при анализе ультразвуковой картины учитываются национальные особенности. И зачастую отклонение от нормативных значений можно принять за этнические черты.
Статистически в популяции на 100 000 плодов только 200 будут иметь синдром Дауна. При этом еще 200 будут иметь другие хромосомные дефекты и 99 600 будут иметь нормальный набор хромосом. Таким образом у порядка 5% эмбрионов воротниковое пространство, как ключевой показатель, будет выше нормативных значений.
Акушер-гинеколог, ведущий беременность, основываясь только на данных ультразвукового исследования и на уровне биохимических маркеров, не может судить, есть ли у плода синдром Дауна. После комбинированного скрининга пациентка направляется в медико-генетический центр. Для подтверждения или опровержения диагноза потребуется консультация врача-генетика и инвазивная пренатальная диагностика.
Врач-генетик анализирует уровень сывороточных маркеров, собирает анамнез, анализирует ультразвуковое исследование и, возможно, назначает повторный ультразвук у врача экспертного уровня. Если высокий риск присутствия хромосомной патологии подтверждается, следующий этап — это инвазивная пренатальная диагностика. В зависимости от срока беременности выделяют хорионбиопсию (на сроке от 11 до 15 недель) и амниоцентез.
Хорион — это будущая плацента, для анализа берут ее образец, в этом материале выявляют клетки плода и исследуют их ДНК. Амниоцентез выполняется после 15 недель — для анализа берется амниотическая жидкость (жидкость, в которой находится плод), в ней также выделяются клетки плода.
Инвазивное исследование назначается только при выявлении высокого риска по результатам комбинированного скрининга — 1:100 и выше (1:50, 1:20). Дело в том, что у каждой инвазивной методики есть процент потерь беременности. Он приблизительно равен 1%. То есть после проведения процедуры одна из ста пациенток может потерять беременность. Поэтому проведение инвазивного исследования должно быть оправдано высокими рисками появления ребенка с хромосомными аномалиями.
Инвазивные методы исследование дают порядка 90-99% точности в определении хромосомной патологии плода. Проводить или не проводить инвазивный тест, оставлять или прерывать беременность после подтверждения подозрений — окончательное решение остается за будущими родителями. Им предстоит оценить все риски, возможные последствия и принять итоговое решение. Долг врача — предоставить пациентке максимально полную информацию, дать предполагаемый прогноз. Но решение судьбы беременности и ответственность за будущее ребенка все-таки лежит на его родителях.
В 21 веке планирование и рождение детей происходит в принципиально изменившихся реалиях. Новые возможности медицины по диагностике, ухудшение экологической ситуации, повышение возраста первой беременности. Все эти факторы значительно меняют сам подход к рождению детей. Сегодня вынашивание ребенка требует от женщины достаточно высокой компетентности в медицинских, социальных и даже правовых вопросах. Все большее значение приобретает подготовка к зачатию. Поэтому мировая медицина однозначна в своих рекомендациях: планирование любой беременности стоит начинать с консультации репродуктолога. Обращаясь в Клинику МАМА, вы можете быть уверены, что получите полный цикл диагностических и лечебных услуг европейского уровня.
Сделайте первый шаг — запишитесь на прием!
или позвоните +7 495 921-34-26 8 800 550-05-33 бесплатный телефон по России info@ma-ma.ru
Заболевание Синдром Дауна — это генетическая врожденная патология, считающаяся формой умственной отсталости. Дети с Синдромом Дауна медленно развиваются, обладают плохой памятью и визуально отличаются от сверстников. Некоторые пары решают родить такого малыша и с удовольствием его воспитывают. Других диагноз приводит в шоковое состояние и они принимают решение об аборте. Чтобы понять, как поступить, если УЗИ выявило у плода Синдром Дауна, давайте рассмотрим причины и последствия патологии.
Что такое Синдром Дауна
Патология подразумевает врожденную, генетически обусловленную, а значит неизлечимую, задержку физического и психического развития. У таких детей нарушается рост костей, что приводит к изменению строения тела.
У детишек с СД характерная внешность:
- маленькая округлая головка;
- раскосые, суженные, припухшие глаза, уши и нос меньше нормы, губы утолщены, язык удлиненный;
- рост низкий, укороченные пальцы;
- кожа отечная, волосы истончены;
- половые органы недоразвиты.
Умственное развитие человека с СД даже во взрослом возрасте сохраняется на уровне дошкольника — это главная причина, по которой многие семейные пары выбирают аборт.
При этом нужно отметить, что люди с этим диагнозом очень добрые, ласковые, любят животных и с усердием занимаются разными простыми делами. За открытость и беззлобие их называют «солнечными». Многие из пациентов могут себя обслуживать самостоятельно — одеваться, убирать за собой посуду. Некоторые считают и читают на уровне первоклашек. Но выжить без опекуна они не смогут.
Важные факты о синдроме Дауна
- Первым описал это заболевание английский врач Джон Даун, поэтому в названии патологии нет ничего оскорбительного — болезнь названа в честь великого ученого.
- Частота генетической аномалии не зависит от пола и выявляется с одинаковой частотой и у девочек, и у мальчиков.
- Большинство ученых считает, что СД — не наследственная патология, в одной семье могут быть и здоровые и больные дети. Но, врачи советуют с вниманием отнестись к случаям, если в роду уже рождались больные детки, и тщательнее обследоваться на ранних сроках беременности.
- Болезнь Дауна выявляется на сроках беременности до 12 недель на скрининговом УЗИ. Поэтому, проходя своевременно обследование на хорошем УЗ-аппарате, можно обнаружить патологию ещё в тот период, когда разрешен аборт.
- По статистике, значительными нарушениями мозговой деятельности, включая умственную отсталость, в разных формах страдает до 10% новорожденных малышей.
- Многие родители, родив «даунят», очень их любят и рады, что когда-то отказались сделать аборт. Некоторые семьи, напротив, устают от трудностей и распадаются. Мужчины уходят, устав от бесконечной опеки малыша, с которым приходится очень много и терпеливо заниматься.
Причины развития синдрома Дауна
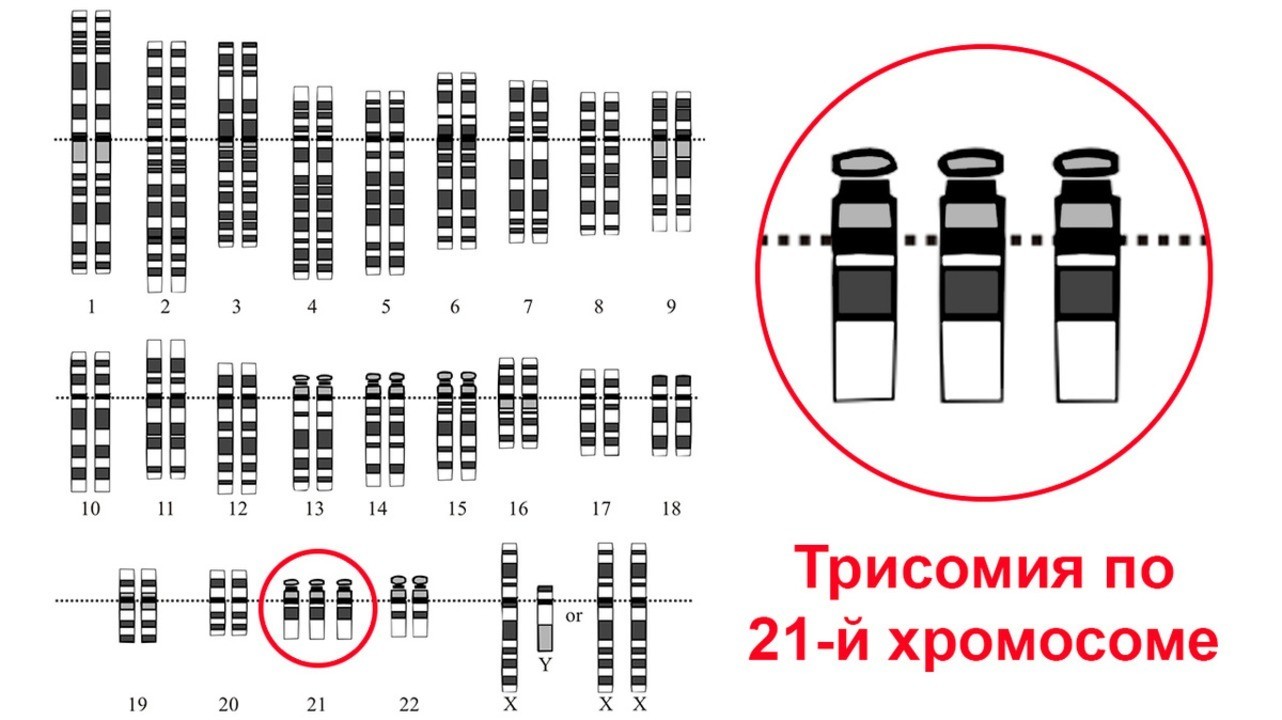
Истинная причина развития синдрома Дауна определена совсем недавно — у больных людей выявляется не 46, а 47 хромосом. Лишняя хромосома в кариотипе — результат нарушений в момент созревания и деления половых клеток.
Половая клетка делится, наделяя каждую из новых клеток 23-мя хромосомами. Если в этот момент одна из хромосомных пар не смогла разделиться (явление трисомии), остается лишняя хромосома. Чаще всего такая проблема возникает в возрастных браках — у женщин старше 35 лет, риск рождения малыша с синдромом Дауна повышен.
Группы риска, требующие обязательного скрининга на Синдром Дауна:
- Наличие в семье ребенка с генетическими заболеваниями или пороками развития;
- Наличие у одного из супругов или у кого-либо из близких родственников наследственных генетических и хромосомных заболеваний;
- Возраст женщины более 35 лет и/или возраст мужчины более 40 лет;
- Неблагоприятные условия жизни или профессиональной деятельности;
- Наличие в анамнезе спонтанных (самопроизвольных) абортов (выкидышей, привычных выкидышей) или замерших беременностей;
- Близкородственный брак;
- Прием лекарств на ранних сроках беременности, в т.ч. средств для медикаментозного аборта, антибиотиков,
Как выявляется СД — эффективная диагностика при беременности
В настоящее время все беременные, вне зависимости от наличия у них наследственных заболеваний, должны проходить скрининг плода на УЗИ и биохимическую диагностику. Всемирная Организация Здравоохранения (ВОЗ) рекомендует пройти хотя бы одну процедуру скрининга во втором триместре беременности.
Болезнь Дауна во время беременности можно определить несколькими методами:
- Скрининговое УЗИ плода. Доктор измеряет размер воротниковой зоны плода, определяя наличие подкожной жидкости, рост плода и другие параметры, характерные для разных генно-хромосомных патологий.
- Неинвазивная антенатальная диагностика — анализ крови с использованием биохимических маркеров. Кровь берут из вены и воздействуют на нее специальными веществами.
- Амниоцентез — исследование околоплодных вод. Методика требует вмешательства в организм, поэтому относится к инвазивным процедурам. Жидкость берут тонкой иглой через микроскопический прокол в животе и направляют на исследование.
При подозрение на СД нужно пройти минимум два типа диагностики, чтобы удостовериться в наличии патологии на 100% и только после этого принимать решение об аборте.
Результаты УЗИ анализируются вкупе с данными биохимического скрининга, позволяя более точно оценить вероятность наличия генетических аномалий у плода. Если по данным биохимического и УЗИ скрининга риски наличия того или иного генетического нарушения оказываются достаточно велики, назначается инвазивная процедура генетического анализа, которая дает результат с точностью, близкой к 100%. По результатам инвазивного анализа принимается решение о прерывании беременности.
Определение маркеров в крови беременной женщины
Биохимический скрининг подразумевает анализ крови матери, в котором выявляют определенные вещества, которые появляются при наличия генетических отклонений у плода. Их доля постоянно меняется в зависимости от срока беременности.
Биохимический скрининг проводится в два этапа:
- В первом триместре беременности – на содержание свободной β-субъединицы хорионического гонадотропина человека (ХГЧ) и плазменного протеина А, связанного с беременностью (PPP-A);
- Во втором триместре – на содержание ХЧГ или свободной β-субъединицы ХГЧ, свободного эстриола, ингибина А и альфа-фетопротеина (АФП).
Для каждого из перечисленных выше веществ есть некоторые нормы содержания в крови в зависимости от срока беременности. Отклонения в количестве маркеров от определенных норм не подтверждает на 100% генно-хромосомной болезни, а лишь указывает на высокий риск генетических пороков и аномалий. Поэтому, исследование дополняется результатами УЗИ плода. А если остаются сомнения, потребуется дополнительное обследование инвазивными методами.
Кроме данных анализов крови, при биохимическом скрининге учитываются также ряд общих данных о беременной (особенно важную роль играет возраст) и показания УЗИ, сделанного на том же самом сроке. Так или иначе, в качестве результата выдается лишь вероятность существования генетического заболевания у будущего ребенка. Достоверные сведения можно получить лишь в результате инвазивных процедур, то есть амниоцентеза, кордоцентеза или биопсии ворсинок хориона.
Амниоцентез, кордоцентез и биопсия хориона — инвазивные методы генетического скрининга
Если СД не выявлен до 15 недель (женщина пропустила сроки УЗИ, пренебрегала анализами), но есть подозрения на наличие патологии, гинеколог направляет беременную на неприятные инвазивные процедуры.
- Амниоцентез – метод генетического скрининга плода, выполняемый, начиная с 15-й недели беременности. Доктор берет амниотическую жидкость из матки, контролируя процесс на УЗИ. В амниотической жидкости содержатся клетки плода, поэтому после амниоцентеза есть возможность изучить непосредственно хромосомный набор будущего ребенка. Процедура практически безболезненна, но ее использование несколько повышает риск преждевременных родов и развития внутриутробной инфекции. Кроме этого, сам процесс очень неприятен для женщины, также как и ожидание результатов анализа.
- Биопсия ворсинок хориона. Врачи получают клетки околоплодной оболочки плода (хориона), которые генетически идентичны клеткам эмбриона. Риски инфекции и преждевременных родов сохраняются.
- Кордоцентез. Врач берет пуповинную кровь, в которой также содержатся клетки плода.
Полученный клеточный материал культивируют в лаборатории в специальных условиях примерно в течение 2-х недель и затем подвергают полному генетическому анализу. Исследования могут различаться в зависимости от назначений врача-генетика.
Существует более срочная диагностика клеток плода — флуоресцентная гибридизация (FISH), результат такого анализа обычно бывает готов в течение 2-3 дней. Однако возможности метода ограничены, и количество определяемых таким методом отклонений отличается от полного списка наследственных заболеваний. Методом FISH обычно определяют нарушения в количестве хромосом из 13, 15, 17, 18, 21, 22 пар хромосом, а также среди половых хромосом X и Y.
Точность инвазивных методов генетического скрининга составляет 97-99%.
Обязательно ли прерывать беременность?
Начнем с того, что делать или не делать аборт при Синдроме Дауна, женщина решает самостоятельно. Т.е. прерывать беременность в связи с патологией плода ее никто не заставит. Но гинеколог и генетик обязательно предупредят о последствиях — болезнь неизлечима и будет прогрессировать.
Некоторые женщины не хотят делать аборт, планируя сдать больного ребенка в детский дом. Если раньше достаточно было подписать отказ на малыша, теперь закон обязывает платить бессовестных мамаш алименты. Поэтому, произведя на свет ребенка с СД и отказываясь от него, жить счастливо и беззаботно не получится.
В какие сроки делается аборт, если у плода обнаружен СД
Если женщина решает сделать аборт, то его назначают в срочном порядке, чтобы провести его в щадящем режиме. Чем больше срок — тем больше возможных негативных последствий для психики и здоровья можно ожидать.
Нормальные сроки для аборта:
- До 6 недель — медикаментозный аборт. Выполняется с помощью приема таблеток, вызывающих выкидыш;
- До 7 недель — вакуумный аборт. Делается с помощью специального оборудования, не затрагивающего стенки матки;
- До 12 недель — хирургический аборт. Плод удаляют с помощью хирургического инструмента. Стенки матки выскабливаются.
Если сроки упущены, делают поздний аборт — допустимый срок до 22 недель гестации.
В случае, когда женщина решила сохранить беременность, все последующие обследования проводятся по стандартному плану. Роды также ничем не отличаются от обычных.
Синдром Дауна — это порок развития, одно из самых распространенных генетических заболеваний, встречается примерно 1 случай на 600-700 новорожденных. На вопросы пациентов о синдроме Дауна отвечают врачи медицинских клиник «Арт-Мед».
Помогите расшифровать результаты скрининга.
Мне 31 год. Беременность вторая. Вес 65 кг. Сдавала биохимию и делала скрининг на сроке по последнему дню м.ц.– 12,4 нед.
Результаты УЗИ:
КТР 56,6 мм
БПР 17,5 мм
ТВП 1,2 мм
Носовая кость визуализируется
ЧСС 165 у/мин.
Результаты биохимического скрининга:
ТВП 1,2 мм
РАРР-А 6,89 мЕд/мл (2,03 МоМ)
Св. бета ХГЧ 172,23 нг/мл (4,05 МоМ)
Результаты перинатального скрининга:
Возрастной риск синдрома Дауна (0,144%)
Индивидуальный риск синдрома Дауна (0,154%)
Результат скрининга на синдром Дауна — ниже популяционного
Риск трисомии 18 — ниже популяционного
Хоть риски и указаны ниже популяционного, но меня смущают завышенные ХГЧ и РАРР-А. Наблюдающий гинеколог звучала крайне не убедительно и не дала никаких рекомендаций (консультация генетика или повторный биохимический скрининг для уточнения результатов).
Окончательный результат биохимического и УЗ исследований, просчитанный программой I скрининг, не установил повышенного риска хромосомных аномалий.
Если Вас смущают повышенные значения индексов МоМ, Вы можете настоять на повторном исследовании.
В 12 недель носовая кость визуализируется 1.9 мм, про гипоплазию ничего не написано, остальные показания на этот момент: ТВП 1,4 мм, КТР 53 мм, ХГЧ 111,00 МЕ/л эквивалентно 2,440 МоМ, PAPP-A 1,790 МЕ/л эквивалентно 1,074 МоМ, Трисомия 21 (б)1:936 (и)1:18712, Трисомия 18 (б)1:2163 (и)
В вашем случае, у врача УЗИ диагностики не было оснований обозначить полученный размер, как гипоплазию. Рекомендуется проведение УЗИ в динамике, для оценки роста.
Мне 36 лет, мужу 41. Шестая беременность (2 роды, 1 выкидыш, 2 фармаборта). На сроке 19 недель и 3 дня делала второй скрининг(УЗИ). У ребёночка обнаружили 2 кисты в головном мозге и направили к генетику. Генетик рекомендует провести инвазивную диагностику (прокол), т.к. в факторе риска по возрасту, кисты и выкидыш в анамнезе. Оба скрининга в целом в норме(УЗИ и кровь), врач улльтразвуковой диагностики пишет, что вероятность отклонений низкая. Как быть? Соглашаться на процедуру, ведь и риски выкидыша, инфекций, подтекание Вод также присутствуют.
При инвазивных методах всегда оговариваются вероятные осложнения. Но – это единственно достоверные методы диагностики, поскольку на дообследования используется ткани плода. В любом случае, без Вашего согласия, никакие процедуры проводиться не будут.
Мне 31 год, моему мужу 35. Планируем беременность в ближайший год. Дело в том, что у мужа уже есть ребенок (7 лет) от другой женщины, и он родился с синдромом Дауна. Каков риск, что и у нас родится подобный ребенок? Как проверить, не паталогия ли это именно со стороны мужчины? Какую роль тут играет несовпадение резус-факторов? Какова подробная ситуация, не знаю, знаю только, что та женщина была на тот момент старше мужа на 9 лет.
Синдром Дауна в 97% случае – это результат случайной вновь возникшей мутации, поэтому от плода с таким диагнозом никто не застрахован. Риск повторения ситуации равен 0,7% + возрастной риск. Для исключения Вы можете определить Ваши с мужем кариотипы. А при наступлении беременности необходимо сделать 1 скрининг (биохимический + УЗИ), и на основании их результатов принимать решение об инвазивной диагностике.
Нам с супругом 41 год, первый ребенок рождён 14 лет назад, здорова. 2 беременности -медикаментозный аборт. Сейчас 4-ая беременность естественным путем. На 1-ом скрининге (12 недель 6 дней) по КТР. КТР 65,0 ТВП 1,7 БПР 19,0 ОГ 74,0 ОЖ 58,0. По УЗИ патологий не выявлено, хотя межтеменной размер меньше нормы! По биохимии ХГЧ 0,997 МоМ РАРР-А 0,222. Гипотериоз, гестационный сахарный диабет (под ?), После 4-х дней приема Л-Тироксин 50 по 1 таб сдала самостоятельно анализы в Инвитро: сахар и гормон щитовидной железы в норме. Возвращаясь к результатам скрининга: высокий риск аномалий у плода. Трисомия 21 базовый 1:56 индивидуальный 1:83, Трисомия 18 базовый 1:136 индивидуальный 1:196, Трисомия 13 базовый 1:427 индивидуальный 1:324. Задержка роста плода до 37 недель беременности 1:62. По передней и задней стенке матки миоматозные узлы. Показан ли амниоцентез (в данный момент сделали неинвазивный тест Прена Тест 21, ждём результаты) в нашем случае?
Первый скрининг в 12 недель показал носовую косточку 2 мм, шейная складка 1,5 мм, но по всем остальным показателям срок поставили 13-14 недель (13 недель +2), PAPP-A 2,21, fb-hCG-0,75. Второй скрининг в 20 недель носовая косточка 5,4 (Врач УЗИ сказала маловато, ниже нормы), а ребенок по всем показателям на 21-22 недели. Результаты анализа крови показывают низкие риски и в первом и во втором скрининге. Есть ли повод для беспокойства?
Вторая беременность 15 недель. Есть ребенок 10 месяцев, здоровая девочка. На сроке 11 нед 5 дней скрининг показал: КТР 50 мм, ТВП 1,6, кость носа осмотреть не удалось, внутренние органы в норме, цервикальный канал 46 мм, ХГЧ 1,777 МоМ, РАРР-А 0,208 МоМ, Uterine artery PI 0,940 MoM. Риск трисомии 21 1:60. Во время исследования была простужена. Есть вероятность, что результаты некорректны из-за болезни? И какова вероятность синдрома Дауна? Мне 26 лет.
ОРВИ, как правило, не влияет на результаты скрининга беременных. Риск трисомии 21 у плода примерно 1,5%. Это считается повышенным риском.
Генетические болезни – особый вид патологии, который имеет свои законы диагностики и терапии. Одним из ее видов является мозаичный синдром Дауна– сложное и интересное заболевание. С одной стороны, оно в определенной мере ущемляет и ограничивает человека, а с другой – способно раскрыть его безграничные возможности вопреки всем устоям.
ЧТО ТАКОЕ СИНДРОМ ДАУНА
В норме хромосомный набор человека содержит 23 пары или 46 хромосом. Но при определенных условиях 21 пара способна мутировать (чаще утраиваться), приводя к генетическому дефекту. Именно он и называется синдром Дауна.
Первый раз проявления болезни были зафиксированы в 1866 году врачом из Англии Джоном Дауном. Его имя и дало название синдрому. Однако зависимость между заболеванием и хромосомными парами установлена лишь в 50-х годах 20 века.
Википедия трактует данное понятие как геномное нарушение, при котором кариотип содержит 47 хромосом вместо привычных 46. Это происходит потому, что 1 из 23 пар хромосом — 21, вместо двух имеет 3 копии.
Но под данную трактовку подпадает самый распространенный вид дефекта – трисомия 21 пары, развивающаяся во всех клетках организма. Это самый тяжелый вид заболевания с ярко выраженными патологиями.
Другим вариантом синдромаявляется робертсоновская транслокация. Встречается она чуть реже, чем первый вариант. При ней 21 пара не утроена, а, наоборот, ее хромосомы склеены между собой, а общее количество хромосом составляет 45.
И, наконец, еще один вид патологии – мозаичный синдром Дауна. Его особенность проявляется тем, что пресловутая пара хромосом утраивается, но патология затрагивает только часть клеток.
МОЗАИЦИЗМ – ОБЩАЯ ХАРАКТЕРИСТИКА
Мозаичную форму синдрома Дауна еще называют мозаицизмом. Это редчайший тип данного заболевания, который проявляется в двух случаях из ста. Он характеризуется менее выраженными симптомами, то есть, можно сказать, что это легкая степень заболевания.
Она развивается на самой ранней стадии формирования зародыша, из-за чего в процесс вовлекаются не все клетки. Такая особенность этого вида патологии значительно осложняет ее диагностику.
Степень выраженности этого типа синдрома зависит от того, какие ткани и сколько вовлечены в процесс.
Детки с мозаичной формой синдрома Дауна в состоянии вполне нормально развиваться, их внешность может быть вполне гармоничной. Но некоторые особые признаки патологии имеются.
Отдельные трудности у таких детей развиваются в раннем возрасте. В этот период у малышей отмечается отставание в психомоторном развитии. При взрослении эти дефекты сглаживаются, и умственное развитие таких людей мало чем отличается от среднестатистических. Однако у них наблюдается своеобразное восприятие окружающего мира и нюансы речи, но подобные особенности встречаются и у обычных индивидов.
ПРИЧИНЫ И СПОСОБСТВУЮЩИЕ ФАКТОРЫ
Причин, по которым происходит мутация 21 хромосомной пары, существует несколько:
- патологическое зиготное деление;
- хромосомные расхождения во время митоза;
- перекомбинирование хромосом;
- наследование от родителей.
Подобные патологические изменения провоцируются рядом факторов:
- В первую очередь, это возраст родителей. Примечательно, что большее влияние здесь имеет возраст отца. Шансы родить больного малыша значительно повышаются после 35 лет.
- Инцест. Ребенок, рожденный вследствие половой связи между кровными родственниками, имеет высокую вероятность заполучить генетическое заболевание.
- Алкоголизм, курение, наркомания приводят к уродствам, в том числе и на хромосомном уровне.
- Наследственность, причем зачинщиками могут стать не только отец с матерью, но и ближайшие родственники. Некоторые ученые считают, что на возникновение синдрома влияет возраст бабушки, в котором она родила мать.
Болезнь не имеет половой, расовой и географической принадлежности. Она распространена по всему земному шару. А СД, как таковой, является самым распространенным генетическим заболеванием.
ВНЕШНИЕ ПРИЗНАКИ МОЗАИЧНОГО СИНДРОМА
Как уже было сказано, люди с подобной формой заболевания могут особо не различаться по развитию и внешности со своими сверстниками. Среди них есть даже очень привлекательные дети и взрослые.
Хотя, с другой стороны, многие носители этого дефекта имеют такие же признаки, как при часто встречающейся трисомии.
Дети с мозаичным синдромом Дауна часто маленького роста, и его увеличение происходит крайне медленно. Конечности непропорциональны по отношению к телу и имеют уменьшенные размеры.
В 90% случаев такие люди являются обладателями плоского лица и брахицефалии – укороченного черепа с плоским затылком. Шея, как правило, короткая с утолщенной кожной складкой. Подобный признак заметен уже в период новорожденности.
Характерные признаки лица у людей с подобным дефектом – плоская переносица и маленький нос, в 30% случаев возможно развитие страбизма (косоглазия).
Самое яркое проявление синдрома Дауна, которое сопровождает все его формы – это эпикантус. Данным понятием обозначают кожную складку, которая слегка нависает над внутренним краем глаза. Из-за такой особенности люди-дауны напоминают представителей монголоидной расы. И именно поэтому первооткрыватель дефекта назвал его изначально монголизмом, а больных – монголоидами.
К другим особенностям лица относят искаженное небо в виде арки и аномальные зубы. Данные дефекты и мышечная гипотония мешают закрыть рот, поэтому он всегда полуоткрыт. Язык у детей с мозаичной формой синдромабороздчатый. Вместе с готическим небом они затрудняют сосание, из-за чего такой ребенок плохо прибавляет в весе. Впрочем, для легкой степени заболевания, коим является мозаицизм, это характерно не всегда.
На радужке, по ее окружности могут присутствовать пигментные пятна Брушфильда. Еще одна особенность — аномальные уши, которые расположены ниже линии глаз. Они деформированы, часто оттопыриваются и могут вызывать проблемы со слухом.
Аномалии захватывают и опорно-двигательный аппарат. Они проявляются лабильностью суставов и деформацией костей. К примеру, грудина имеет килевидную форму. Патогномоничный симптом – клинодактилия или искривление мизинца. Деформируются также ребра и позвоночник. Это связано с недоразвитостью костной ткани.
Появление лишних кожных складок – частый признак даунизма. Они формируются из-за недоразвития костей, поэтому кожа между ними плохо натягивается. Кроме шейной, характерны также складки поперек ладони и в локтевом сгибе.
Внешние деформации часто становятся причиной нарушений в работе внутренних органов. Неправильная форма костей, гипотония мышц и другие особенности приводят к таким внутренним патологиям:
- аномалии развития сосудов и сердца;
- проблемы со зрением и слухом;
- нарушения органов пищеварения;
- недоразвитие почек;
- гипотиреоз.
Еще раз заметим, что у людей-даунов с мозаичным вариантом далеко не всегда все симптомы сочетаются. Многие из них не проявляются, что затрудняет распознавание заболевания.
ПСИХОМОТОРНОЕ И УМСТВЕННОЕ РАЗВИТИЕ
Дефекты в развитии детей с таким синдромом появляются по нескольким причинам:
- снижение зрения и слуха, из-за чего ребенок не в состоянии воспринимать информацию. Вследствие этого происходят и когнитивные нарушения;
- гипотонус мышц — малыши поздно начинают держать голову, переворачиваться, ходить. Страдает моторика;
- проблемы с опорно-двигательным аппаратом;
- деформация неба, зубов и языка вызывает речевые затруднения, поэтому речь таких людей может быть непонятной.
При мозаичной форме заболевания таких дефектов может и не быть, поэтому эти детки достаточно хорошо развиваются, их умственное развитие практически не страдает. Для них разрабатывают специальные программы, и здесь большая роль принадлежит родителям. От того, насколько качественно и стабильно они будут заниматься со своим ребенком, зависят его дальнейшие способности и успехи.
Дети с мозаицизмом очень способные к обучению. Они могут посещать обычный садик и школу, и даже преуспевать больше, чем некоторые их здоровые сверстники.
Их возможности, способности и развитие в целом очень разнятся. На форумах мамочки таких детей делятся своими достижениями и по-разному описывают своих малышей с подобным синдромом.
К примеру, одна мама говорит о том, что ее сын, которому уже 8 лет и который страдает мозаичной формой СД, до сих пор не разговаривает. Хотя они проходят реабилитацию в соответствующем центре.
Тогда как другая мама, у которой младший малыш имеет такое заболевание, утверждает, что он ничем не отличается от старшего, даже более находчивый.
Многие дети с мозаичным типом СД сублимируют свои дефектные особенности в невероятные достижения.
Айя Ивамото — девушка с мозаицизмом из Японии, родители которой рассказали о её болезни только на втором курсе института. Она посещала садик, успешно окончила школу и университет. Изучила два языка: английский и французский, и занимается иностранными переводами. Преподает в школах и вузах, принимала участие в международной конференции.
Совместно с мамой издала книгу о путешествии во Францию. Регулярно поддерживает и борется за права людей с синдромом Дауна.
Раймонд Ху – парень с мозаичным синдромом Дауна из США, который рисует картины с помощью старинной китайской техники. Он создает их акварельными красками и тушью на рисовом бумажном полотне.
В группу людей с подобным дефектом входит много актеров. К одной из наиболее известных таких личностей относится актер Пабло Пинеда. Ему досталась главная роль в фильме «Я тоже». Он также является частым гостем в различных телешоу, где освещает проблемы педагогики и развития детей.
Джейми Бауэр, сыгравший в «Американской истории ужасов», Паскаль Дюкенн, Крис Берк — все эти актеры имеют мозаичный синдром Дауна.
Люди с таким диагнозом находят себя в разных сферах жизни. Тим Харрис – владелец ресторана. Рональд Дженкинс – известный музыкант, приручивший синтезатор. Ему нет равных в электронной музыке. Мигель Томасин — популярный барабанщик, участник группы Reynols. Карен Гафнии – девушка, занимающаяся плаванием. Стала первой, кто преодолел дистанцию в 15 км. Вода при этом достигала температуры +15.
Глядя на такие примеры, сложно предугадать, как будет развиваться ребенок с мозаичной формой синдрома Дауна. Ясно одно: чтобы он стал успешным и развитым, нужна кропотливая работа как со стороны ребенка, так и его родителей.
КАК ДИАГНОСТИРОВАТЬ БОЛЕЗНЬ
Синдром Дауна можно распознать еще в пренатальном периоде, то есть во время беременности. Что касается его мозаичной формы, то в отдельных случаях его диагностика на данном этапе затрудняется ввиду скудности проявлений и поражении не всех хромосом. В таком случае его раскрывают только после родов.
Выявить заболевание удается несколькими методами:
1.УЗИ-диагностика. Ее проводят каждые 3 месяца беременности. Уже в первом триместре, с 8 по 12 неделю, можно распознать некоторые признаки СД. Например, утолщение воротниковой зоны.
2.Во втором триместре УЗИ покажет дефекты развития ЦНС, органов пищеварения, выделительной системы и слуха, а также сердечные пороки. На третьем УЗИ специалист увидит мелкие аномалии развития.
3.Анализ крови матери. Первый триместр (с 8 по 12 недели) определяет количество веществ, которые продуцирует плод:
- ассоциированный с беременностью плазменный протеин А (РАРР-А);
- хориогонадотропин человека (ХГЧ). Если уровень ХГЧ повышен, а РАРР-А понижен, это может говорить о патологии;
4.Второй триместр (с 18 по 21 неделю) определяет следующие показатели:
- альфа-фетопротеин;
- ХГЧ;
- свободный эстриол.
Подобные исследования не дают 100% гарантии наличия или отсутствия патологии. Если беременная попала в зону риска, то есть перечисленные анализы показали нестандартный результат, женщине проводят инвазивные процедуры. Они позволяют получить материал плода для уточнения диагноза:
- биопсия хориона – процедура дает возможность получить тканевые образцы плода. Ее осуществляют с помощью пункции брюшной стенки, а также через шейку матки специальными щипцами или катетером. Проводят на ранних сроках беременности, в 8—12 недель;
- амниоцентез – осуществляют в период 14—18 недель. Делают пункцию оболочки плода для забора околоплодных вод;
- кордоцентез проводится на поздних сроках вынашивания. Производят забор крови из пуповины.
Данные инвазивные методы являются довольно опасными, так как существует риск разрыва околоплодного пузыря, выкидыша, а также инфицирования матери и ребенка.
ПОМОГИ СВОЕМУ РЕБЕНКУ
Мозаичный вариант СД, несмотря на более легкое течение, требует постоянной работы с такими детьми. К сожалению, окончательно избавиться от патологии невозможно, но с помощью многопрофильной терапии можно помочь ребенку лучше адаптироваться к социуму и не чувствовать себя обделенным.
Очень важно для детей с синдромом Дауна проводить массаж и лечебную физкультуру. Они позволят повысить тонус мышц и укрепить их, устранят контрактуры, стабилизируют работу суставов и всего опорно-двигательного аппарата.
Массаж показан с 2 недель рождения. Но не все приемы позволительно использовать в этом возрасте. Разминание не применяется детям до 3 месяцев. Если у малыша есть проблемы с сердцем, следует проконсультироваться с врачом по поводу массажных приемов.
Из методов ЛФК обязательно используйте упражнения на мяче. Благодаря им происходит развитие двигательных рефлексов и координации.
Показаны для детей с СД занятия плаванием. Оно выполняет функцию гидромассажа.
Особо выделяют такие методы лечения, как иппотерапия и дельфинотерапия.
Иппотерапия – это терапевтическое воздействие, достигаемое при общении с лошадьми. Такой метод обеспечивает:
- развитие равновесия и внимания;
- придает уверенности в себе;
- тепло, которое исходит от лошади, успокаивает ребенка и дает ему чувство защищенности.
Это отличный метод, позволяющий уравновесить нервную систему людей с любым типом синдрома Дауна. Но он требует выполнения некоторых условий:
- Важно, чтобы лошадь была большая, а не пони. Они чрезмерно суетливы.
- Перед тем как сесть на лошадь, с ней нужно установить контакт: поговорить, покормить, погладить.
- Животное должно быть без седла и подков.
- Не рекомендуется кататься по асфальту.
Дельфинотерапия обеспечивает расслабление и улучшение настроения, придает уверенности в себе, помогает приобрести навыки общения. Этот метод также стимулирует физическое развитие. Ультразвук, который выделяют дельфины, восстанавливает нормальные биотоки.
К другим способам терапии относят:
- назначение медикаментозных средств — гормоны, психостимуляторы, нейрометаболиты, витаминные комплексы;
- консультации психолога и психотерапевта;
- диетотерапия — нередко такие больные страдают ожирением, которое способно приводить к другим патологиям. Поэтому следует соблюдать систему правильного питания, чтобы предотвратить чрезмерный набор веса;
- постоянное наблюдение у узких специалистов.
ПСИХОМОТОРНОЕ РАЗВИТИЕ
Обучение людей с синдромом Дауна – очень благодарное дело. Каждое достижение приносит им чрезвычайно много радости. Они с большим энтузиазмом подходят к этому процессу, прилагая немало усилий.
С самого раннего возраста люди с СД требуют пристального внимания и тщательной работы с ними. Дети с мозаичной формой по своему развитию приближены к норме, но все-таки имеют некоторые особенности, которые нужно корректировать.
Следует понимать, что мышление у таких детей немного иное. Оно более инертное, нередко такому малышу сложно сконцентрироваться, ему не хватает усидчивости. Поэтому к процессу их обучения нужно подходить творчески, лучше в игровой форме.
Новую информацию им следует преподносить короткими фразами, повторяя их по несколько раз, так как кратковременная память развита недостаточно. Но главное, делать это интересно и увлекательно. Учитывайте, что такие ученики быстрее других утомляются, поэтому следует делать перерывы в процессе занятий, чередовать умственную деятельность с физической.
Проблемы со слухом и зрением также снижают способность воспринимать информацию, замедляют учебный процесс. Это также следует учитывать, и подстраивать занятия под эти особенности.
Следует обращать внимание на развитие образного и абстрактного мышления: разъяснение утверждений и понятий, предъявление доказательств, расположение предметов в пространстве, их классификация и т.д.
Речь у детей с СД может быть неразборчивой и скудной. Это проблема требует занятий с логопедом. Это позволит правильно поставить речь и сделать ее более доступной для понимания.
Важно развивать моторику, ведь она дает возможность детям обслуживать себя в быту. Мышечная слабость снижает способность манипулировать ладонью и пальцами. Их следует разрабатывать. Например, можно использовать упражнение, при котором кисть фиксируется на поверхности стола на ребре ладони. При этом рисование выполняется 3 пальцами, исключая мизинец и безымянный.
Разрабатывать кисти можно с помощью различных приемов:
- сжимать кулаки, имитировать пинцетный захват и в виде щепотки. Поочередно дотрагиваться всеми пальцами руки до большого пальца;
- рисование, в том числе пальчиковое, в разных плоскостях — в строго горизонтальной или вертикальной, под острым или тупым углом;
- лепка из любого материала — пластилин, глина, тесто;
- играть в ладушки;
- разрыв газеты;
- перелистывание страниц книги;
- использование подручных средств — раскладывать пуговицы по разным категориям, собирать их на нитке, изготавливать украшения. Можно сортировать и пересыпать крупы. Но здесь важна умеренность, чтобы не утомить маленького ученика. Применимы также манипуляции с банками и крышками;
- складывание мозаики и пазл. Но следует подбирать подходящие для возраста ребенка объекты, чтобы он мог самостоятельно их собрать;
- работа с ножницами, выкладывание аппликаций. Создание выкроек;
- обучайте малыша самостоятельно одеваться, совладать со шнурками, молнией, пуговицами. Можно тренировать его с помощью куклы.
Занимаясь с детьми подобным образом, можно не только обучить их физическим навыкам — это обеспечивает непосредственное общение с малышом, стимулирует его психическое и умственное развитие.
Существуют специальные методики, которые дают направление в обучении детей-даунов:
- Метод Зайцева. Автор разработал специальные кубики, таблицы и музыкальное сопровождение, которые призваны обучать навыкам чтения. Это, в свою очередь, влияет на качество письма в дальнейшем и сглаживает интеллектуальные проблемы.
- Методика Монтессори. Его суть – создать обстановку, в которой малыш будет заниматься по собственному желанию. Он сам выбирает себе род занятий из предложенного ассортимента. Как правило, обучение ведется в игровой форме.
- Метод Никитиных — легкость и свобода в обучении, непринужденная обстановка. Упор делается на физическом развитии и закаливании. Все игровые принадлежности должны иметь обучающую основу.
- Методика Глена Домана — начинать обучение с самого раннего возраста. Уже с 1 года жизни развивать речь, преподавать основы счета и чтения.
- Методика Сесиль Лупан — преподносить информацию ребенку так, чтобы заинтересовать его, чтобы он сам стремился к обучению. Для этого постоянно предлагать что-то новое, постепенно стимулируя его и самому расширять свои познания. Главные критерии – любознательность и самостоятельность.
Очень важны коллективные занятия, при которых дети тянутся и ориентируются друг на друга.
ВЗГЛЯД В БУДУЩЕЕ
Ученые постоянно ведут исследования в области генетических заболеваний, ищут новые эффективные методы их диагностики и лечения.
Так, ученые из США разработали компьютерную программу, с помощью которой можно определить легкую степень синдрома Дауна и других подобных патологий по фотографии, когда эти признаки не видны вооруженным глазом. Программа сканирует фото, и выдает даже те нюансы, которые не видит специалист.
Английские ученые разработали метод определения синдрома по анализу крови беременной. Исследование проводилось среди более 2 тыс. женщин и проявило точность до 99%. Данный анализ базируется на определении лишней хромосомы. Он способен заменить даже небезопасные инвазивные методы диагностики мозаичного синдрома Дауна.
В среднем, люди с данной патологией живут до 50 лет, а при легкой степени — и больше. Женщины способны к зачатию при всех формах болезни. У мужчин повышается эта способность при мозаичном варианте. Союз таких людей дает высокую вероятность рождения ребенка с синдромом Дауна. Но, тем не менее, остается небольшой процент вероятности появления здорового малыша.
Мозаичный синдром Дауна – это патология, которая легко поддается корректировке. Такие люди могут мало отличаться от здорового населения. Некоторые из них даже становятся успешными в жизни, проявляя невероятные умения и способности.
Мы должны понимать, что эти «особенные» люди – часть нашего социума. Они, как никто другой, нуждаются в поддержке и заботе, а главное, во внимании!
Вся информация взята из открытых источников.
Если вы считаете, что ваши авторские права нарушены, пожалуйста,
напишите в чате на этом сайте, приложив скан документа подтверждающего ваше право.
Мы убедимся в этом и сразу снимем публикацию.
13 Янв Скрининг показал риск синдрома Дауна у плода
Мне сорок лет, четвертый ребенок. Во время беременности на скринингах мне поставили высокий риск Синдрома Дауна у малыша — сначала 1:6, потом 1:4 и 1:2.
Высокий риск считается уже от 1:250, поэтому, когда я увидела эти цифры, у меня потемнело в глазах.
На УЗИ носовую кость сначала не видели, а потом она была значительно меньше нормы: в два раза меньше самого минимального значения.
Я бросилась искать информацию о синдроме, рисках и вообще всем, что с этим связано. Информацию собирала в интернете на сайтах и форумах, что-то мне рассказывали люди, которые воспитывали или общались с детками, у которых такой синдром.
Я хочу поделиться своим опытом, потому что возможно кто-то также, как и я, окажется в ситуации, когда не знаешь, что делать, у кого спрашивать, и от этого незнания голова разрывается на части. Эмоциональную сторону я намеренно опущу, потому что то напряжение, в котором я была эти полгода, описать невозможно.
Первый скрининг делается на сроке 11-13 недель и включает в себя УЗИ и анализ крови на ряд показателей. На УЗИ смотрят воротниковую зону, носовую кость, кровоток.
У меня носовую кость на тринадцатой неделе не обнаружили и отправили в ЦПСИР переделать через неделю. Через неделю кость также не увидели. Все другие показатели были в норме. В анализе крови при учете первого УЗИ ХГЧ была чуть выше нормы (2,57 при норме 0,5- 2,5 моль), при учете второго УЗИ – 2,7 моль. Повышенный ХГЧ также считается маркером СД у ребенка. Меня отправили к генетику тут же в соседний кабинет. Генетик очень сухим языком еще раз повторила цифры и рекомендовала сделать амниоцентез, то есть анализ, когда иглой берется амниотическая жидкость и считают хромосомы.
На более ранних сроках, 9-13 недель, делают биопсию хориона, но я уже не успевала. На более позднем – после 22 недель – кардоцентез, когда берут кровь из пуповины ребенка.
Что я поняла уже постфактум: после 35 лет коэффициент риска с каждым годом сильно возрастает. То есть в мои 40 лет он уже 1:75 просто априори без анализов и УЗИ. А в 48 лет он будет гораздо больше. При норме УЗИ на чуть повышенный хгч никто бы не обратил внимания, но 40 лет, отсутствие носовой кости и 2,7 вместо 2,5 моль в итоге превратились в риск 1:4.
Я сделала неинвазивный тест — сдала анализ крови Пренетикс на определение распространенных хромосомных аномалий. Результат пришел отрицательный. Я решила не делать амниоцентез, хотя сдала все анализы и была готова. На следующий день мы улетали, а это все-таки маленькая операция, рекомендуется покой и есть небольшая, но угроза выкидыша. Я читала о таких случаях, причем, когда женщина теряла здорового ребенка. Плюс я приняла решение оставить малыша в любом случае, и результат бы уже ничего не решил.
Первый раз носовую кость увидели на экспертном УЗИ в 16 недель, она была 2 мм и отставала где-то на месяц.
Все это время я мониторила интернет и искала информацию. На одном из форумов был опрос мам, у которых родились дети с СД, о том, когда они узнали о диагнозе. Результаты получились примерно такие: 40% мам имели риски на скрининге или даже знали о диагнозе, сдав анализ, но решили рожать. У 40% и скрининг, и УЗИ были в норме. И 20% не делали никаких исследований.
В интернете я нашла несколько ложноположительных результатов неинвазивных тестов, но ни одного ложноотрицательного. У одной моей знакомой были плохие целых два анализа – биопсия хориона и неинвазивный тест, показавший не СД, но другую патологию. Только амниоцентез снял все риски.
Когда я пришла в ЦПСИР на второй скрининг в 21 неделю, меня отругали, что я отказалась от амниоцентеза, сказали, что неинвазивные тесты — это ерунда и таких ложноотрицательных результатов бывает достаточно. В частности, есть мозаичная форма СД, когда часть клеток имеют дополнительную 21ую хромосому, а часть нет, и эту форму могут не диагностировать, если в анализ попадут клетки с обычным рядом хромосом. На этом скрининге носовая кость была 5,1 мм при минимуме 5,7, и риск уже 1:2. В 32 недели носовая кость была в два раза меньше допустимого минимума.
В роддоме на УЗИ уже перед родами меня стали пугать, что у ребенка гиперэхогенный кишечник, что является одним из маркеров генетических патологий, но срок уже был 41 неделя и, скорее всего, в кишечнике у ребенка был меконий.
Также говорили, что неинвазивный тест надо было делать развернутый, не на четыре распространенные патологии, так как гипоплазия носовой кости (слишком маленькая кость) — это маркер не только СД, но и других генетических отклонений.
Первой моей фразой после рождения ребенка была: «Есть ли у него нос?».
Нос был, причем вполне приличный.
Родился обычный ребенок.
Я сейчас задаю себе вопрос: а нужны ли эти скрининги? Я понимаю, что есть другие патологии, кроме Синдрома Дауна, более сложные и опасные, и, возможно, для их диагностики на раннем сроке скрининг очень важен. Но сколько женщин с риском СД у ребенка решили не ждать 16 недель и амниоцентеза и сделали аборт, чтобы не упустить время?
Амниоцентез делается на сроке 16-18 недель, какое-то еще время нужно для получения результата. В итоге срок уже большой и женщину отправляют на искусственные роды. Я даже писать не буду о том, как они происходят: это страшно.
Что бы я точно добавила в том же ЦПСИРЕ или консультациях — это должность психолога, который должен сидеть в кабинете рядом с генетиком и по-человечески объяснять и рассказывать женщине все за и против в любом решении, которое она примет.
Мне повезло — рядом оказались люди, которые поддержали меня, рассказали, что даже если риск подтвердится и у ребенка будет СД — это не так страшно, как описывают врачи по старым исследованиям, проводившимся в интернатах, где и обычные дети не будут психологически здоровыми. Но скольких женщин, особенно в глубинке, убеждают делать аборт при риске, значительно меньшем, чем у меня?
Что касается финансовой стороны исследований: все скрининги, инвазивные анализы, амниоцентез и другие делаются бесплатно в рамках ОМС, неинвазивный пренатальный тест «Пренетикс» стоил 29 000 рублей, периодически на него бывают скидки до 10 000 рублей. Расширенный анализ будет стоить около 60 000 рублей. Также и неинвазивные, и инвазивные анализы определяют пол ребенка.
За экспертное УЗИ я заплатила 5500 рублей.
Очень надеюсь, что все, написанное выше, поможет не унывать женщинам, которые оказались в ситуации, похожей на мою. Риск — это всего лишь риск, а не диагноз. И машина, и люди могут ошибаться.
Анастасия А.
Что такое синдром Дауна?
Синдром Дауна — это генетическое заболевание, при котором в результате случайной мутации в 21-й паре хромосом получается третья копия. В норме у здорового человека — 23 пары хромосом, каждая содержит индивидуальный набор генов. Любое изменение их количества (недоразвитие одной пары, появление третьей хромосомы в паре, удвоение пары) и качества (всевозможные изменения внутри самой хромосомы) приводит к необратимым врожденным нарушениям развития человека.
По данным фонда «Даунсайд Ап», в России ежегодно рождается около 2500 тыс. детей с синдромом Дауна. 85% семей отказываются от них еще в родильном доме, в том числе и по рекомендации медицинского персонала.
В случае с синдромом Дауна дополнительная хромосома становится причиной некоторых особенности во внешности и патологий внутренних органов. Чаще всего затрагивается сердечно-сосудистая система и желудочно-кишечный тракт. Степень проявления симптомов отличается у разных людей, но все больные имеют пожизненную умственную отсталость и задержку развития. Несмотря на это, люди с синдромом Дауна могут учиться, работать, заниматься спортом, сдавать экзамены на водительские права, играть в театре и участвовать в конкурсах красоты².
В последние десятилетия отмечается рост заболеваемости синдромом Дауна. Это связано с увеличением возраста беременных женщин и отрицательным влиянием факторов окружающей среды на здоровье человека. За период с 1979 по 2003 заболеваемость синдромом Дауна в США увеличилась на 30%¹.
В России помощь детям и взрослым с синдромом Дауна оказывают такие проекты, как «Синдром Любви», фонд «Даунсайд Ап» и другие. Они организовывают денежные сборы, проводят тематические встречи, акции в поддержку своих подопечных, помогают ребятам с трудоустройством.
Факторы риска рождения ребенка с синдромом Дауна
Нет конкретной причины, которая в 100% случаев приводит к рождению ребенка с синдромом Дауна. Однако есть факторы риска, которые увеличивают вероятность появления таких детей. К ним относят:
- Возраст матери. Риск зачатия ребенка с синдромом Дауна увеличивается у женщин после 35 лет, так как с годами яйцеклетки имеют склонность к неправильному делению хромосом. Так, по данным Национального общества синдрома Дауна (США), в 35 лет у женщины риск зачатия больного ребенка составляет 1: 350 случаям, 1: 100 — к 40 годам и достигает 1: 30 в 45 лет. Согласно некоторым исследованиям4, возраст отца также является фактором риска: в исследуемой группе у мужчин после 40 лет вероятность рождения ребенка с синдромом Дауна увеличилась в 2 раза. Однако этот фактор пока менее изучен.
- В семье уже есть ребенок с синдромом Дауна. Риск в этом случае значительно увеличивается. При планировании беременности оба родителя направляются к консультанту-генетику, который назначит дополнительное обследование, проанализирует конкретно их ситуацию и сможет оценить риски более точно.
- Один из родителей является мозаиком или носителем транслокации. 7-8% детей с синдромом Дауна имеют транслокационную или мозаичную форму синдрома. Небольшая их часть унаследовала транслокацию от родителей, несмотря на то, что признаков и симптомов синдрома Дауна у отца и матери не было.
Лечение
Вылечить синдром Дауна невозможно. Терапия направлена на патологические состояния, обусловленные самим синдромом. Проводится хирургическая операция при врожденных пороках развития, лечатся инфекционные заболевания, корректируются офтальмопатологии, метаболические нарушения и др. Все это проводится при участии группы врачей-специалистов — посещать их дети с синдромом Дауна должны регулярно.
В 2011 году Американская Академия педиатрии (AAP) по медицинскому наблюдению детей с синдромом Дауна разработала методические рекомендации, в которых описан возрастной рутинный скрининг ребенка с синдромом Дауна. Его цель заключается в ранней диагностике сопутствующих патологий:
- Эхокардиография: во время пренатальной консультации или сразу после родов.
- Исследование щитовидной железы (уровней тиреотропного гормона (ТТГ): проводится при рождении, в 6 месяцев, в 12 месяцев, а затем ежегодно.
- Оценка слуха: при рождении, затем каждые 6 месяцев до момента, пока не будет подтвержден нормальный слух (около 4 лет), после чего ежегодно.
- Офтальмологическая оценка: к 6 месяцам, затем ежегодно до 5 лет; затем каждые 2 года до 13 лет и каждые 3 года до 21 года.
- Физическое развитие: рост, вес и окружность головы определяют при каждом обследовании с использованием ростовой шкалы для синдрома Дауна.
- Исследование сна при синдроме обструктивного апноэ во сне: завершается к 4 годам.
Кроме узких специалистов, важнейшую роль в жизни особенного ребенка играют специалисты профилактического профиля: логопеды, физиотерапевты, врачи-реабилитологи, дефектологи, массажисты и т.д.
Синдром Дауна — не помеха для успеха
Люди, ставшие известными, своим примером показывают, что и с синдромом Дауна можно реализовать себя в жизни и добиться успеха.
- Каррен Гафни. Руководит некоммерческой организацией, которая занимается адаптацией в обществе детей с ограниченными возможностями. Левая нога у Каррен парализована, но она стала первым человеком с синдром Дауна, сумевшим переплыть Ла-Манш. Завоевала золотую медаль на Паралимпийских играх, а недавно получила диплом почетного доктора Университета Портленда в штате Орегон.
- Пабло Пинеда. Испанский актер, в 2009 году получивший «Серебряную раковину» кинофестиваля в Сан-Себастьяне — за лучшую мужскую роль в фильме «Я тоже». Живет в Малаге, работает в муниципалитете, преподает, имеет несколько дипломов: преподавателя, бакалавра искусств и диплом в области педагогической психологии.
- Рональд Дженкинс. Молодой мужчина с синдромом Дауна, музыкант и композитор. Рональд начал заниматься игрой на пианино в четыре года. В 17 лет стал выкладывать свои ролики на Youtube под псевдонимом Big Cheez. Тогда же у него вышел первый альбом — Straight Laced by Fish.
- Паула Саж. Родилась в Шотландии в 1980 году. Снялась в нескольких фильмах, профессионально играет в нетбол, стала адвокатом. Паула оказывает юридическую поддержку двум международным фондам — Ann Craft и Mancap.
- Мелани Сегард. Девушка мечтала стать ведущей прогноза погоды. Подруга посоветовала ей снять небольшой ролик с рассказом о себе и выложить в соцсети. За несколько дней ее мечту поддержали более 180 тысяч человек, а сейчас у страницы свыше 255 тысяч подписчиков. Через неделю мечта Мелани исполнилась — она получила предложение от двух национальных каналов, и теперь рассказывает о погоде.
Характерные признаки и симптомы
Люди с синдромом Дауна могут вести себя одинаково и быть похожими друг на друга, но у каждого будет различная степень выраженности симптомов. Из общих можно выделить показатель интеллекта (IQ) в диапазоне от умеренного до низкого, более медленную речь, чем у других детей, некоторые физические особенности.
Внешние признаки синдрома Дауна:
- уплощенное лицо, особенно переносица;
- раскосые миндалевидные глаза, эпикант — вертикальная складка века у внутреннего угла глаза;
- небольшие белые пятна (пятна Брушфильда) на радужной оболочке глаза;
- язык, который часто виден из приоткрытого рта;
- короткая шея;
- маленькие уши;
- одна ладонная складка вместо двух;
- низкий рост;
- низкий мышечный тонус и слабые суставы.
Кроме внешне видимых особенностей физического развития, при синдроме Дауна наблюдают различные патологии внутренних органов³.
Часто встречаются пороки сердца: примерно у половины детей с синдромом Дауна есть какий-либо врожденный порок. Если возникает угроза для жизни, то в первые недели после рождения младенцу проводят кардиохирургическую операцию. Кроме пороков сердца, у некоторых детей формируются аномалии развития желудочно-кишечного тракта: кишечника, пищевода, заднего прохода. Возрастает риск развития проблем с пищеварением, таких как непроходимость желудочно-кишечного тракта, изжога (гастроэзофагеальный рефлюкс) или целиакия. Из-за сбоев в работе иммунной системы люди с синдромом Дауна имеют повышенный риск развития аутоиммунных и инфекционных заболеваний, некоторых форм рака.
Изменения мягких тканей и скелета могут привести к обструкции дыхательных путей, из-за чего как у детей, так и у взрослых может возникать апноэ (остановка дыхания во сне).
Также из-за особенностей метаболизма и работы эндокринной системы люди с синдромом Дауна чаще страдают ожирением по сравнению с населением в целом.
Диагностика синдрома Дауна
Диагноз ставится на основании характерной клинической картины — совокупности внешних признаков, наблюдения за темпами физического и интеллектуального развития ребенка, наличия патологии внутренних органов. Новорожденных проверяют на синдром Дауна, когда есть показания — в частности, если на него указывают внешние признаки. Диагноз подтверждается кариотипированием — исследованием хромосом ребенка на наличие измененного кариотипа.
Кроме того, исследуются функции внутренних органов, которые часто бывают нарушены при синдроме Дауна — щитовидной железы, зрительного, слухового анализаторов. Выявляются возможные пороки сердца, лейкемия. С этой целью ребенку назначают УЗИ-обследование органов брюшной полости и сердца, консультации врачей-специалистов: детского кардиолога, хирурга, офтальмолога, травматолога-ортопеда.
Женщины во время беременности проходят следующие исследования: скрининговые — они обязательные для всех и специальные, которые назначаются врачом по показаниям. Обследования направлены на выявление различных заболеваний и генетических аномалий у плода (в том числе и синдрома Дауна, одного из самых частых генетических нарушений).
Пренатальная диагностика
Общая схема пренатальной диагностики выглядит так:
1. В первом триместре беременности:
- Хорионический гонадотропин человека (ХГЧ) — гормон, который вырабатывается оболочкой зародыша и участвует в поддержании беременности.
- Ассоциированный с беременностью протеин А плазмы (РАРР А). Аномальный уровень ХГЧ и РАРР-А может указывать на нарушения развития плода.
- Ультразвуковое исследование — позволяет выявить специфические УЗИ-признаки аномалии у плода.
2. Во втором триместре беременности:
- УЗИ-диагностика.
- Альфа-фетопротеин (альфа-ФП) — низкий уровень может указывать на синдром Дауна.
- Бета-субъединица хорионического гонадотропина человека (бета-ХГЧ). Повышение концентрации ХГЧ в некоторых случаях связано с заболеванием ребенка.
- Эстриол свободный. Низкий уровень эстриола бывает признаком синдрома Дауна.
Результаты УЗИ, РАРР-А, альфа-ФП, ХГЧ и эстриола в сочетании с данными о возрасте и наследственности матери позволяют рассчитать риск рождения ребенка с синдромом Дауна.
Данные пренатального исследования особенно важны для женщин, входящих в группу риска по рождению детей с синдромом Дауна. Если риск оказался очень высоким, могут быть назначены следующие инвазивные (с нарушением кожных покровов) исследования:
- Амниоцентез — взятие образца околоплодных вод и последующее изучение хромосом плода.
- Биопсия хориона — получение образца ткани хориона (наружной зародышевой оболочки, окружающей эмбрион). Также позволяет выявить хромосомные аномалии.
- Пуповинное взятие крови — тест проводится, если предыдущие исследования оказались неэффективны.
Женщинам с предрасположенностью к заболеванию во время планирования беременности рекомендуется генетическая консультация.
Причины развития синдрома Дауна
В норме клетки человека содержат 23 пары хромосом. Одна хромосома из пары принадлежит отцу, другая — матери. Синдром Дауна возникает, когда в 21-ой паре вместо двух хромосом получается три. Дополнительный генетический материал отвечает за характерные особенности и проблемы развития у ребенка. Существуют три генетических вариации формирования синдрома.
Классический вариант синдрома Дауна — это трисомия 21, когда каждая клетка в организме имеет по три копии 21-й хромосомы вместо обычных двух.
Есть и другие варианты. В некоторых случаях синдром возникает, когда часть 21-й хромосомы прикрепляется к другой хромосоме во время формирования яйцеклеток и сперматозоидов у родителя или на очень раннем этапе развития плода. Тогда у человека есть две нормальные копии и дополнительная часть хромосомы 21, прикрепленная к другой хромосоме. В результате получаются те же три копии генетического материала. Такая форма называется транслокационной.
Небольшой процент людей с синдромом Дауна(1-2%) имеет дополнительную копию хромосомы 21 только в части клеток организма. Это называется мозаичным синдромом Дауна.
Видео 1. Причины, симптомы и диагностика синдрома Дауна.
Классификация
По механизму развития синдрома Дауна, выделяют три формы:
- Трисомия по 21-ой хромосоме.
- Транслокационная форма синдрома Дауна.
- Мозаичная форма синдрома Дауна.
На первую форму приходится около 95% случаев заболевания и до 5% — на две другие.
Прогноз для людей с синдромом Дауна
Продолжительность жизни людей с синдромом Дауна значительно увеличилась. Так, в 1960 году ребенок с синдромом Дауна часто не доживал до своего 10-летия. Сегодня ожидаемая продолжительность жизни людей с этим заболеванием составляет 50-60 лет.
Видео 2. Люди с синдромом Дауна отвечают на вопросы, рассказывают об отношении к ним окружающих, о семье, любви, своих мечтах и планах на будущее.
Возможности обучения и социализации лиц с синдромом Дауна различаются. Во многом они зависят от интеллектуальных способностей ребенка и от усилий, прилагаемых родителями и педагогами. Почти во всех случаях детям с синдромом Дауна удается привить бытовые и коммуникационные навыки, необходимые в повседневной жизни. Есть пациенты, добившиеся успеха в области искусства, актерского мастерства, спорта, а также в получении высшего образования. Взрослые с синдромом Дауна могут вести самостоятельную жизнь, овладевать несложными профессиями, иметь свою семью.
Поддержка опытных профессионалов (врачей, реабилитологов, психологов, социальных педагогов) и понимание семьи и друзей имеют решающее значение для людей с синдромом Дауна. Во многих странах существуют сообщества больных, где родители таких детей и сами дети, а также взрослые с синдромом Дауна могут получить поддержку, обсудить насущные проблемы, поделиться своими успехами.
Заключение
Синдром Дауна — одно из самых распространенных хромосомных заболеваний, при котором у плода возникает дополнительная копия в 21-й паре хромосом. Риск зачатия больного ребенка повышается у женщин после 35 лет. На сегодняшний день лечения нет, однако при ранней социализации, участии в программах психологической реабилитации люди с синдромом Дауна имеют возможность жить активной и полноценной жизнью.
Источники
- Shin M, Besser LM, Kucik JE, Lu C, Siffel C, Correa A. Prevalence of Down syndrome among children and adolescents in 10 regions of the United States. Pediatrics. 2009 Dec;124(6):1565-71.
- Виктор Вайц. Люди с синдромом Дауна в Германии: «Мы — не больные, мы — другие!» [Электронный ресурс] // dw.com, 2020.
- Down syndrome [Электронный ресурс] // mayoclinic.org, 2018.
- Down syndrome [Электронный ресурс] // healthline.com